Андрей Иорданишвили - Стоматологические конструкционные материалы: патофизиологическое обоснование к оптимальному использованию при дентальной имплантации и протезировании.
- Название:Стоматологические конструкционные материалы: патофизиологическое обоснование к оптимальному использованию при дентальной имплантации и протезировании.
- Автор:
- Жанр:
- Издательство:Array Литагент «Нордмедиздат»
- Год:2011
- Город:Санкт-Петербург
- ISBN:978-5-98306-092-0
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Андрей Иорданишвили - Стоматологические конструкционные материалы: патофизиологическое обоснование к оптимальному использованию при дентальной имплантации и протезировании. краткое содержание
При клиническом исследовании изучены местные и общие осложнения зубного протезирования в различные сроки после его завершения. Выявлены причины и проведен анализ динамики течения периимплантитов, а также состояния мягких и костной ткани альвеолярного отростка челюсти при различном использовании временных коронок из акриловых пластмасс в ближайший период после дентальной имплантации.
Стоматологические конструкционные материалы: патофизиологическое обоснование к оптимальному использованию при дентальной имплантации и протезировании. - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Оксидный слой на поверхности титана определяет также его умеренно выраженные остеокондуктивные свойства. Многочисленные исследования показали, что на нем происходит адгезия и связывание белков, а также ионов кальция и фосфора [Д. Вильяме, Р. Роуф, 1978; Ф. Вортингтон, Б. Ланг, В. Лавелле, 1994;. C Stanford, J. Keller, M. Solursh, 1994].
Таким образом, оксидная пленка является базой для формирования остеокондуктивной матрицы, на которой может осуществляться митоз остеогенных клеток и последующая жизнедеятельность остеобластов и остеоцитов [K. Bowers, J. Keller, 1991; L. Cooper et al., 1999].
В хирургии титан широко используется с 1952 г., хорошо изучен и является основным материалом для производства различных имплантатов.
Материал для внутрикостного имплантата может считаться биосовместимым, если на его поверхности происходит формирование кост-ной ткани и создаётся интерфейс, способный к адекватному распределению функциональной нагрузки на окружающие имплантат ткани [L. Hench, R. Splinter, W. Allen, T. Greenlee, 1972; P. Ducheyne, 1987].
Исходя из этого определения, материал, пригодный для изготовления внутрикостных имплантатов, должен обладать определёнными физико-химическими, биологическими, биохимическими и биомеханическими свойствами.
Физико-химические свойства имплантационных материалов
С физико-химической точки зрения материал имплантата не должен:
– растворяться;
– подвергаться коррозии и структурным изменениям в жидких средах организма, а также остеокластической резорбции или иной деградации, связанной с жизнедеятельностью клеток организма;
– вызывать нежелательные электрохимические процессы в тканях и на поверхности раздела имплантат/окружающие ткани.
Растворимость и деградация материалов
Растворимость кальций-фосфатных соединений, как и других биоактивных материалов, очень мала и составляет 1,0x10 9моль/дм 3. Ещё меньшей растворимостью обладают стекло и ситаллы [Ершов Ю.А. и др., 1993]. Однако биоактивные материалы подвергаются остеокластической резорбции и, таким образом, являются биодеградируемыми.
Биоинертные и биотолерантные материалы можно считать практически нерастворимыми. Например, растворимость поверхностного оксидного слоя титана в физиологическом растворе составляет всего 0,043 нм в день [K.D. Allard, M. Ahrens, K. Heusler, 1975].
Таблица 3
Сроки биологической деградации биоактивных материалов
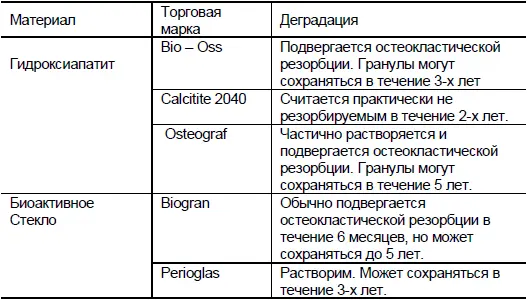
Кроме того, эти материалы не подвергаются остеокластической резорбции и поэтому являются небиодеградируемыми.
Кроме растворимости любой материал в той или иной степени подвержен диссоциации – распаду молекул в жидкой среде на ионы (атомы и молекулы, потерявшие или присоединившие электроны).
Суть диссоциации как физико-химического процесса заключается во взаимодействии молекул материала и растворителя (например, воды, тканевой жидкости или слюны), которое приводит к ослаблению взаимного притяжения положительно и отрицательно заряженных ионов, что вызывает распад части молекул растворяемого вещества на ионы.
Соотношение между числом распавшихся на ионы молекул и общим количеством молекул вещества называется степенью диссоциации [Б.М. Яворский, Ю.А. Селезнёв, 1989; Ю.А. Ершов и др., 1993].
Степень диссоциации и коррозия, под которой подразумевается разрушение или растворение вещества под химическим воздействием внешней среды или жидкости, являются одним из основных показателей пригодности того или иного материала для изготовления имплантатов.
В соответствии с Европейским стандартом (EN ISO 8891, 1995), коррозия материала, пригодного для изготовления имплантатов, должна быть менее 14,3 мкг/см 2в день. Согласно тестам, коррозия титана и его сплавов составляет 11 мкг/см в день [Б. Венц, 1998].
Биологические свойства имплантационных материалов
С биологической точки зрения материал имплантата, его химические элементы а также возможные продукты, образующиеся при его взаимодействии с биологической системой, не должны:
– вызывать патологических изменений в окружающих тканях во время их регенерации;
– нарушать гомеостаз организма, жизнедеятельность органов и тканей в течение всего периода функционирования;
– оказывать токсического, канцерогенного и аллергического воздействия на ткани и организм в целом.
Диссоциация приводит к диффузии ионов материала имплантата, что, естественно, оказывает влияние на процессы жизнедеятельности как окружающих имплантат тканей, так и организма в целом [А.И. Воложин, Г.В. Порядина, 1998].
Если суммировать химический состав биосовместимых материалов, то можно составить перечень ионов неметаллов, которые широко представлены в организме человека [Ю.А. Ершов и др., 1993; P. Марри, Д. Греннер, П. Мейес, В. Родуэл, 1993] – это Са 2+, N+, H+, С+, сО 3 2, РО4.
При этом можно допустить, что в результате диссоциации биосовместимого материала незначительное увеличение концентрации этих ионов не будет оказывать существенного влияния как на окружающие имплантат ткани, так и на организм в целом.
Некоторые металлы, входящие в состав биосовместимых материалов, например, железо, также широко представлены в организме и согласно классификации Ю.А. Ершова и соавт. (1993) являются макроэлементами. Содержание других – алюминия, кобальта, хрома, молибдена и ванадия – составляет от 10 3до 10 5% от общей массы организма человека.
Эти металлы являются микроэлементами. Концентрация титана и никеля в живых организмах ещё меньше, и они считаются ультрамикроэлементами [Ю.А. Ершов и др., 1993].
Таким образом, при введении в организм материалов, в составе которых имеются микро– и ультрамикроэлементы, содержание этих химических элементов может превышать их физиологический уровень. Следовательно, возможно определённое их воздействие на окружающие имплантат ткани и организм в целом.
Ионы железа являются одним из компонентов гемоглобина, миоглобина и различных ферментов. Кроме того, они принимают активное участие в трансформации аморфных кальций-фосфатных соединений в гидроксиапатит. Однако увеличение содержания железа может привести к нарушению окислительно-восстановительных процессов в тканях и оказывать токсическое воздействие на клетки.
Ионы алюминия ингибируют синтез АТФ, поэтому его повышенное содержание может существенно снизить метаболическую активность костной ткани и замедлить минерализацию [D. Williams, 1981].
Ионы алюминия могут угнетать эритропоэз и поражать центральную нервную систему. Считается, что их длительная аккумуляция в тканях головного мозга способна вызвать мутации генов AD3 и AD2, находящихся в 14-й и 19-й хромосомах, вследствие чего может развиться болезнь Альцгеймера.
Читать дальшеИнтервал:
Закладка: