Владимир Виноградов - Стресс и патология
- Название:Стресс и патология
- Автор:
- Жанр:
- Издательство:Array Литагент «Белорусская наука»
- Год:2007
- Город:Минск
- ISBN:978-985-08-0829-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Владимир Виноградов - Стресс и патология краткое содержание
Книга рассчитана на медиков и широкий круг специалистов, интересующихся проблемой коррекции кардио– и иммунопатологии стресса.
Стресс и патология - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
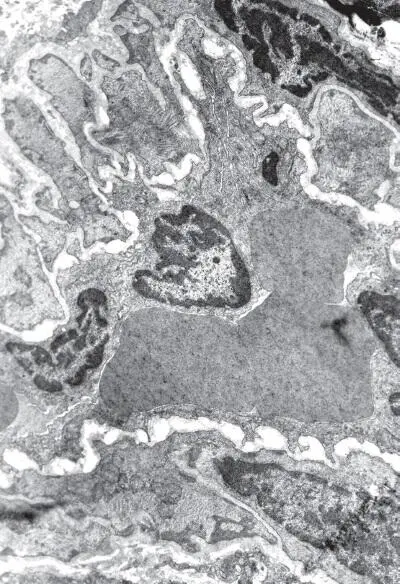
Рис. I-12. То же, что и на рис. I-11. Конец фазы резистентности – начало фазы истощения (48 ч опыта). Спазм интрамуральных артериол. × 71 000
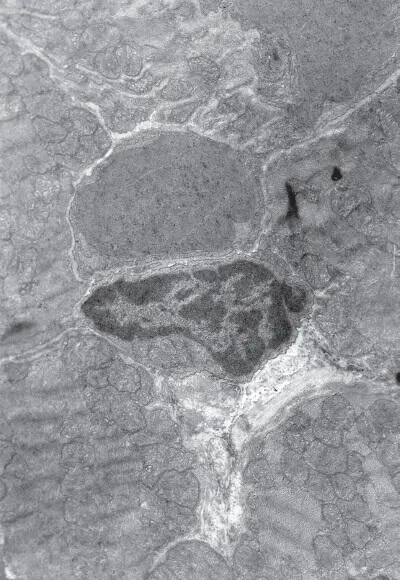
Рис. I-13. То же, что и на рис. I-11. Конец фазы резистентности – начало фазы истощения (48 ч опыта). Сдавливание капилляров пересократившимися темными клетками. × 71 000
Повсеместно наблюдаются явления гемостаза, обусловленные сдавливанием капилляров пересократившимися темными клетками (рис. I-13) и гипертрофированными перицитами, которые в сложной связи своих отростков охватывают эндотелиальную трубку в виде своеобразной муфты (рис. I-14). Свой вклад в сужение просвета капилляров в данный срок опыта вносят и сами эндотелиальные клетки, способные к периодическому набуханию под влиянием нервных импульсов. В схеме двигательной иннервации кровеносных капилляров важная роль отводится перицитам, где находятся окончания симпатических нервов, которые воспринимают, трансформируют и далее передают нервный импульс через свои отростки на эндотелиальную клетку по типу электрического синапса [168]. Если принять гипотезу электрического синапса, то из рис. І-15 видно, что последний может возникать и без посредничества перицитов, поскольку нервные терминали непосредственно граничат с эндотелиальными клетками.
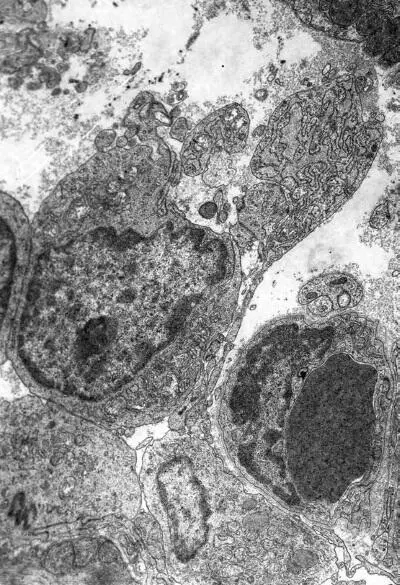
Рис. I-14. То же, что и на рис. I-11. Конец фазы резистентности – начало фазы истощения (48 ч опыта). Сдавливание капилляров гипертрофированными перицитами. × 71 000
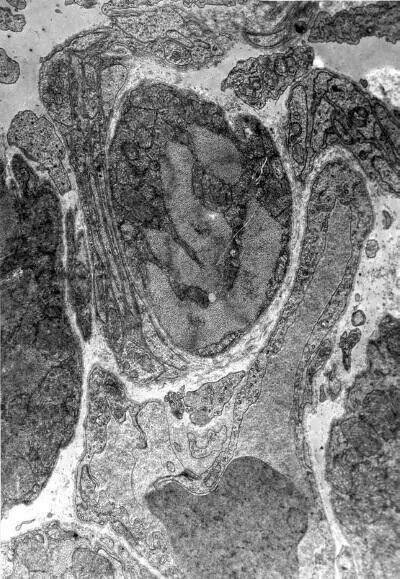
Рис. I-15. То же, что и на рис. I-11. Конец фазы резистентности – начало фазы истощения (48 ч опыта). Окончания нервных терминалей. × 71 000
Согласно гипотезе, нервный импульс, направленный в сторону эндотелиальной клетки, вызывает деполяризацию ее плазмалеммы, что может способствовать потере или накоплению клеткой жидкости, которая, по всей вероятности, проникает через микропоры в плазмалемме [168]. По мнению автора гипотезы, на электронномикроскопических снимках и при прижизненных наблюдениях можно обнаружить набухшие эндотелиальные клетки, которые полностью закрывают просвет капилляра. Вслед за набуханием эндотелиальной клетки через несколько секунд можно видеть ее спадение. Такая периодичность, ведущая в первом случае к сужению просвета кровеносного капилляра и освобождению просвета для движения крови во втором случае, физиологически оправдана и не может быть осуществлена без участия нервной системы.
Фаза истощения (72 ч опыта). В терминальной стадии иммобилизационного стресса типовая гетерогенность кардиомиоцитов практически исчезает. Как и в самом начале развития стрессорной реакции, в левом желудочке в этот период доминируют светлые клетки (90 %; 10 % составляют полутемные клетки), что, очевидно, является результатом длительной перегрузки ультраструктурных элементов сердца. Однако в отличие от фазы напряжения (1—12 ч опыта), где светлые клетки были в основном однородными и различались только по степени набухания, здесь отмечается их выраженная внутрипуловая гетерогенность, обусловленная различной выраженностью деструкции митохондриального и контрактильного аппарата. В сарколемме таких кардиомиоцитов появляются множественные дефекты. На отдельных участках, особенно в тех, к которым близко прилежат капилляры, сарколемма становится размытой. В большинстве мышечных клеток отмечается отек саркоплазмы, особенно в субсарколемной зоне. Наряду с набухшими, но сохранившими нативную ультраструктуру кардиомиоцитами (30 %) – светлые клетки 1-го типа (рис. I-16) – появляются светлые клетки 2-го типа, в которых почти все митохондрии разрушены (20 %). Миофибриллы в них в основном фрагментированы на уровне дисков I, но имеются и большие участки гомогенизации, разволокнения и разрыва миофиламентов. Многие диски Z смещаются по отношению друг к другу в лежащих рядом миофибриллах (рис. I-17). В светлых клетках 3-го типа (40 %) большинство митохондрий в состоянии либо выраженного, либо умеренного набухания, матрикс их очагово просветлен. Резко уменьшено количество крист, имеющиеся кристы фрагментированы, хаотично расположены, в центре митохондрий они превращаются в гомогенную слабоосмиофильную массу. Наружные мембраны митохондрий теряют двухконтурность либо на всем протяжении, либо на значительных участках. Немало митохондрий полностью гомогенизированных, а также резко набухших, лишенных матрикса и крист.
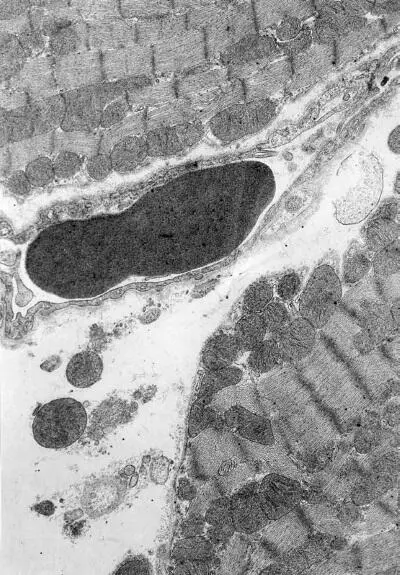
Рис. I-16. Миокард левого желудочка крысы при иммобилизационном стрессе. Фаза истощения (72 ч опыта). Деструктивные кардиомиоциты первого типа. × 71 000
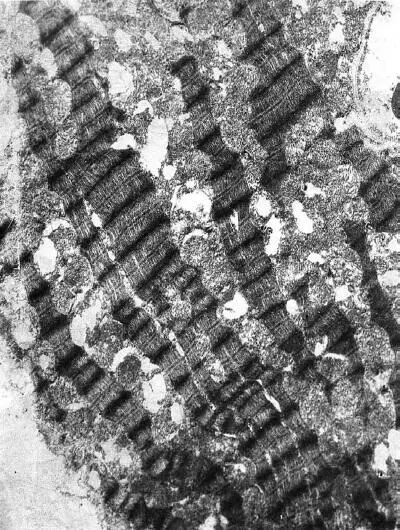
Рис. I-17. То же, что и на рис. I-16. Фаза истощения (72 ч опыта). Деструктивные кардиомиоциты второго типа. × 71 000
Примечательна мозаичность изменения митохондрий: в одной и той же клетке имеются митохондрии с различной степенью изменений – от умеренного набухания и неравномерного расположения крист до полной деструкции органелл (рис. I-18). В миофибриллах отмечается появление множественных участков деструкции. На продольных срезах отчетливо видно, что вначале происходит расплавление тонких миофиламентов. Затем возникают очаги их деструкции на протяжении нескольких саркомеров. Разделительные диски Z исчезают. В этих участках сохраняются лишь обрывки толстых миофиламентов и остатки дисков I (рис. I-18). В других участках происходит гомогенизация миофибрилл. В очагах гомогенизации заметны обрывки миофиламентов, которые затем подвергаются расплавлению. Наблюдается значительная вариабельность в степени повреждения между различными мышечными клетками этого типа. В некоторых кардиомиоцитах в областях разрушения миофибрилл видна гомогенная масса миофиламентов, в то время как другие области имели нормальный или почти нормальный вид. В очагах тяжелого повреждения клетки спектр изменения был довольно широким – от конденсации до полного лизиса миофибрилл.
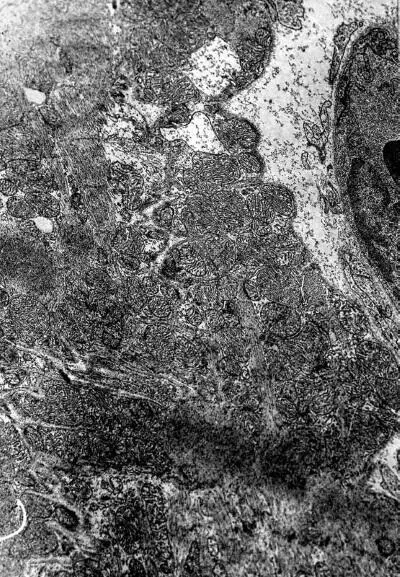
Рис. I-18. То же, что и на рис. I-16. Фаза истощения (72 ч опыта). Деструктивные кардиомиоциты третьего типа. × 71 000
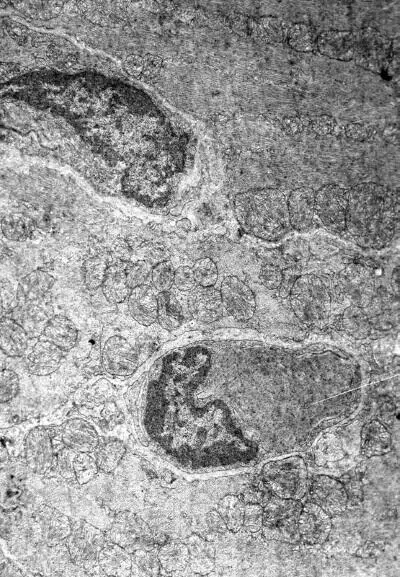
Рис. I-19. То же, что и на рис. I-16. Фаза истощения (72 ч опыта). Лизис кардиомиоцитов. × 71 000
Читать дальшеИнтервал:
Закладка: