Лев Николаев - Металлы в живых организмах
- Название:Металлы в живых организмах
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1986
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Лев Николаев - Металлы в живых организмах краткое содержание
Металлы в живых организмах - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Во-первых, оказывается, что одно и то же координационное соединение, содержащее лиганды нескольких видов, может существовать в нескольких формах, различающихся способом размещения лигандов и соответственно физическими и химическими свойствами. Так, соединение Pt(NH 3) 2(NO 2)2Cl 2, имеющее лиганды трех сортов, может существовать в пяти различных формах (положение иона платины указано точкой в центре квадрата):
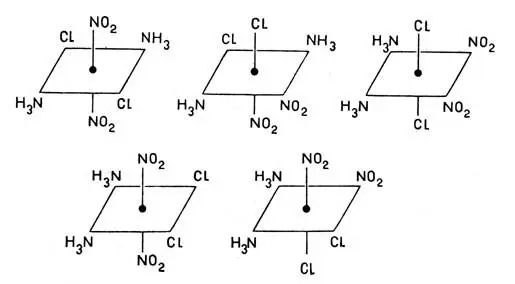
Соединение Pt(NH 3) 2(NO 2)2Cl 2, имеющее лиганды трех сортов, может существовать в пяти различных формах (положение иона платины указано точкой в центре квадрата):
Все пять форм были получены советскими учеными И. И. Черняевым и Г. С. Муравейской. Это явление аналогично явлению изомерии, характерному для органических соединений. Очевидно, все вышенаписанные формулы представляют строение изомеров одного и того же координационного соединения Pt(NH 3) 2(NO 2) 2Cl 2.
Во-вторых, геометрическая форма комплекса влияет на способность центрального иона металла вступать в те или иные взаимодействия с дгими молекулами. Если ион металла имеет координационное число 6 и находится в центре октаэдра, то он, конечно, довольно хорошо изолирован от внешней среды, и молекулам, с которыми о бы вступить в соединение, трудно до него добраться. Но если тот же ион располагается в центре плоского квадрата и имеет КЧ, равное 4, то он открыт с двух сторон. Даже в том случае, когда с одной стороны ион уже присоединил какую-либо частицу (например, частицу белка), все равно с другой стороны к нему открыт доступ.
Именно так обстоит дело с гемоглобином. Комплекс железа с протопорфирином (замещенным порфином) имеет плоское строение, КЧ равно 4. Кроме того, с одной стороны к иону железа присоединена молекула белка (глобин), но шестое место в координационной сфере свободно. Это место и занимает молекула кислорода, переносимого гемоглобином в процессе дыхания. Если бы комплекс железа имел КЧ, равное 6, и ион железа был бы изолирован от среды, гемоглобин не мог бы переносить кислород, необходимый для дыхания клеток.
Как видно, даже геометрические особенности координационных соединений имеют жизненно важное значение. Одной из самых характерных особенностей химии координационных соединений является глубокое различие между свойствами простого иона и иона, окруженного лигандами. Иначе говоря, свойства комплексного иона существенно зависят от химической природы как центрального иона, так и лигандов (табл. 4).
Таблица 4. Сравнение свойств комплексов и гидратированных ионов тех же металлов
Медь | Аммиак, амины | Реагируют с целлюлозой, темно-синяя окраска; бурно разлагают пероксид водорода | Не реагируют с целлюлозой, слабоголубая окраска; медленно разлагают пероксид водорода
Железо | Порфин (его производные) | Переносят кислород. Энергично разлагают пероксид водорода, ускоряют окисление различных веществ | Не способен переносить кислород. Окислительные свойства выражены относительно слабо
Цинк | Белки То же | Ускоряют разложение гидрокарбонатов. Способствуют усвоению белков | Не влияет на разложение гидрокарбонатов и усвоение белков
Молибден | Белки | Способствуют усвоению бактериями атмосферного азота | Не влияет на усвоение атмосферного азота
Магний | Производное порфина | Хлорофилл обусловливает превращение диоксида углерода и воды в углеводы (фотосинтез) | Не ускоряет фотосинтез
Ионы металлов, не связанные с лигандами, встречаются редко. В сущности, химик может наблюдать свойства такого "простого" иона металла разве что при очень высоких температурах в газообразной среде, нагревая ту или иную соль до температур порядка тысяч градусов. В растворах солей ионы металлов связаны с молекулами воды (гидратированы) и, следовательно, находятся там в виде комплексов. Но заменим молекулы воды на молекулы аммиака, например в растворе соли меди CuCl 2. Как мы уже знаем, при этом получится темно-синий комплекс, имеющий свойства, которых нет у гидратированного иона.
Гидратированные ионы слабо окрашены, они легко взаимодействуют с ионами карбоната, образуя осадок карбоната меди, практически не реагируют с целлюлозой. А вот комплексные ионы Cu(NH 3) 4 2+с ионами карбонатов СО 3 2-осадка не образуют, а целлюлозу (например, вату) в щелочной среде растворяют (на этом основан один из способов получения искусственного шелка). Ионы цинка в виде гидратного комплекса не влияют на разложение кислых солей угольной кислоты, а комплексное соединение цинка, содержащееся в крови, ускоряет распад гидрокарбонатов и выделение из крови в легкие диоксида углерода. Не будь этого комплекса в организме, мы не могли бы дышать, так как освобождение крови от углекислоты происходило бы слишком медленно. Наконец, если бы исчезло комплексное соединение магния — хлорофилл, то растения не могли бы развиваться и жизнь на Земле, лишившись притока поддерживающей ее солнечной энергии, прекратилась бы! Отсюда следует, что, изменяя состав комплексов, природа может в очень широких пределах варьировать свойства соединений данного металла и для решения множества биохимических задач обходиться относительно небольшим числом металлов.
Суммируем вкратце, что мы узнали о том, каким образом действуют ионы металлов в клетках организма.
Металлы находятся в клетках в виде комплексных соединений с различными органическими, веществами: белками, различными производными порфина и др. Комплексные ионы присоединяют к себе частицы-лиганды так, что получается правильная геометрическая форма: треугольник, тетраэдр, октаэдр и т. п. Одно или два места около иона могут остаться свободными, и туда попадают другие молекулы, например молекула кислорода в частицу гемоглобина. Все лиганды занимают определенные положения и относительно иона, и относительно друг друга; они, как говорят, правильно ориентированы в пространстве.
Ион металла имеет положительный заряд и притягивает к себе отрицательные заряды — электроны, находящиеся в молекулах (или ионах) лигандов. Таким образом, молекулы лигандов поляризуются. Но свойства комплексного иона так своеобразны и так сильно зависят от природы лигандов, что приходится предположить, что между лигандами и центральным ионом металла образуются химические связи. Это значит, что ион и лиганды имеют общие электроны.
Вопрос об электронном строении координационных соединений вызывал споры среди ученых на протяжении не одного десятка лет. Казалось очень странным, что к соединению, в котором явно насыщены все валентности, можно присоединить нейтральные молекулы. Придумывали очень сложные структурные формулы, приписывали атомам несвойственные им валентности, но все это не привело к успеху. Только развитие теории строения атома и химической связи, а также достижения квантовой химии помогли понять, почему образуются координационные соединения и какова их роль в процессах обмена веществ в организмах.
Читать дальшеИнтервал:
Закладка: