Александр Артеменко - Удивительный мир органической химии
- Название:Удивительный мир органической химии
- Автор:
- Жанр:
- Издательство:Дрофа
- Год:2005
- Город:Москва
- ISBN:5-7107-9540-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Александр Артеменко - Удивительный мир органической химии краткое содержание
Книга адресована старшеклассникам, учителям, а также тем, кто интересуется органической химией.
Удивительный мир органической химии - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
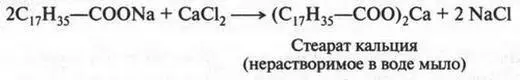
Существует несколько сортов мыла. Наибольшее распространение получили туалетные мыла. В них добавляют различные душистые вещества (отдушки), красители, антисептики и другие добавки. Специальные сорта мыла входят в состав кремов для бритья, зубных паст и т. д. А вот нерастворимые мыла нашли применение в технике. Например, добавляя кальциевое мыло в нефтяные масла, получают смазки для автотранспорта (солидол), а обрабатывая плотную хлопчатобумажную ткань алюминиевым мылом, изготавливают брезент, из которого шьют чехлы, дождевые плащи, палатки и др. Свинцовое, марганцевое и кобальтовое мыла нашли применение в качестве добавок при изготовлении олифы (сиккативы), масляных красок.
Особо следует сказать об олеиновой кислоте. В отличие от твердых пальмитиновой и стеариновой кислот она — жидкая (маслообразная), но на холоде твердеет. В молекуле этой кислоты содержится одна двойная связь:
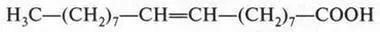
Поэтому она легко присоединяет по месту двойной связи водород и галогены. При восстановлении олеиновая кислота переходит в предельную кислоту — стеариновую:
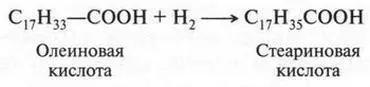
Олеиновую кислоту получают омылением некоторых растительных масел.
Известны еще более непредельные кислоты — линолевая и линоленовая. Они также входят в состав растительных масел. В молекуле линолевой кислоты содержатся две двойные связи, а в молекуле линоленовой кислоты — три:
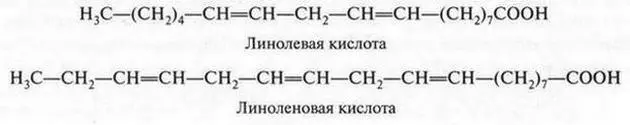
Эти кислоты — жидкости. Они легко окисляются и полимеризуются. При восстановлении превращаются в стеариновую кислоту. Эти кислоты крайне необходимы для нормальной деятельности живого организма и конечно же должны содержаться в пище. Их относят к незаменимым карбоновым кислотам. Поэтому растительные масла, содержащие их, являются ценными продуктами (особенно для людей пожилого возраста). Они способствуют удалению холестерина и повышают эластичность стенок кровеносных сосудов.
В рассмотренных нами кислотах содержится одна карбоксильная группа. Такие карбоновые кислоты называются одноосновными. Однако известны кислоты, в молекулах которых имеются две и более карбоксильных групп. Карбоновые кислоты с двумя карбоксильными группами называются двухосновными. Самой простой кислотой такого строения является щавелевая кислота НООС—СООН. Как видите, молекула этой кислоты — соединение двух карбоксильных групп друг с другом.
Впервые щавелевая кислота была обнаружена в кислом щавеле (конский щавель) в виде кислой калиевой соли, а в 1776 г. она была получена в свободном виде. В 1824 г. щавелевую кислоту синтезировал Ф. Вёлер при взаимодействии дициана с водой:
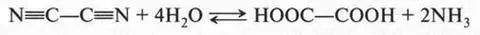
Известно, что ни сам Ф. Вёлер, ни его современники не обратили особого внимания на этот синтез. А ведь при этом происходило превращение неорганического вещества в органическое!
В промышленности щавелевую кислоту получают при нагревании натриевой соли муравьиной кислоты (формиата натрия):
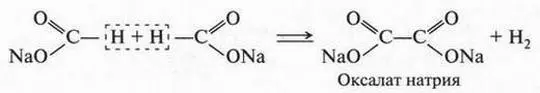
Затем на соль — оксалат натрия — действуют серной кислотой и получают свободную щавелевую кислоту.
Щавелевая кислота — довольно сильная кислота. По кислотным свойствам она превосходит даже муравьиную кислоту. Обладает всеми свойствами карбоновых кислот. Но у нее есть и особые свойства: она известна как восстановитель. Поэтому ее используют для отбеливания тканей, в производстве красителей, применяют в кожевенной и деревообрабатывающей промышленности. Она может удалять ржавчину и накипь. Без этой кислоты не обходится и пищевая промышленность, но применять ее как пищевую добавку нужно осторожно: она связывается в кишечнике с кальцием, образуя нерастворимые соли. Это приводит к тому, что кальций — важнейший элемент для организма — не всасывается в кровь.
Наш рассказ о карбоновых кислотах был бы неполным, если мы обойдем другие, не менее интересные, кислоты. Представьте себе, что в молекуле щавелевой кислоты две карбоксильные группы разделены одной двойной связью:
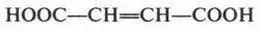
Эту непредельную двухосновную кислоту называют этилендикарбоновой кислотой. Эта кислота существует в виде двух изомеров, которые различаются пространственным строением. Эти изомеры представляют собой две различные кислоты. Одна из них (реформа) называется малеиновой кислотой , другая (трансформа) — фумаровой кислотой.

Еще в 1838 г. Ю. Либих обратил внимание на то, что эти кислоты отличаются по химическим свойствам, хотя и имеют одну и ту же эмпирическую формулу. Это оставалось загадкой до 1874 г., когда Я. Вант-Гофф на основе теории тетраэдрического углеродного атома объяснил причину различия свойств этих кислот.
Малеиновая кислота, в отличие от фумаровой, теряя воду, легко образует малеиновый ангидрид:
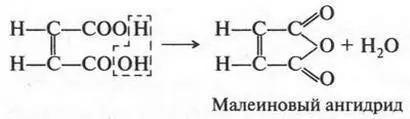
А вот фумаровая кислота так легко ангидрид не образует. Почему? Очень просто: две карбоксильные группы, от которых отщепляется молекула воды, расположены далеко друг от друга.
Кроме этого, у этих кислот имеются и другие отличия. Так, малеиновая кислота токсична, а фумаровая нет. Она наряду с лимонной, винной и яблочной кислотами используется в пищевой промышленности (например, в США при приготовлении напитков).
Малеиновая кислота содержится во многих растениях, в особенности в грибах и лишайниках. Применяется для получения различных ПАВ, а также в качестве антиокислителя для жиров. Что же касается фумаровой кислоты, то она идет на производство синтетических высыхающих масел и пластификаторов.
6.4. Бензол и карбоксильная группа
Будем считать, что наш рассказ о карбоновых кислотах не закончен. Представьте себе такую молекулу: карбоксильная группа связана с бензольным кольцом. Соединения такого строения относятся к ароматическим карбоновым кислотам. Самой простой из них является бензойная кислота.
Читать дальшеИнтервал:
Закладка:









