БСЭ БСЭ - Большая Советская Энциклопедия (АМ)
- Название:Большая Советская Энциклопедия (АМ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (АМ) краткое содержание
Большая Советская Энциклопедия (АМ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
C 5H 5N + NaNH 2® C 5H 4N(NH 2) + NaH.
При пропускании паров бензола с аммиаком через накалённую трубку образуется (с очень низким выходом) анилин :
C 6H 6+ NH 3®C 6H 5NH 2+ H 2.
Аминоантрахиноновые красители
Аминоантрахино'новые краси'тели,см. Антрахиноновые красители .
Аминогруппа
Аминогру'ппа,одновалентная группа —NH 2, остаток аммиака NH 6. А. содержится во многих органических соединениях — аминах, аминокислотах, аминоспиртах и др.
Аминодонты
Аминодо'нты(Amynodontidae), семейство вымерших примитивных носорогов. Жили в палеогене (эоцен, олигоцен) в Евразии и Северной Америке; обитали на болотах и по берегам рек. По размеру и пропорциям тела близки к бегемоту. Имели короткие массивные ноги (передние с 4, задние с 3 пальцами), крупный череп, мощные клыки, редуцированные резцы и передние коренные зубы.
Аминокапроновая кислота
e-Аминокапро'новая кислота',NH 2(CH 2) 5COOH, органическая кислота, бесцветные кристаллы, хорошо растворимые в воде, нерастворимые в обычных органических растворителях. А. к. получают обычно гидролизом e- капролактама— сырья для производства полиамидной смолы капрон. А. к. применяют для синтеза некоторых аминокислот, например лизина .
Аминокислоты
Аминокисло'ты,класс органических соединений, объединяющих в себе свойства кислот и аминов, т. е. содержащих наряду с карбоксильной группой —COOH аминогруппу —NH 2. В зависимости от положения аминогруппы относительно карбоксильной группы различают a-, b-, g - и др. А. А. играют очень большую роль в жизни организмов, т. к. все белковые вещества построены из А. Все белки при полном гидролизе (расщеплении с присоединением воды) распадаются до свободных А., играющих роль мономеров в полимерной белковой молекуле. При биосинтезе белка порядок, последовательность расположения А. задаются генетическим кодом, записанным в химической структуре дезоксирибонуклеиновой кислоты. 20 важнейших А., входящих в состав белков, отвечают общей формуле RCH(NH 2)COOH и относятся к a-А. В природе встречаются и b-А., RCH(NH 2)CH 2COOH, например b-аланин CH 2NH 2CH 2COOH, входящий в состав пантотеновой кислоты. А. могут содержать одну NH 2-группу и одну СООН-группу (моноаминокарбоновые кислоты), одну NH 2-группу и две СООН-группы (моноаминодикарбоновые кислоты), две NH 2-группы и одну СООН-группу (диаминомонокарбоновые кислоты).
Моноаминокарбоновые кислоты:
Глицин - NH 2CH 2COOH
Аланин - CH 3CH (NH 2) COOH
Цистеин - CH 2(SH)CH(NH 2)COOH
Метионин - CH 2(SCH 3) CH 2CH (NH 2) COOH
Валин-(СН 3) 2СНСН(МН 2)СООН и др.
Моноаминодикарбоновые кислоты:
Аспарагиновая - HOOC CH 2CH (NH 2) COOH
Глутаминовая - HOOC (CH 2) 2CH (NH 2) COOH
Диаминомонокарбоновые кислоты:
Лизин - NH 2CH 2(CH 3) 2CH(NH 2)COOH
Аргинин - NH2C(=NH)NH(CH 2) 3CH(NH 2)COOH и др.
А. — бесцветные кристаллические вещества, растворимые в воде; t п л 220—315°С. Высокая температура плавления А. связана с тем, что их молекулы имеют структуру главным образом амфотерных (двузарядных) ионов. Например, строение простейшей А. — глицина— можно выразить формулой 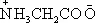 (а не NH 2CH 2COOH).
(а не NH 2CH 2COOH).
Все природные А., кроме глицина, содержат асимметричные атомы углерода, существуют в оптически активных модификациях и, как правило, относятся к L-ряду. А. D-ряда содержатся только в некоторых антибиотиках и в оболочках бактерий.
Многие растения и бактерии могут синтезировать все необходимые им А. из простых неорганических соединений. Большинство А. синтезируются в теле человека и животных из обычных безазотистых продуктов обмена веществ и усвояемого азота. Однако 8 А. (валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан и фенилаланин) являются незаменимыми, т. е. не могут синтезироваться в организме животных и человека, и должны доставляться с пищей. Суточная потребность взрослого человека в каждой из незаменимых А. составляет в среднем около 1 г. При недостатке этих А. (чаще триптофана, лизина, метионина) или в случае отсутствия в пище хотя бы одной из них невозможен синтез белков и многих др. биологически важных веществ, необходимых для жизни. Гистидин и аргинин синтезируются в животном организме, но лишь в ограниченной, иногда недостаточной, мере. Цистеин и тирозин образуются лишь из своих предшественников — соответственно метионина и фенилаланина — и могут стать незаменимыми при недостатке этих А. Некоторые А. могут синтезироваться в животном организме из безазотистых предшественников при помощи процесса переаминирования, т. е. переноса аминогруппы с одной А. на др. В организме А. постоянно используются для синтеза и ресинтеза белков и др. веществ — гормонов, аминов, алкалоидов, коферментов, пигментов и др. Избыток А. подвергается распаду до конечных продуктов обмена (у человека и млекопитающих до мочевины, двуокиси углерода и воды), при котором выделяется энергия, необходимая организму для процессов жизнедеятельности. Промежуточным этапом такого распада является обычно дезаминирование (чаще всего окислительное).
К числу производных А., представляющих большой практический интерес, относится лактам w-аминокапроновой кислоты (см. Капролактам ) — исходный продукт производства капрона.
Известно много методов синтеза А., например действие аммиака на галогензамещённые карбоновые кислоты:
RCHCICOOH+2NH 3® RCHNH 2COOH + NH 4CI,
восстановление оксимов или гидразонов, кето- или альдегидокислот:
RC(= NOH)COOH ® RCHNH 2COOH
и др. Некоторые А. выделяют из продуктов гидролиза богатых ими белков методом адсорбции на ионообменных смолах; так выделяют глутаминовую кислоту из казеина и клейковины злаков; тирозин — из фиброина шёлка; аргинин— из желатины; гистидин из белков крови. Некоторые А. производят синтетически, например метионин, лизин и глутаминовую кислоту. А. получают в больших количествах также микробиологическим синтезом. Поступление в организм незаменимых А. определяется количеством и аминокислотным составом пищевых белков. Это следует учитывать для организации правильного общественного питания и составления рационов для разных возрастных и профессиональных групп населения. Потребность в пищевом белке может быть полностью покрыта за счёт смеси А. Этим пользуются в лечебном питании.
А. применяют в медицине: для парентерального питания больных (т. е. минуя желудочно-кишечный тракт) с заболеваниями пищеварительных и др. органов, а также для лечения заболеваний печени, малокровия, ожогов (метионин), язв желудка (гистидин), при нервно-психических заболеваниях (глутаминовая кислота и т. п.); в животноводстве и ветеринарии — для питания (см. ниже) и лечения животных, а также в микробиологической, медицинской и пищевой промышленности.
Читать дальшеИнтервал:
Закладка:
