БСЭ БСЭ - Большая Советская Энциклопедия (ПЕ)
- Название:Большая Советская Энциклопедия (ПЕ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ПЕ) краткое содержание
Большая Советская Энциклопедия (ПЕ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
По современной терминологии (см. далее), элементы этих периодов относятся к s -элементам (щелочные и щёлочноземельные металлы), составляющим I a - и II a -подгруппы (выделены на цветной таблице красным цветом), и р -элементам (В — Ne, At — Ar), входящим в III a — VIII a -подгруппы (их символы выделены оранжевым цветом). Для элементов малых периодов с возрастанием порядковых номеров сначала наблюдается уменьшение атомных радиусов , а затем, когда число электронов в наружной оболочке атома уже значительно возрастает, их взаимное отталкивание приводит к увеличению атомных радиусов. Очередной максимум достигается в начале следующего периода на щелочном элементе. Примерно такая же закономерность характерна для ионных радиусов.
Четвёртый период (K — Kr) содержит 18 элементов (первый большой период, по Менделееву). После щелочного металла K и щёлочноземельного Ca (s-элементы) следует ряд из десяти так называемых переходных элементов (Sc — Zn), или d- элементов (символы даны синим цветом), которые входят в подгруппы б соответствующих групп П. с. э. Большинство переходных элементов (все они металлы) проявляет высшие степени окисления, равные номеру группы. Исключение — триада Fe — Co — Ni, где два последних элемента максимально положительно трёхвалентны, а железо в определённых условиях известно в степени окисления VI. Элементы, начиная с Ga и кончая Kr ( р -элементы), принадлежат к подгруппам а , и характер изменения их свойств такой же, как и в соответствующих интервалах Z у элементов второго и третьего периодов. Установлено, что Kr способен образовывать химические соединения (главным образом с F), но степень окисления VIII для него неизвестна.
Пятый период (Rb — Xe) построен аналогично четвёртому; в нём также имеется вставка из 10 переходных элементов (Y — Cd), d -элементов. Специфические особенности периода: 1) в триаде Ru — Rh — Pd только рутений проявляет степень окисления VIII; 2) все элементы подгрупп а проявляют высшие степени окисления, равные номеру группы, включая и Xe; 3) у I отмечаются слабые металлические свойства. Таким образом, характер изменения свойств по мере увеличения Z у элементов четвёртого и пятого периодов более сложен, поскольку металлические свойства сохраняются в большом интервале порядковых номеров.
Шестой период (Cs — Rn) включает 32 элемента. В нём помимо 10 d -элементов (La, Hf — Hg) содержится совокупность из 14 f -элементов, лантаноидов , от Ce до Lu (символы чёрного цвета). Элементы от La до Lu химически весьма сходны. В короткой форме П. с. э. лантаноиды включаются в клетку La (поскольку их преобладающая степень окисления III) и записываются отдельной строкой внизу таблицы. Этот приём несколько неудобен, поскольку 14 элементов оказываются как бы вне таблицы. Подобного недостатка лишены длинная и лестничная формы П. с. э., хорошо отражающие специфику лантаноидов на фоне целостной структуры П. с. э. Особенности периода: 1) в триаде Os — Ir — Pt только осмий проявляет степень окисления VIII; 2) At имеет более выраженный (по сравнению с 1) металлический характер; 3) Rn, по-видимому (его химия мало изучена), должен быть наиболее реакционноспособным из инертных газов.
Седьмой период, начинающийся с Fr (Z = 87), также должен содержать 32 элемента, из которых пока известно 20 (до элемента с Z = 106). Fr и Ra — элементы соответственно I a - и II a -подгрупп (s-элементы), Ac — аналог элементов III б -подгруппы ( d -элемент). Следующие 14 элементов, f -элементы (с Z от 90 до 103), составляют семейство актиноидов . В короткой форме П. с. э. они занимают клетку Ac и записываются отдельной строкой внизу таблицы, подобно лантаноидам, в отличие от которых характеризуются значительным разнообразием степеней окисления. В связи с этим в химическом отношении ряды лантаноидов и актиноидов обнаруживают заметные различия. Изучение химической природы элементов с Z = 104 и Z = 105 показало, что эти элементы являются аналогами гафния и тантала соответственно, то есть d -элементами, и должны размещаться в IV б - и V б -подгруппах. Членами б -подгрупп должны быть и последующие элементы до Z = 112, а далее (Z = 113—118) появятся р -элементы (III a — VIll a -подгруппы).
Теория П. с. э.В основе теории П. с. э. лежит представление о специфических закономерностях построения электронных оболочек (слоев, уровней) и подоболочек (оболочек, подуровней) в атомах по мере роста Z (см. Атом , Атомная физика ). Это представление было развито Бором в 1913—21 с учётом характера изменения свойств химических элементов в П. с. э. и результатов изучения их атомных спектров. Бор выявил три существенные особенности формирования электронных конфигураций атомов: 1) заполнение электронных оболочек (кроме оболочек, отвечающих значениям главного квантового числа n = 1 и 2) происходит не монотонно до полной их ёмкости, а прерывается появлением совокупностей электронов, относящихся к оболочкам с большими значениями n ; 2) сходные типы электронных конфигураций атомов периодически повторяются; 3) границы периодов П. с. э. (за исключением первого и второго) не совпадают с границами последовательных электронных оболочек.
В обозначениях, принятых в атомной физике, реальная схема формирования электронных конфигураций атомов по мере роста Z может быть в общем виде записана следующим образом:
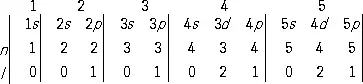

Вертикальными чертами разделены периоды П. с. э. (их номера обозначены цифрами наверху); жирным шрифтом выделены подоболочки, которыми завершается построение оболочек с данным n . Под обозначениями подоболочек проставлены значения главного ( n ) и орбитального ( l ) квантовых чисел, характеризующие последовательно заполняющиеся подоболочки. В соответствии с Паули принципом ёмкость каждой электронной оболочки равна 2n 2 , а ёмкость каждой подоболочки — 2(2 l + 1). Из вышеприведённой схемы легко определяются ёмкости последовательных периодов: 2, 8, 8, 18, 18, 32, 32... Каждый период начинается элементом, в атоме которого появляется электрон с новым значением n . Таким образом, периоды можно характеризовать как совокупности элементов, начинающиеся элементом со значением n , равным номеру периода, и l = 0 ( ns 1-элементы), и завершающиеся элементом с тем же n и l = 1 ( np 6-элементы); исключение — первый период, содержащий только ls -элементы. При этом к а -подгруппам принадлежат элементы, для атомов которых n равно номеру периода, а l = 0 или 1, то есть происходит построение электронной оболочки с данным n . К б -подгруппам принадлежат элементы, в атомах которых происходит достройка оболочек, остававшихся незавершёнными (в данном случае n меньше номера периода, а l = 2 или 3). Первый — третий периоды П. с. э. содержат только элементы а -подгрупп.
Читать дальшеИнтервал:
Закладка:
