БСЭ БСЭ - Большая Советская Энциклопедия (РЕ)
- Название:Большая Советская Энциклопедия (РЕ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (РЕ) краткое содержание
Большая Советская Энциклопедия (РЕ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
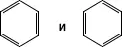
можно записать формулы
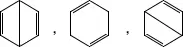
(структуры Дьюара), в которых один из валентных штрихов соединяет несоседние атомы. Такие структуры должны играть при описании действительного состояния молекулы бензола меньшую роль, чем структуры Кекуле. Роль тех или иных структур определяется качественными следствиями вариационного принципа квантовой механики: для основного состояния наиболее существенны те структуры, энергия которых минимальна. Чем выше энергия данной структуры по сравнению с минимальной величиной энергии структур, тем менее существенна эта структура для описания молекулы в целом. Согласно вариационному принципу, энергия Е , вычисляемая с оптимальной линейной комбинацией волновых функций структур i меньше энергии E iкаждой отдельной структуры. Минимальное значение разности E i— Е носит название энергии резонанса. Как правило, чем больше значение этой разности, тем больше отклоняется описание состояния реальной молекулы от описания, получаемого в рамках классической теории строения при использовании только одной структурной формулы. На практике обычно пользуются иной величиной, называемой экспериментальной энергией резонанса и определяемой как разность между экспериментальной теплотой образования соединения и энергией, вычисленной для одной структуры, отвечающей классической структурной формуле, при использовании табличных значений энергий отдельных связей.
Для описания молекул многих классов соединений достаточно ограничиться одной валентной структурой (например, молекулы насыщенных углеводородов). Для других молекул, например с сопряжённым двойными и тройными связями, приходится использовать представление о наложении (резонансе) нескольких валентных структур. В этих случаях Р. т. прибегает к совокупности структурных формул вместо какой-либо одной формулы, что отличает её от других способов описания, пользующихся пунктирными линиями для валентных штрихов, стрелками для указания смещений электронной плотности и т. п. Отдельные структуры при этом не представляют каких-либо независимых, реально существующих состояний молекулы и являются лишь составными элементами единого описания одного состояния, аналогично тому, как отдельные элементы классического описания (простые связи, двойные связи и т. д.) служат для единого описания структуры молекулы в целом.
Р. т. позволяет качественно или полуколичественно (путём простых вычислений на базе упрощённых вариантов метода валентных схем) судить о симметрии молекул, об эквивалентности тех или иных связей и структурных элементов в молекулах, о стабильности и реакционной способности молекул. Она помогает понять, а отчасти и предвидеть результаты экспериментальных исследований, не претендуя на большую строгость рассуждений и не опираясь на достаточно строгие, но громоздкие квантовомеханические расчёты. В рамках Р. т. были введены такие широко используемые в настоящее время представления, как одно- и трёх-электронные связи, гибридизация связевых орбиталей, сверхсопряжение, а также представление о частично ионном характере ковалентных связей между различными атомами (резонанс ковалентной и ионной структур).
Р. т. была предложена Л. Полингом в 1928—31 гг. и развита в последующие годы в основном в трудах его школы. Термин «резонанс» был заимствован у В. Гейзенберга , проследившего аналогию между квантовомеханическим описанием систем, например двух связанных осцилляторов, и их классическим описанием, учитывающим резонанс в такой системе.
Лит.: Паулинг Л., Природа химической связи, пер. с англ., М. — Л., 1947; Уэланд Д., Теория резонанса и её применение в органической химии, пер. с англ., М., 1948; Полинг Л., Теория резонанса в химии, «Журнал Всесоюзного химического общества им. Д. И. Менделеева», 1962, т. 7, № 4, с. 462; Pauling L., The nature of the chemical bond, 3 ed., lthaca — N. Y., 1960.
Резонансная линия
Резона'нсная ли'ния,спектральная линия излучения атома, частота которой совпадает с частотой света, поглощаемого им в основном состоянии. Обычно Р. л. называют одну или несколько наиболее интенсивных линий в спектре при резонансном излучении.
Резонансное излучение
Резона'нсное излуче'ние,излучение, испускаемое системой связанных зарядов (например, атомом, атомным ядром), при котором частота излучения совпадает с частотой возбуждающего света. Р. и. могут испускать газы, жидкости и твёрдые тела, по наиболее чёткая картина наблюдается в атомных парах Hg, Cd, Na и др. Открыто Р. и. было при исследовании свечения паров Na Р. Вудом (1905).
Для возбуждения Р. и. атом (или др. систему связанных зарядов) облучают светом частоты n. Поглощая квант с энергией h n ( h — Планка постоянная ), атом с основного уровня E 0переходит на возбуждённый уровень E n(уровень E 2на рис .). При спонтанном переходе атома из возбуждённого состояния E nв основное E 0и происходит Р. и. — атом испускает квант с частотой n, и в спектре излучения появляется резонансная линия. Совокупность резонансных линий образует резонансный спектр атома. Р. и. атомов и молекул является резонансной люминесценцией. При взаимодействии атомного ядра с g-излучением может возникать Р. и. g-квантов.
Р. и. наблюдается лишь при определённых условиях (в разрежённых атомных парах, замороженных растворах). Обычно атом безызлучательно переходит из возбуждённого состояния в промежуточное (на рис . на уровень E 1), и лишь затем происходит излучательный переход в основное состояние с частотой < n. Если в результате возбуждения атом сразу перешёл на уровень E 1, Р. и. наблюдается в чистом виде (поскольку в этом случае промежуточных уровней нет).
Р. и. — процесс, наблюдаемый в течение некоторого времени t. Интенсивность Р. и. I меняется со временем по закону: I = I 0 e — t / t , где I 0 — начальная интенсивность, t — среднее время жизни атома в возбуждённом состоянии. Обычно t @ 10 -8 сек ; если электронный переход запрещен отбора правилами , продолжительность Р. и. может значительно увеличиться (например, в парах Hg наблюдается переход с t @ 10 -7 сек ).
Р. и. всегда поляризовано, причём степень и характер поляризации определяются поляризацией возбуждающего света, направлением наблюдения, излучающим объектом, наличием в нём примесей. Особенно существенно влияет на поляризацию Р. и. магнитное поле (в экспериментах приходится учитывать магнитное поле Земли).
Читать дальшеИнтервал:
Закладка:
