БСЭ БСЭ - Большая Советская Энциклопедия (ЭЛ)
- Название:Большая Советская Энциклопедия (ЭЛ)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ЭЛ) краткое содержание
Большая Советская Энциклопедия (ЭЛ) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Скорости электродных реакций зависят от состава и концентрации электролита, от материала электрода, электродного потенциала, температуры и ряда других факторов. Скорость каждой электродной реакции определяется скоростью переноса электрических зарядов через единицу поверхности электрода в единицу времени; мерой скорости, следовательно, служит плотность тока.
Количество образующихся при Э. продуктов определяется законами Фарадея. Если на каждом из электродов одновременно образуется ряд продуктов в результате нескольких электрохимических реакций, доля тока (в %), идущая на образование продукта одной из них, называется выходом данного продукта по току.
Преимущества Э. перед химическим методами получения целевых продуктов заключаются в возможности сравнительно просто (регулируя ток) управлять скоростью и селективной направленностью реакций. Условия Э. легко контролировать, благодаря чему можно осуществлять процессы как в самых «мягких», так и в наиболее «жёстких» условиях окисления или восстановления, получать сильнейшие окислители и восстановители, используемые в науке и технике. Э. — основной метод промышленного производства алюминия, хлора и едкого натра, важнейший способ получения фтора, щелочных и щелочноземельных металлов, эффективный метод рафинирования металлов. Путём Э. воды производят водород и кислород. Электрохимический метод используется для синтеза органических соединений различных классов и многих окислителей (персульфатов, перманганатов, перхлоратов, перфторорганических соединений и др.). Применение Э. для обработки поверхностей включает как катодные процессы гальванотехники (в машиностроении, приборостроении, авиационной, электротехнической, электронной промышленности), так и анодные процессы полировки, травления, размерной анодно-механической обработки, оксидирования ( анодирования ) металлических изделий (см. также Электрофизические и электрохимические методы обработки ) . Путём Э. в контролируемых условиях осуществляют защиту от коррозии металлических сооружений и конструкций (анодная и катодная защита).
Лит. см. при ст. Электрохимия.
Э. В. Касаткин.
Электролизёры
Электролизёры,аппараты для электролиза, состоящие из одной или многих электролитических ячеек. Э. представляет собой сосуд (или систему сосудов), наполненный электролитом с размещенными в нём электродами — катодом и анодом, соединёнными соответственно с отрицательным и положительным полюсами источника постоянного тока. В промышленности и лабораторной практике применяют Э. различных типов и конструкций (например, открытые и герметически закрытые, для периодической и непрерывной работы, с неподвижными и движущимися электродами, с различными системами разделения продуктов электролиза). В зависимости от назначения Э. рассчитываются для работы при различных температурах — от минусовых (при электрохимическом синтезе малостойких кислородных соединений) до высоких плюсовых (при электролизе расплавленных электролитов в производстве алюминия, кальция и др. металлов). Соответственно Э . снабжают устройствами для нагрева или охлаждения электролита пли электродов.
Применяют Э. с диафрагмой — пористой перегородкой или мембраной, отделяющей катодное пространство от анодного, проницаемой для ионов, но затрудняющей механическое смешение и диффузию. Для изготовления диафрагм используются асбест, полимерные материалы и керамика, находят применения Э. с ионообменными мембранами. По способу включения в электрическую цепь Э. разделяются на моно- и биполярные. Монополярный Э. состоит из одной электролитической ячейки с электродами одной полярности, каждый из которых может состоять из нескольких элементов, включенных параллельно в цепь тока. Биполярный Э. имеет большое число ячеек (до 100—160), включенных последовательно в цепь тока, причём каждый электрод, за исключением двух крайних, работает одной стороной как катод, а другой как анод.
Для изготовления анодов применяют графит, углеграфитовые материалы, платину, окислы некоторых металлов, свинец и его сплавы; используются малоизнашивающиеся титановые аноды с активным покрытием из смеси окислов рутения и титана, а также платины и её сплавов. Для катодов в большинстве Э. используется сталь. Применяются также Э. с жидкими электродами (например, в одном из методов производства хлора и гидроокиси натрия в качестве катода используют ртуть). Некоторые Э. работают под давлением, например разложение воды ведётся под давлением до 4 Мн / м 2(40 кгс / см 2) ; разрабатываются Э. для работы под более высоким давлением. Материалы для изготовления Э. выбираются с учётом агрессивности электролита и продуктов электролиза, температуры и других условий. Широко применяется сталь, в том числе с различными защитными покрытиями, пластические массы, стекло и стеклопластики, керамика. Современные крупные Э. имеют высокую нагрузку: монополярные до 400—500 ка, биполярные — эквивалентную 1600 ка.
Л. М. Якименко.
Электролитическая диссоциация
Электролити'ческая диссоциа'ция,распад вещества на ионы при растворении. Э. д. происходит вследствие взаимодействия растворённого вещества с растворителем; по данным спектроскопических методов, это взаимодействие носит в значительной мере химический характер (см. Сольватация ) . Наряду с сольватирующей способностью молекул растворителя определённую роль в Э. д. играет также макроскопическое свойство растворителя — его диэлектрическая проницаемость.
Классическая теория Э. д. была создана С. Аррениусом и В. Оствальдом в 80-х гг. 19 в. Она основана на предположении о неполной диссоциации растворённого вещества, характеризуемой степенью диссоциации а, т. е. долей распавшихся молекул электролита. Динамическое равновесие между недиссоциированными молекулами и ионами описывается действующих масс законом. Например, Э. д. бинарного электролита КА выражается уравнением типа КА Û К ++ А -. Константа диссоциации К допределяется активностями катионов а К +, анионов а А- и недиссоциированных молекул а КАследующим образом:
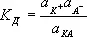 (1)
(1)
Значение К дзависит от природы растворённого вещества и растворителя, а также от температуры и может быть определено несколькими экспериментальными методами. Степень диссоциации ее может быть рассчитана при любой концентрации a электролита с помощью соотношения:
Читать дальшеИнтервал:
Закладка:
