Михаил Ермолаев - Биологическая химия
- Название:Биологическая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1974
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Ермолаев - Биологическая химия краткое содержание
В учебнике нашли отражение последние научные данные о ферментах, белках, гормонах, обмене веществ и энергии и т. д. Особое внимание обращено на значение и использование данных биохимии в медицине, в связи с чем расширены разделы, посвященные патологии разных видов обменов и их исследованиям в клинике Включены материалы по наследственным заболеваниям, связанным с нарушением синтеза белка и ферментов.
Учебник написан по программе, утвержденной Министерством здраво" хранения СССР, и предназначен для учащихся фельдшерско-лаборантских отделениях медицинских училищ.
Биологическая химия - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
В зависимости от пространственною расположения полипептидной цепи (третичная структура) молекулы белков могут быть различной формы. Если полипептидная цепь уложена в виде клубка, то молекула белка имеет в сущности шаровидную форму. Такие белки называются глобулярными (лат. globulus — шарик). В другой группе белков полипептидные цепи образуют молекулы нитевидной формы и белки называются фибриллярными (лат. fibrilla — нить). Эти белки различаются и по своим свойствам. Так, глобулярные белки хорошо растворимы в воде, фибриллярные — плохо или совсем не растворимы. Представителями глобулярных белков являются яичный белок, казеин молока, белки сыворотки крови и т. д. К фибриллярным белкам относятся белки опорных тканей: белки мышц — миозин, белки костей — оссеин, кератин, крови — фибрин и др.
Видовая и тканевая специфичность белков
Каждый вид животного организма отличается по количеству и составу содержащихся в нем веществ. Это в полной мере относится и к белкам. Так, при изучении состава гемоглобина разных видов животных и человека были обнаружены определенные, строго специфические различия, например в отношении входящих в его состав аминокислот. Так, в табл. 2 показано различное содержание двух аминокислот — метионина и цистеина в гемоглобине человека, собаки и крупного рогатого скота.

Таблица 2. Содержание метионина и цистеина в гемоглобине в процентах
Различия обнаружены при изучении состава инсулина и ряда других белков. Наряду с этим существуют определенные различия в составе белков в зависимости от возраста. Так, у плода человека в крови обнаружен специфический вид гемоглобина, который называется фетальным. Этот вид гемоглобина после рождения практически исчезает. При изучении его структуры также были выявлены определенные изменения аминокислотного состава по сравнению с гемоглобином взрослого человека.
Эти данные свидетельствуют о том, что структура белка внутри одного вида строится по вполне определенному плану, специфичному именно для представителей данного вида.
Важно отметить, что внутри одного и того же вида имеются и индивидуальные различия в составе белка. Показано, что одни особи обладают только одним видом гемоглобина и β-лактоглобулином молока, у других встречается смесь двух различных видов этих белков. Существуют и наследственные различия в составе белков, что в ряде случаев является причиной тяжелых наследственных заболеваний.
Приведенные примеры касались в основном гемоглобина как наиболее изученного белка, но все сказанное в полной мере относится и к другим белкам.
Вопрос тканевой специфичности белков в основе своей повторяет их видовую специфичность. Белки мышечной .ткани отличаются от белков костей или печени. Это можно подтвердить на примере ферментов. Например, и в печени, и в сердечной мышце находится фермент лактатдегидрогеназа, катализирующий синтез молочной кислоты. При детальном изучении свойств ферментов оказалось, что, несмотря на их одинаковую функцию, они различаются по некоторым свойствам Таким образом, каждый вид, каждый представитель этого вида, как и любая ткань, а возможно и клетка, характеризуется наличием строго специфичных белков, определяющих их индивидуальность.
Классификация белков
Все белки в зависимости от состава и структуры делятся на простые — протеины, которые состоят только из аминокислот, и сложные — протеиды, в молекуле которых, помимо белковой части, имеется еще и небелковая часть — простетическая группа .
Простые белки
Представителями простых белков являются альбумины и глобулины. Эти виды белков широко представлены в организме. Альбумины и глобулины практически встречаются во всех животных и растительных клетках и в большинстве жидкостей организма (плазма крови, сыворотка молока и др.). В сыворотке крови между альбуминами и глобулинами существует определенное отношение — альбумино-глобулиновый коэффициент (показатель А/Г).
По своим свойствам альбумины отличаются от глобулинов. Альбумины растворимы в воде, а глобулины — только в разбавленных растворах нейтральных солей. Молекулярный вес альбуминов меньше, чем глобулинов. Поэтому альбумины выпадают в осадок при полном насыщении водного раствора нейтральными солями, тогда как глобулины высаливаются при полунасыщении раствора. Этим свойством пользуются для получения антитоксических сывороток (противодифтерийная, противококлюшная и др.), так как антитоксины по своей химической природе являются γ-глобулинами.
Сложные белки — протеиды
Как уже было отмечено, сложные белки состоят из белковой части и небелковой — простетической группы, которая может быть представлена различными соединениями. Название протеидов зависит от названия простетической группы. К сложным белкам относятся: нуклеопротеиды, небелковая часть которых представлена нуклеиновыми кислотами; хромопротеиды — сложные белки, простетическая группа которых является окрашенным соединением, фосфопротеиды, имеющие в своем составе остатки фосфорных кислот; липопротеиды и глюкопротеиды Простетическими группами последних являются соответственно жиры и углеводы.
Нуклеопротеиды
Значение этого класса протеидов трудно переоценить, потому что они входят во все клетки организма и выполняют основные жизненные функции — являются носителями генетической информации и участвуют в биосинтезе белка. Белковая часть нуклеопротеидов представлена в основном протаминами и гистонами. Небелковая часть — это рибо- и дезоксирибонуклеиновые кислоты. Строение нуклеопротеидов представлено на следующей схеме:
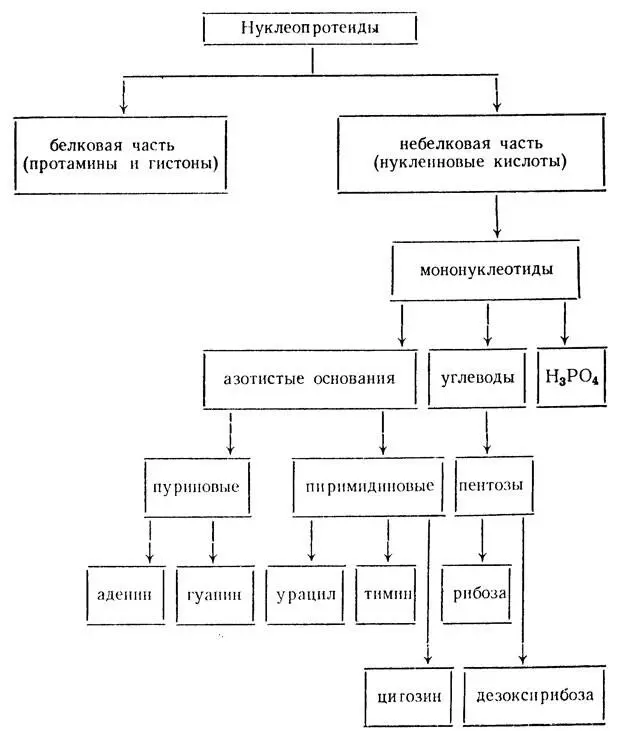
Схема 1
Нуклеопротеиды — это соединения с высоким молекулярным весом — от 25 000 до 1 000 000 и выше, состоящие из огромного числа мономеров — мононуклеотидов. Последние состоят из азотистых оснований, пентоз и остатка фосфорной кислоты.
Из пентоз в мононуклеотидах представлены рибозаи дезоксирибоза:
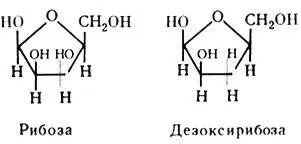
Азотистые основания являются производными пуринов или пиримидинов.
К пуриновым основаниям относятся аденин— 6-амино-пурин и гуанин— 2-амино-6-оксипурин.
Читать дальшеИнтервал:
Закладка:






