Елена Вовк - Неалкогольная жировая болезнь печени
- Название:Неалкогольная жировая болезнь печени
- Автор:
- Жанр:
- Издательство:Эксмо
- Год:2018
- Город:Москва
- ISBN:978-5-04-094647-1
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Елена Вовк - Неалкогольная жировая болезнь печени краткое содержание
Неалкогольная жировая болезнь печени - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
1) «средний» уровень доходов населения;
2) недавно начавшийся процесс активной урбанизации и необходимость для еще недавно сельского населения в течение жизни 1–2 поколений адаптироваться к высокой стрессовости жизни в мегаполисе;
3) урбанистический литогенный и атерогенный рационы питания приводят к срыву генетически детерминированных механизмов активной экскреции холестерина и поддержания его растворимости в желчи [36].
Универсальными признаками «литогенного» рациона современных горожан можно считать нарастающие в течение последних 2000 лет диспропорции в рационе:
✓ обилие продуктов с высоким содержанием рафинированных углеводов, насыщенных и жареных транс-жиров;
✓ дефицит продуктов, содержащих ПНЖК и антиоксиданты;
✓ недостаточное количество природных холеретиков и балластной (неперевариваемой) растительной клетчатки (рис. 21).
Среди факторов городской жизни существует еще один триггер НАЖБП — экологическое загрязнение, прежде всего органическими соединениями тяжелых металлов и диоксинами (ВОЗ, 2006). Например, в таком мегаполисе, как Москва, по данным Мосэкомониторинга, 100 % жителей живут в условиях «высокого и очень высокого» загрязнения воздуха: в 1 кубометре содержится 6–7 мг диоксида азота, диоксида серы, формальдегида и органических соединений хлора, ртути и свинца, мышьяка и т. д. (Авалиани С., Ревич Б., 2009).
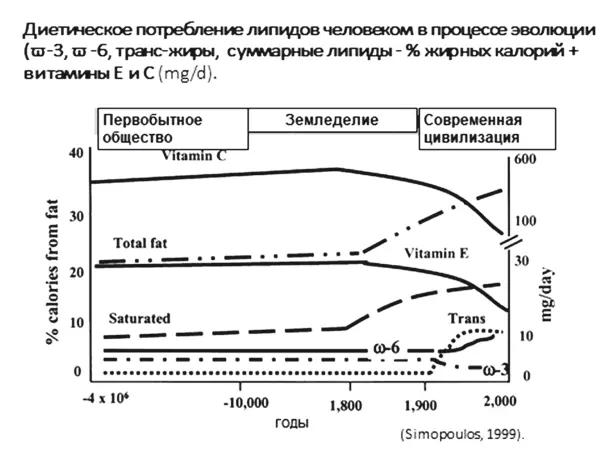
Рис. 21. Динамика структуры жиров в рационе человека в течение 10 тысяч лет (модифицировано по Simopoulos А.Р., 2000) [74]
Попадая внутрь организма с воздухом и водой, диоксины или органические соединения свинца из автовыхлопа включаются в энтерогепатическую циркуляцию и накапливаются в наружных клеточных мембранах и органеллах клеток, разрушая их ПНЖК и нарушая функциональное состояние мембран. В печени органические соли свинца нарушают синтез гема и снижают активность микросомальных оксидаз-ферментов I фазы метаболизма ксенобиотиков: С-редуктазы и CYP450, в частности, СУР 1А2 и ЗА4, находящихся в эндоплазматическом ретикулуме гепатоцитов и ответственных за окисление субстратов из окружающей среды, а также СУР2А6, 2С19, 2D6, 2Е6, 2D6, участвующих в окислении около 30 лекарств. Посредством блокады митохондриальной феррохелатазы свинец вызывает митохондриальную цитопатию и снижение уровня метаболической активности гепатоцита по всем направлениям [36].
Органические соли свинца также прямо нарушают детоксикацию желчных кислот и продуктов перекисного окисления липидов, поскольку они истощают гепатоцит по содержанию глутатионпероксидазы и сульфотрансферазы — ферментов II фазы метаболизма ксенобиотиков. Однако важнейшим механизмом, реализующим особую роль соединений свинца в развитии НАЖБП и ЖКБ, служит его универсальная способность избирательно накапливать в печени холестерин и липиды, вызывая, таким образом, формирование НАСГ и билиарной недостаточности (рис. 22).
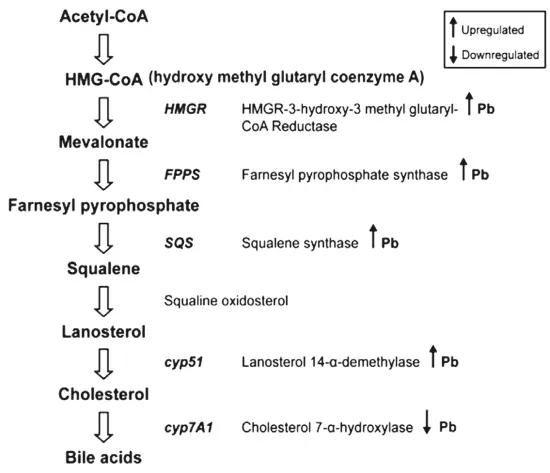
Рис. 22. Влияние свинца на синтез холестерина в печени (модифицировано по A Mudipalli, 2007)
Последствия хронической экологической интоксикации особенно опасны для пациентов групп риска:
✓ злоупотребляющих алкоголем;
✓ людей, работающих во вредных условиях;
✓ больных с MC и СД 2 типа;
✓ длительно принимающих гепатотоксичную лекарственную терапию (туберкулостатики, НПВП, фибраты, кетоконазол, пероральные контрацептивы);
✓ беременных женщин.
Таким образом, в печени сосредоточены метаболические и эндокринные механизмы, тонко регулирующие содержание ТГ, СЖК и холестерина в соответствии с:
1) потребностями в энергии (температурой окружающей среды, физической нагрузкой, активностью щитовидной железы);
2) потребностью в синтезе биологически активных веществ.
Так, большая, но ограниченная во времени физическая или другая стрессорная нагрузка приводит к активации липолиза в жировой ткани и росту концентрации СЖК, увеличению синтеза холестерина и его производных — прогестерона, минерало- и глюкокортикоидных гормонов, половых стероидов, а также фосфолипидов и желчных кислот, увеличению содержания в крови ЛПОНП, ЛПНП и ЛПВП. По окончании нагрузки избыточные липиды утилизируются или выводятся из организма. Нормальный физиологический процесс утилизации липидов и холестерина в плазме крови нарушается и приводит к стойкой гиперлипидемии, только если:
1) вследствие хронического стресса или возрастной инволюции активация симпатической нервной системы и потребность в увеличении содержания холестерина становится постоянной:
2) нарушается механизм выведения избытков холестерина.
У пациентов с МС, НАЖБП и СД 2 типа развивается специфический вариант высоко атерогенной дислипидемии, который образно назвают «липидный квартет»: ↑ титров ТГ, ЛПОНП, ЛППП и ЛПНП, ↓ титров ЛПВП — фенотип II b (рис. 23).
У пациентов с MC, НАЖБП и СД 2 типа развивается специфический вариант высоко атерогенной дислипидемии, который образно называют «липидный квартет»: ф титров ТГ, ЛПОНП, ЛППП и ЛПНП, ф титров ЛПВП — фенотип II b (рис. 23).
Ранее считалось, что высокие титры ЛПОНП и ЛППП не являются высоко атерогенными, поскольку эти липопротеиды содержат холестерин, который не может быть прямо мобилизован в сыворотку крови, не доступен для тканей и, следовательно, не может инфильтрировать интиму артерий или клеточные стенки. Согласно современным представлениям, роль ТГ, ЛПОНП в атерогенезе является важнейшей: из ЛПОНП образуются ЛППП, которые:
1) служат основным субстратом для образования высокоатерогенных ЛПНП;
2) будучи мелкими и жесткими частицами, способны инициировать локусы повреждения эндотелия артерий, в которых позднее образуются атеросклеротические бляшки.
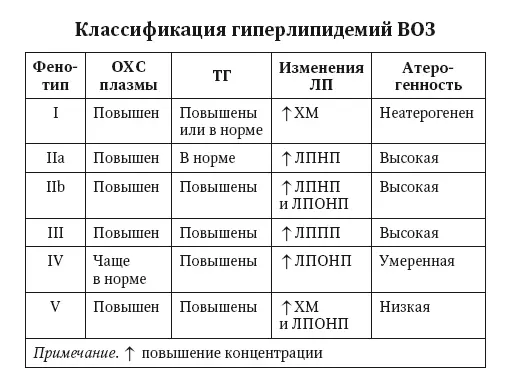
Рис. 23. Классификация гиперлипидемий (ВОЗ, 2009)
Терапия статинами, ингибирующими конечный этап синтеза холестерина, остается единственным эффективным методом снижения уровня ЛПНП и является «золотым стандартом» лечения атерогенной дислипидемии. Во множестве рандомизированных исследований показана высокая эффективность статинов в отношении уменьшения концентраций ЛПНП и снижения частоты коронарных событий и внезапной коронарной смерти (на 25–40 %). Терапия статинами показана всем больным с высоким фатальным риском по шкале SCORE уровнями ЛПНП > 2,5 ммоль/л для риска > 5 %, уровнем ЛПНП > 3,0 для риска < 5 %. Однако терапия статинами практически не влияет на уровень ЛПОНП и триглицеридов и, кроме того, в 5-10 % случаев сопровождается развитием диспепсии и преходящими нарушениями печеночных проб, а в 0,5 % случаев — миопатией и развитием рабдомиолиза, риск которых увеличивается при назначении в комбинациях с фибратами и ниацином. У пациентов с НАЖБП, получающих статины, также повышен риск неблагоприятного лекарственного взаимодействия при одновременном лечении амиодароном, клопидогрелем, глюкокортикоидами и другими широко применяемыми лекарственными средствами.
Читать дальшеИнтервал:
Закладка: