Виктор Сбойчаков - Микробиология с основами эпидемиологии и методами микробиологических исследований
- Название:Микробиология с основами эпидемиологии и методами микробиологических исследований
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:978-5-299-00404-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Виктор Сбойчаков - Микробиология с основами эпидемиологии и методами микробиологических исследований краткое содержание
Книга также будет полезна практическим лаборантам и фельдшерам, врачам микробиологам и студентам медицинских вузов.
Микробиология с основами эпидемиологии и методами микробиологических исследований - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Углеводный компонент вируса определяется клеткой хозяина, укрепляет суперкапсидную структуру, придавая ей жесткость. Удаление гликопротеидных комплексов у сложно устроенных вирусов ведет к потере способности к адсорбции на чувствительных клетках. У просто устроенных вирусов углеводный компонент отсутствует.
В составе вирусов могут быть и другие компоненты. В состав полипептидов, например, часто включаются фосфаты (аденовирусы, ретровирусы, герпесвирусы, поксвирусы, ортомиксовирусы), их конкретная функция пока точно не установлена. Некоторые вирусы содержат микроэлементы: медь, молибден, а отдельные вирусы – целый набор ферментов: поксвирусы – 10, ВИЧ – 4, вирус гриппа – 3 фермента. Ферменты обеспечивают вирусную репродукцию: реакцию полимеризации (образования иРНК), репликацию (образование новых нитей нуклеиновых кислот) по принципу комплементарности. В ряде случаев ферменты синтезируются за счет генома вируса.
Вирусы также активно используют клеточные ферменты, например, у гриппа гемагглютинин находится в составе шипов в неактивном состоянии и для адсорбции на клеточном эпителии необходима протеолитическая активация гемагглютинина за счет ферментов клеточного секрета. Только после этого достигается соответствие прикрепительного белка структурам чувствительной клетки.
У ДНК-геномных вирусов ДНК-зависимая полимераза обеспечивает синтез иРНК. Благодаря ферментам происходит модификация синтезированной цепочки НК: удлинение цепи, укорочение, «подчищение» или процессинг нуклеиновых кислот – разрезание и удаление из определенных участков 1 – 2 нуклеотидов, а затем сшивание этого участка лигазой.
2.4. Бактериофаги
Бактериофаг – вирус бактерий, паразитирующий только на живой микробной клетке и являющийся важным генетическим фактором микроорганизмов. Открыт в 1917 г. французским ученым д’Эррелем. Название бактериофага происходит от греч. «фагос» – пожиратель. Бактериофаг имеет корпускулярное строение и представляет собой шаровидное тело (головку) с отростком. Вирус покрыт белковой оболочкой. В головке фага заключены ДНК или РНК. Размеры фага колеблются в пределах 45 – 100 нм (рис. 11).
По сравнению с вирусами фаги довольно устойчивы во внешней среде. Они хорошо переносят низкие температуры, но при +70 °C инактивируются. Формалин инактивирует фаги через несколько минут. Также губительно действуют на фаги ультрафиолетовое и ионизирующее излучения, однако в малых дозах они могут вызвать мутации.
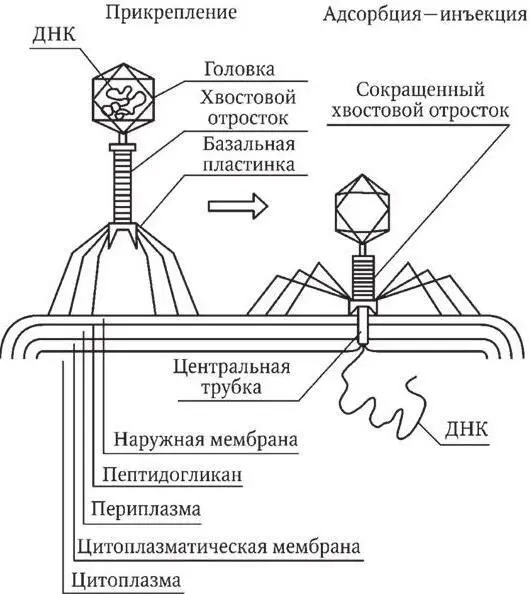
Рис. 11. Начальные этапы взаимодействия фага с оболочкой бактерии (по: Воробьев А. А. и Кривошеин Ю. С., 2002)
Стадии взаимодействия бактериофага с бактериальной клеткой:
I фаза – адсорбция на клетке при соответствии фаговых рецепторов с рецепторами бактериальной клетки;
II фаза – внедрение фага в клетку, через канал фага в клетку попадает его нуклеиновая кислота; в отличие от вирусов капсидные белки головки и отростка остаются вне клетки;
III фаза – репликация фаговой РНК или ДНК, синтез фагоспецифических ферментов транскрипции и репликации;
IV фаза – сборка фаговых частиц, которая происходит гораздо быстрее, чем при репродукции других вирусов;
V фаза – выход фагов из клетки происходит по типу взрыва, во время которого зараженные бактерии лизируются.
Существуют вирулентные и умеренные фаги. Вирулентные фаги вызывают инфекцию, заканчивающуюся лизисом бактериальных клеток и синтезом новых фаговых частиц. Умеренные фаги не лизируют зараженные ими клетки. ДНК этих фагов включается в хромосому бактерий и передается при их делении неограниченному числу потомков. Такой тип взаимодействия фага с клеткой называется лизогенией , а бактерии, несущие в геноме фаговую ДНК (профаг), называются лизогенными . Они широко распространены в природе и обнаруживаются в воде, почве, сточных водах, испражнениях больных и других биосубстратах.
Репродукция вирулентного фага в клетках бульонной бактериальной культуры сопровождается их лизисом и просветлением среды. На газоне чувствительных бактерий, выращенных на агаровой среде в чашке Петри, фаги образуют зоны очагового или сплошного лизиса, что зависит от их концентрации. Зоны очагового лизиса получили название негативных колоний фага или стерильных пятен-бляшек. Они имеют морфологию, характерную для определенных фагов, и образуются из одной фаговой частицы при внедрении ее и последующей репродукции в клетках микроорганизмов.
Большинство фагов характеризуется видоспецифичностью в отношении бактерий. Однако существуют фаги, способные поражать только отдельные варианты одного и того же вида бактерий. Их используют для определения фаговаров (фаготипов) внутри данного вида.
В практической работе фаги применяют для:
– фаготипирования бактерий, что важно для маркировки исследуемых культур при эпидемиологическом анализе заболеваний;
– дифференцировки бактериальных культур с целью установления их видовой принадлежности;
– фагодиагностики, заключающейся в выделении фага из организма больного (например, из испражнений), что косвенно свидетельствует о наличии в материале соответствующих микроорганизмов.
Фаги, так как они обладают антигенными свойствами, используют также для иммунизации животных с целью получения диагностических антифаговых сывороток. Кроме того, в отдельных случаях их применяют для лечения инфекционных заболеваний (фаготерапии).
2.5. Прионы
В 1957 г. американский врач Д. К. Гайдушек при обследовании в Новой Гвинее больных куру – смертельным дегенеративным заболеванием мозга, связанным с ритуальным каннибализмом, обратил внимание на сходство этого заболевания с давно известным медленным вирусным заболеванием овец – скрепи. Позже было выявлено сходство в развитии и некоторых других заболеваний, например болезни Крейтцфельдта – Якоба (БКЯ). За исследования в этой области Д. К. Гайдушек в 1976 г. был удостоен Нобелевской премии.
Инфекционный агент этих заболеваний имел важные отличия от других возбудителей, в том числе вирусов (табл. 1): он не был виден в электронный микроскоп, не вызывал иммунных реакций, не инактивировался факторами, разрушающими нуклеиновые кислоты, имел крайне малые размеры (меньше 25 нм). Ранее было высказано предположение, что этот агент представляет собой принципиально новый тип возбудителя – инфекционный белок.
Таблица 1
Сравнительная характеристика вирусов и прионов
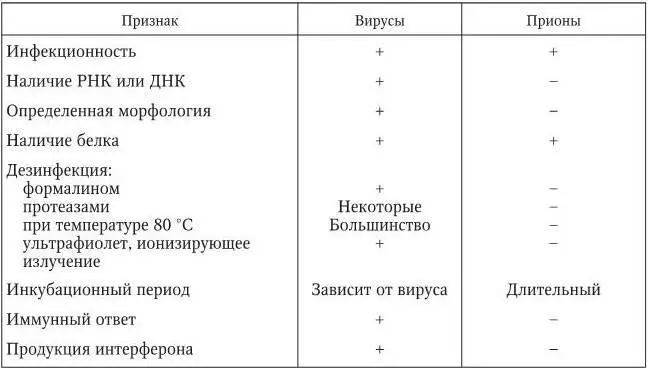
В 1982 г. американский ученый С. Прузинер, используя новые подходы к накоплению и очистке возбудителя, выделил соответствующую протеиновую фракцию. Он доказал, что этот белок способен вызывать спонгиформную энцефалопатию и назвал его прионом (сокращение от протеиновые инфекционные нуклеолы ). В 1984 г. С. Прузинер установил, что прионы лежат в основе как наследственных, так и инфекционных болезней, что вызвало полное недоумение многих специалистов. Значительно позже, в 1997 г., этому ученому была присуждена Нобелевская премия в области физиологии и медицины за серию научных работ о прионах.
Читать дальшеИнтервал:
Закладка:










