Михаил Никитин - Происхождение жизни. От туманности до клетки
- Название:Происхождение жизни. От туманности до клетки
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2016
- Город:Москва
- ISBN:978-5-9614-4350-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Никитин - Происхождение жизни. От туманности до клетки краткое содержание
Происхождение жизни. От туманности до клетки - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Можно проиллюстрировать три типа приведенных ответов на примере выбора азотистых оснований. Пара А-Т связана слабее, чем G-C (две водородных связи, а не три). Если заменить аденин на аминоаденин, то пара аА-Т будет тоже иметь три водородные связи. Такая замена позволила бы повысить точность копирования ДНК. Однако аминоаденин в ДНК не используется. Возможное функциональное объяснение: для оптимальной работы генома нужен выбор между сильными и слабыми связями в парах нуклеотидов. Рудиментарное объяснение: аденин устойчив к ультрафиолетовому излучению. В современных клетках это свойство аденина больше не важно, но менять аденин на другие молекулы уже слишком сложно. Объяснение путем исторической случайности: аденин легко образуется абиогенно из цианида или формамида, в отличие от аминоаденина, поэтому генетические механизмы сформировались раньше, чем появилась возможность попробовать аминоаденин.
Во всех случаях, когда мы спрашиваем «Почему бы не по-другому?», полезно пытаться придумать все три типа ответов, даже если мы не можем экспериментально их проверить.
Выбор химических элементов
Биомолекулы на 99 % состоят из четырех элементов: углерода, водорода, кислорода, азота. Оставшийся процент приходится в основном на фосфор и серу. Какие общие свойства отличают эти элементы?
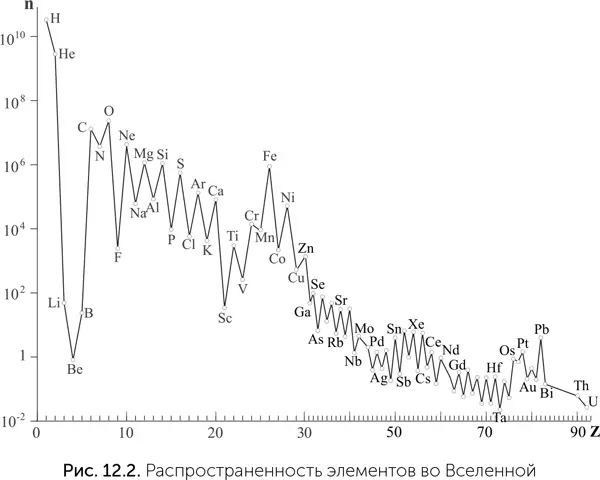
Во-первых, их очень много: все они, кроме фосфора, входят в десятку самых распространенных во Вселенной (рис. 12.2). Во-вторых, все эти элементы отличаются малыми размерами атомов. Размер атома определяется радиусом, на котором находятся самые внешние (валентные) электроны, и сложно зависит от положения атома в таблице Менделеева. В каждом периоде размер атома уменьшается с повышением атомного номера, потому что заряд ядра растет, и притяжение электронов к ядру усиливается. Но при переходе к следующему периоду появляется следующая электронная оболочка, и размер атома увеличивается скачком. C, N, O, P, S занимают правый верхний угол таблицы Менделеева и являются самыми маленькими атомами с валентностью 2 (O), 3 (N), 4 (C), 5 (P) и 6 (S), а водород – самый маленький атом с валентностью 1. В-третьих, все они, кроме водорода, образуют двойные и тройные химические связи. Помимо С, N, O, P и S стабильные двойные связи известны только у хлора, брома, мышьяка и селена.
Молекулы с двойными связями очень важны в биологии. Это азотистые основания (аденин, гуанин, цитозин, урацил), большинство витаминов, гем, хлорофилл и многие другие. Благодаря длинным системам сопряженных двойных связей биомолекулы могут взаимодействовать с видимым светом, обеспечивая окраску и фотосинтез. Кольцевые системы двойных связей в азотистых основаниях обеспечивают их плоскую форму и стэкинг-взаимодействие между соседними основаниями. Стэкинг-взаимодействие облегчает рост цепи при копировании и повышает устойчивость ДНК к ультрафиолету.
Сера и фосфор играют особую роль в биохимии. Их связи с другими атомами менее прочные, чем связи углерода, кислорода и азота. Поэтому фосфор и сера незаменимы в нестабильных промежуточных веществах биохимических реакций, для временного хранения энергии и переноса групп атомов с одних молекул на другие. Энергия, запасенная в фосфоэфирных (P-O-P и P-O-C) связях таких веществ, как АТФ, ацетилфосфат и креатинфосфат, используется для сшивания аминокислот в белки, нуклеотидов – в ДНК и других химических реакций. Сера используется для переноса кислотных групп на коферменте А (ацетил-КоА, сукцинил-КоА и т. д.), при этом энергия, запасенная в тиоэфирной связи (C-S-CO), расходуется на создание новых связей С-С. Другой серосодержащий кофермент, S-аденозил-метионин, аналогично переносит метильные (CH 3) группы и тоже участвует в создании новых связей С-С.
Углерод образует до четырех прочных связей с другими атомами, и из него легко строятся цепочки и разветвленные молекулы. Кремний практически не уступает ему в этом отношении (рис. 12.3). Более того, на поверхности Земли кремния в 150 раз больше, чем углерода, следовательно, доступность углерода не была причиной его выбора для биохимии.
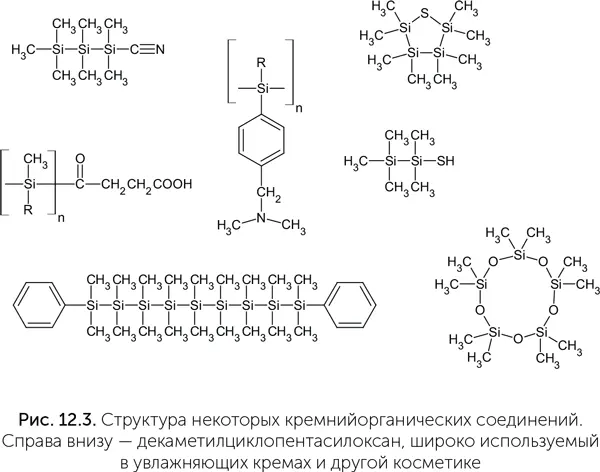
Хотя кремний действительно находится под углеродом в таблице Менделеева и во многом похож на него по свойствам, между ними есть и серьезные различия. Кремний обладает большим атомным радиусом, чем углерод, и поэтому прочность связи Si-Si вдвое меньше, чем связи C–C, а Si-H– меньше, чем C-H. Углерод легко образует двойные связи, в которых расстояние между атомами меньше, чем в обычных.
Кремний из-за большего размера атома практически не способен участвовать в двойных связях. В оксиде углерода CO 2углерод связан двойными связями с двумя атомами кислорода, и при обычных условиях СО 2 – газ. В оксиде кремния SiO 2каждый атом Si связан одинарными связями с четырьмя атомами кислорода, каждый из которых образует мостик между двумя атомами кремния. Поэтому SiO 2образует твердые тугоплавкие кристаллы, например кварц.
Многие соединения кремния более химически активны, чем их аналоги с углеродом. Если метан (СН 4) не реагирует с водой ни в обычных условиях, ни при сильном нагревании, то силан (SiH 4) при комнатной температуре быстро разлагается водой с выделением водорода и кремниевой кислоты:
SiH 4+ 3H 2O → 2H 2+ H 2SiO 3.
В подобные реакции вступают и многие другие соединения кремния, где атомы кремния не связаны с кислородом или азотом. Химик сказал бы примерно следующее: «Кремний – элемент третьего периода, поэтому его атом имеет незаполненные 3d-орбитали, которые позволяют ему проявлять электрофильные свойства и легче вступать в реакции с нуклеофилами».
Так что кремний, с одной стороны, образует очень прочные и устойчивые связи с кислородом, которые, в отличие от связей С-С, практически невозможно ослабить, а с другой – большинство других его химических связей неустойчивы в присутствии воды, аммиака и кислот. Поэтому практически в любых известных в космосе условиях кремний находится в виде устойчивых кристаллов оксида кремния и силикатов, иногда – карбидов и нитридов кремния, но не образует тех сложных молекул, которые получены в лаборатории. Углерод же не только на планетах, но и в межзвездных газово-пылевых облаках легко образует разнообразные органические соединения.
Известны и другие элементы, которые образуют сложные и разнообразные молекулы. Например, сосед углерода слева в периодической системе – бор. Его атом имеет три валентных (образующих химические связи) электрона, поэтому с кислородом образует три связи (например, в борной кислоте H 3BO 3). При этом атом бора не может достроить свою внешнюю электронную оболочку до восьми и образует уникальные дополнительные связи, охватывающие сразу три атома (рис. 12.4, справа).
Читать дальшеИнтервал:
Закладка:







