Михаил Никитин - Происхождение жизни. От туманности до клетки
- Название:Происхождение жизни. От туманности до клетки
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2016
- Город:Москва
- ISBN:978-5-9614-4350-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Никитин - Происхождение жизни. От туманности до клетки краткое содержание
Происхождение жизни. От туманности до клетки - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Процесс фотосинтеза, как он описан в школьных учебниках, состоит из световых и темновых реакций. Световые реакции сводятся к синтезу АТФ и восстановителей, таких как НАДФН, при помощи света и какого-либо донора электронов. Темновые реакции – это восстановление СО 2при помощи НАДФН и АТФ в цикле Кальвина или, реже, в других реакциях, и они уже обсуждались в главе о происхождении обмена веществ. Темновые реакции не уникальны для фотосинтеза. Тот же цикл Кальвина работает и при хемосинтезе, и свет не принимает участия в его реакциях.
Напомним структуру фотосинтетического аппарата зеленых растений. Его функциональное ядро составляют реакционные центры – встроенные в мембрану белки, с которыми связаны молекулы хлорофилла – по две в каждом реакционном центре и несколько вспомогательных, передающих энергию света в центр. Возбужденные молекулы хлорофилла передают электроны на молекулы-переносчики, и затем они попадают в электрон-транспортную цепь. В отличие от дыхательной цепи, в которой электрический ток создается «химической батареей», полюса которой – НАДН и кислород, здесь электрический ток создают реакционные центры фотосистем, работающие подобно солнечным батареям. Они питают две нагрузки: во-первых, за счет энергии света происходит электролиз воды с выделением кислорода. Во-вторых, как и в дыхательной цепи, ток электронов через механизм Q-цикла преобразуется в ток протонов через мембрану и синтез АТФ на роторной АТФазе. Напряжения, создаваемого одной фотосистемой, недостаточно для электролиза воды, поэтому две фотосистемы соединяются последовательно. Как мы помним, модули электрон-транспортных цепей соединяются подвижными переносчиками электронов, поэтому для последовательного соединения нужны разные типы переносчиков и несовместимые «разъемы» для них.
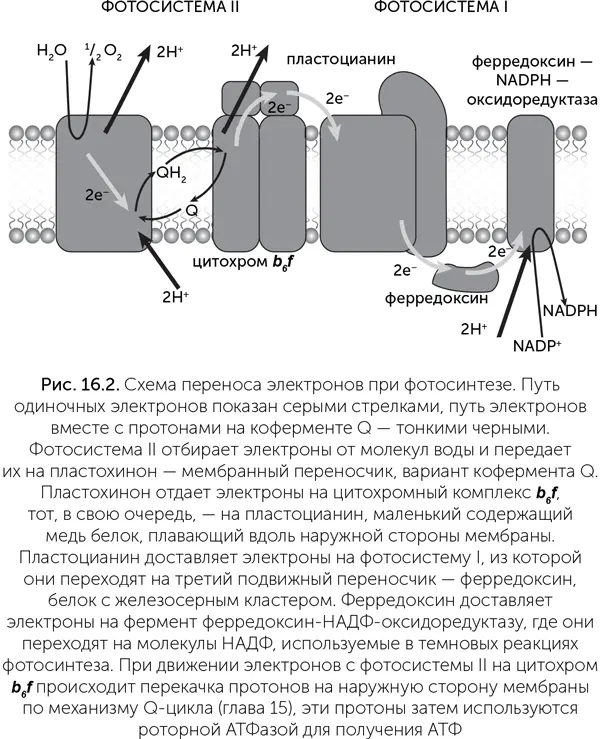
Реакционные центры делятся на два типа по используемым переносчикам электронов: фотосистемы I типа (ФСI) передают электроны на ферредоксин – маленький водорастворимый белок с железосерным кластером, а фотосистемы II типа (ФСII) – на хиноны, плавающие в мембране. Цианобактерии и хлоропласты растений обладают обоими типами фотосистем, а различные фотосинтезирующие бактерии – только одним типом из двух. Электроны ФСI через ферредоксин переносятся на НАДФ и затем используются в реакциях восстановления разных органических веществ. Электроны ФСII проходят через хиноны на цитохромный комплекс b6f , отдавая часть энергии на протонный ток и синтез АТФ, и далее на ФСI. В цианобактериях и хлоропластах растений окисленная ФСII с помощью водоокисляющего комплекса восполняет недостающие электроны из молекул воды, выделяя кислород. Кроме того, если клетке требуется больше АТФ, возможен циклический транспорт электронов по маршруту ФСII – хинон – цитохром b6f – ФСII (рис. 16.2). Реакционные центры окружены большим количеством вспомогательных антенных белков, также связывающих хлорофилл, которые поглощают световые кванты и передают возбуждение на реакционные центры.
Разнообразие систем, запасающих энергию света
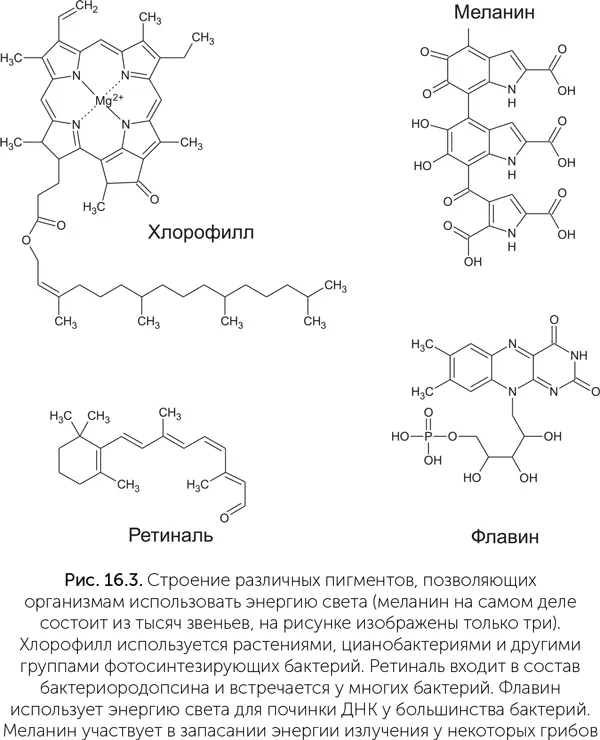
Очевидно, что столь сложная система из хлорофиллов и других пигментов [16]и электрон-транспортных цепей не могла возникнуть сразу. У нее должны были быть более простые предшественники, а возможно, и альтернативные системы фотосинтеза, не использующие хлорофилл. Как мы помним из предыдущих глав, в состав живых систем с самого начала входили молекулы с особыми отношениями со светом. Например, все азотистые основания эффективно рассеивают энергию ультрафиолетового света в тепло, защищая соседние молекулы. Адениновые нуклеотиды в растворе также способны за счет энергии света присоединять фосфатные группы, синтезируя АТФ. Древние окислительно-восстановительные коферменты, такие как НАД и ФАД, тоже могли пройти отбор на особые фотохимические свойства. Как мы помним из главы про мир РНК-коэнзимов, ФАД (флавинадениндинуклеотид) и в современном мире проводит одну реакцию при помощи энергии света. Это реакция восстановления тиминовых димеров – одного из продуктов повреждения ДНК ультрафиолетом. В ходе экспериментов было обнаружено, что силикатно-протеиноидные микросферы, содержащие флавин, могут за счет энергии света синтезировать АТФ из АДФ и фосфата (рис. 16.3).
У животных и растений на основе бактериальной фотолиазы возникли криптохромы – ФАД-содержащие светочувствительные белки, регулирующие суточные и сезонные ритмы. Как ни удивительно, у животных криптохромы также участвуют в восприятии магнитного поля при помощи магниточувствительной реакции с анион-радикалом кислорода (Solovyov, Schulten, 2009).
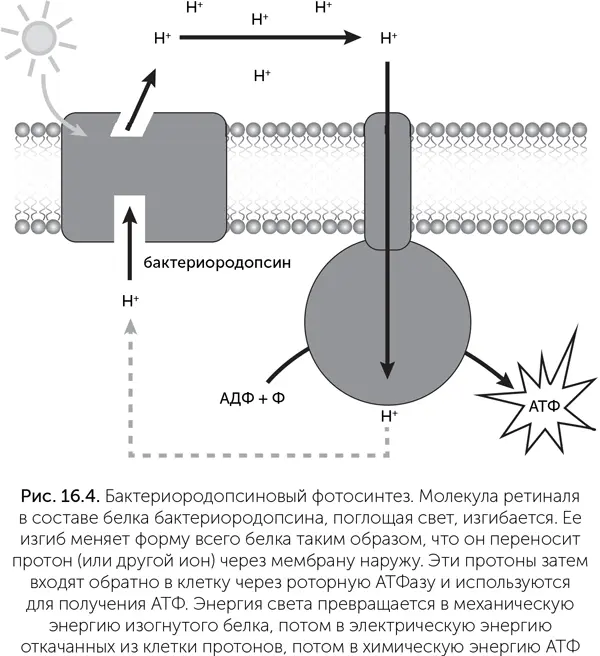
Другая группа светопоглощающих пигментов живых клеток – каротиноиды – тоже имеет разнообразные интересные функции. Один из каротиноидов, ретиналь, поглощает синий и голубой свет и превращает их энергию в механические изгибы молекулы, меняющей форму с прямой на изогнутую и обратно (рис. 16.4). В комплексе с мембранными белками бактериородопсинами ретиналь может переносить протоны, ионы натрия и даже ионы хлора через мембрану. Пропуская эти ионы обратно через вращающуюся мембранную АТФазу, клетка может получать АТФ за счет энергии света при помощи лишь одного дополнительного белка. Такая система гораздо надежнее и устойчивее к экстремальным условиям, чем сложные хлорофиллсодержащие фотосистемы. Бактериородопсины были впервые найдены у Halobacterium halobium, населяющей пересоленные лагуны, но в последнее время обнаружено, что они широко распространены у самых разных морских и пресноводных бактерий и позволяют им подолгу активно плавать без пищи. Родственные ретинальсодержащие белки – родопсины – работают в органах зрения всех животных, и благодаря им вы можете читать этот текст. Однако у одной глубоководной рыбы в глазах обнаружен и хлорофилл, позволяющий ей видеть в ближнем инфракрасном диапазоне! (Douglas et al., 1998).
Каротиноиды относятся к терпеновым веществам, гидрофобны и часто находятся в мембранах среди липидов. Самые распространенные каротиноиды, такие как бета-каротин, лежат в мембране параллельно хвостам липидов, проходя от одной стороны мембраны до другой. Скорее всего, исходно они защищали двойные связи древних липидов от повреждения ультрафиолетом, снимая с них возбуждение и рассеивая его в тепло, на самых ранних этапах эволюции мембран.
Читать дальшеИнтервал:
Закладка:







