Сергей Титов - Естествознание. Базовый уровень. 10 класс
- Название:Естествознание. Базовый уровень. 10 класс
- Автор:
- Жанр:
- Издательство:Array Литагент «Дрофа»
- Год:2013
- Город:Москва
- ISBN:978-5-358-13589-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Сергей Титов - Естествознание. Базовый уровень. 10 класс краткое содержание
Учебник объединяет сведения об основных законах и закономерностях, наиболее важных открытиях и достижениях в области химии, физики, астрономии, что формирует у учащихся представление о природе как целостной системе, а также о взаимосвязи человека, природы и общества.
Современное оформление, многоуровневые вопросы и задания, дополнительная информация и возможность параллельной работы с электронным приложением способствуют эффективному усвоению учебного материала.
Учебник адресован учащимся 10 класса.
Естествознание. Базовый уровень. 10 класс - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Существует огромное многообразие химических реакций. Простейшие из них можно условно разделить на четыре группы: реакции соединения, разложения, замещения и обмена.
В реакциях соединения из нескольких исходных веществ образуется одно сложное вещество. Примером такого вида реакций может служить процесс образования зелёного налёта малахита (CuOH) 2CO 3на поверхности бронзовых изделий (рис. 131):
2Cu + O 2+ H 2O + CO 2= (CuOH) 2CO 3.
Реакции разложения приводят к распаду молекул одного исходного сложного вещества на несколько продуктов. Такие реакции чаще протекают при нагревании. Некоторые вещества разлагаются под действием света. Так, соединения серебра на свету чернеют вследствие выделения серебра. На этом процессе основана чёрно-белая фотография.
Реакции замещения – это реакции между простым и сложным веществами, в результате которых образуются два новых вещества (простое и сложное).
Реакции обмена – это реакции взаимодействия между двумя сложными веществами, при котором они обмениваются атомами или группами атомов.

Рис. 131. Примером реакции соединения является процесс образования зелёного налёта малахита на поверхности бронзовых изделий
1. Какую информацию можно получить на основе уравнения химической реакции?
2. Какие вещества образуются в результате фотосинтеза?
3. Почему в химии применяют физическую величину «количество вещества»? В каких единицах она измеряется?
1. Подберите эпиграф к данному параграфу.
2. При реакции газообразного водорода H 2с газообразным хлором Cl 2образуется хлороводород HCl. Найдите в периодической системе атомную массу хлора и определите, какое количество водорода и хлора надо использовать для того, чтобы получить 10 г хлороводорода.
§ 51 Скорость и энергия химических реакций
Скоростью химической реакции называется изменение концентрации одного из реагирующих веществ за единицу времени. Для того чтобы произошла химическая реакция, атомы или молекулы реагирующих веществ должны прийти в соприкосновение или, попросту говоря, столкнуться. Это необходимое условие для возникновения реакции, но оно не является достаточным. Взаимодействующие частицы должны обладать определённым сродством друг к другу. Это сродство зависит от строения и энергии атомов и молекул, и чем оно больше, тем выше вероятность того, что они образуют соединение. Очевидно, что чем больше частиц содержится в данном объёме реакционной среды, тем чаще они будут сталкиваться. Поэтому скорость реакции пропорциональна произведению концентраций реагирующих веществ. Это правило называют законом действующих масс. Он был сформулирован норвежскими химиками К. Гульдбергом и П. Вааге в 1867 г. Закон действующих масс выражают в виде формулы:
V = k [A] a• [B] b ,
где [A] и [B] – концентрации реагирующих веществ, а и b – их стехиометрические коэффициенты. Величина k называется константой скорости реакции и зависит от степени сродства реагирующих веществ и внешних факторов, влияющих на скорость химической реакции, например температуры.
При повышении температуры скорость движения молекул увеличивается и, следовательно, увеличивается не только вероятность, но и, что гораздо важнее, энергия их соударения. Согласно правилу Вант-Гоффа, при повышении температуры на каждые 10 °C скорость реакции возрастает в 2–4 раза. Отношение константы скорости реакции, протекающей при определённой температуре, к константе скорости при температуре в 10 раз меньшей называют температурным коэффициентом химической реакции.
Если один из компонентов реакции находится в твёрдом состоянии, а другой – в жидком или газообразном, то на скорость реакции влияет также величина поверхности, которой они соприкасаются между собой. Например, растворение металла в кислоте будет происходить тем быстрее, чем больше степень его измельчения. Если опустить в кислоту большой кусок металла, он может реагировать с ней очень долго, а если то же количество металла растереть в порошок, реакция пройдёт практически мгновенно (рис. 132).
Очень важным фактором протекания химической реакции является энергетическая составляющая. Энергию, необходимую для начала реакции, называют энергией активации. Чем меньше энергия активации, тем быстрее протекает реакция. Например, при образовании ионной связи между катионами и анионами энергия активации очень мала, поэтому такие реакции протекают почти мгновенно.
Многие химические реакции можно ускорить или замедлить введением в реакционную среду некоторых дополнительных веществ. Эти вещества не участвуют в реакции и не расходуются в ходе её протекания, но оказывают влияние на её скорость. Вещества, ускоряющие реакцию, называют катализаторами, а вещества, оказывающие противоположное действие, – ингибиторами. Процесс ускорения реакций под действием катализатора называют катализом . Катализаторы чаще всего действуют следующим образом. На их поверхности имеются особые участки – активные центры. К этим участкам присоединяются и накапливаются молекулы реагентов. Такое явление называют адсорбцией.

Рис. 132. Зависимость скорости реакции от площади соприкосновения реагирующих веществ
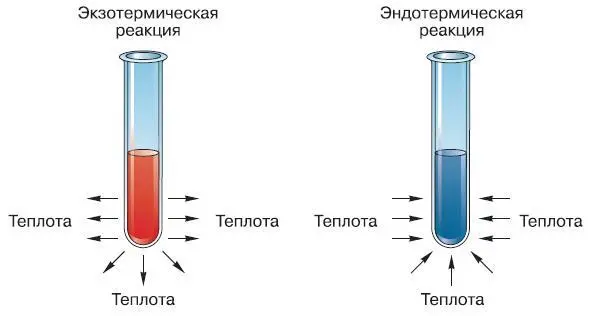
Рис. 133. Схематическое изображение экзотермической и эндотермической реакций
В результате в районе активных центров концентрация взаимодействующих молекул становится очень большой, и это ведёт к ускорению реакции. Кроме того, под действием катализатора у адсорбированных молекул ослабляются связи между атомами.
Как правило, сумма энергий исходных реагентов не бывает равной сумме энергий конечных продуктов реакции. Образующиеся в результате химической реакции вещества обладают либо меньшей, либо большей энергией по сравнению с исходными веществами. В первом случае реакция сопровождается выделением лишней энергии в виде кинетической энергии молекул, т. е. тепла. Такие реакции называют экзотермическими (от лат. exo – наружу и thermo – тепловой) (рис. 133). Так, экзотермической реакцией является любое горение (рис. 134).
Читать дальшеИнтервал:
Закладка:










