Николай Бетенеков - Физико-химические основы синтеза и применения тонкослойных неорганических сорбентов
- Название:Физико-химические основы синтеза и применения тонкослойных неорганических сорбентов
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:2019
- ISBN:978-5-532-10887-5
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Бетенеков - Физико-химические основы синтеза и применения тонкослойных неорганических сорбентов краткое содержание
Физико-химические основы синтеза и применения тонкослойных неорганических сорбентов - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Ион UO 2 2+имеет координационное число 6. Атомы кислорода образуют линейную конфигурацию О–U–O и расположены на коротких расстояниях от атома урана, а шесть лигандов Н 2О находятся вокруг атома урана в положениях, отвечающих конфигурации гексагональной бипирамиды:
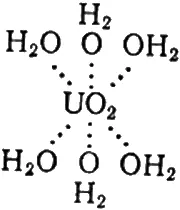
Схематически процесс перехода от мономерного иона к полимерному можно представить следующим образом:
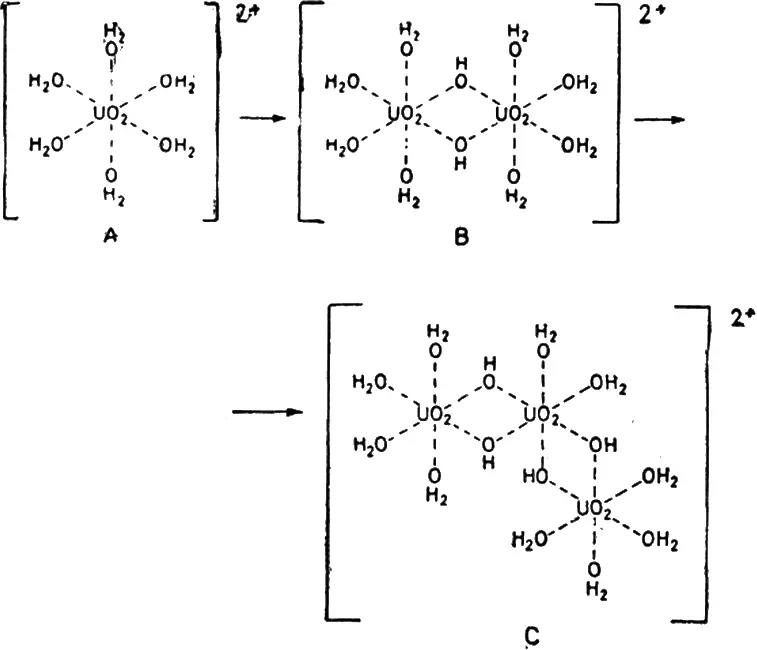
В результате происходит последовательное образование димера (B) и тримера (C). В общем виде эту последовательность можно изобразить следующим образом:
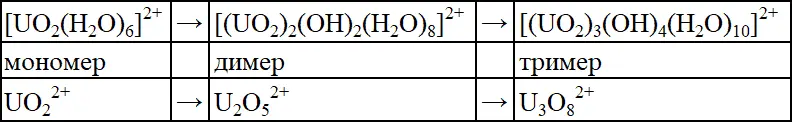
В осуществлении последовательного перехода от мономерного иона к полимерному по крайней мере два явления играют роль: протолиз и полимеризация. Считают, что реакция протолиза быстрая, т.к. эта реакция определяет взаимодействие простого иона с окружающей жидкостью, в которой состояние равновесия определяется рН (соотношением ОН/Н 2О). Скорость протекания протолиза обусловлена значением рН системы. В результате происходит уменьшение положительного заряда иона, взаимное отталкивание между катионами в растворе ослабляется, благодаря чему увеличивается скорость ориентированной агломерации – полимеризации. Полимеризация, как правило, протекает медленно и является скорость определяющей стадией. Процесс полимеризации осуществляется путем образования ол-связи, в результате чего образуются оловые соединения.
Оловые соединения – это комплексные соединения, в которых атомы металла связаны между собой посредством мостиковых ОН-групп

Чтобы их можно было отличить от гидроксогрупп, их называют «ол-группы». Координированная ОН-группа связана только с одним атомом металла
(–М–ОН). Процесс образования оловых соединений из гидроксосоединений называется оляцией.
Оляция часто сопровождается оксоляцией и/или замещение анионами.
Оксоляция – это превращение оловых групп в мостиковые оксогруппы
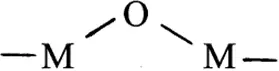
причем каждая оловая группа при этом отщепляет протон.
Замещение анионами состоит в замещении координированной группы, такой, как анион, гидроксогруппа, аква– или ол-группа, другим анионом.
Процесс оляции в принципе не ограничен и может продолжаться с образованием полимеров до тех пор, пока продукт каждой последующей стадии содержит аква– или гидроксогруппы.
Первой стадией непрерывного процесса оляции является гидролиз. Степень гидролиза возрастает по мере повышения температуры, она зависит от природы аниона и особенно от рН раствора. Если к нагретому раствору соли добавлять щелочь в количестве не достаточном для полной нейтрализации, то вместо осаждения гидроксида или основной соли протекает процесс полимеризации. Начальные стадии этого процесса показаны на примере урана. При углублении этого процесса могут образовываться частицы коллоидных размеров с молекулярной массой 400 – 1000. Получаемые макромолекулы могут иметь различную структуру и кольцевую, и зигзагообразную и др. Если в эти процессы вступают аквагруппы, присоединенные к атомам металла, находящимся внутри цепи или на ее конце, то могут образовываться полимеры с поперечными связями, образуя трехмерные структуры. Как сказано ранее, координированные молекулы воды в гидратированном ионе уранила отвечают конфигурации гексагональной бипирамиды. Если считать, что образующиеся в результате протолиза ионы гидроксила, которые могут играть роль ол-мостиков, сохраняют ту же кофигурацию, то мы получаем трехмерную структуру, в которой ОН-группы располагаются в вершинах деформированного гексагонального цикла (рис. 1.9). Образующиеся объемные структуры имеют не только химический состав, но и элементы строения, присущие выпадающим осадкам.
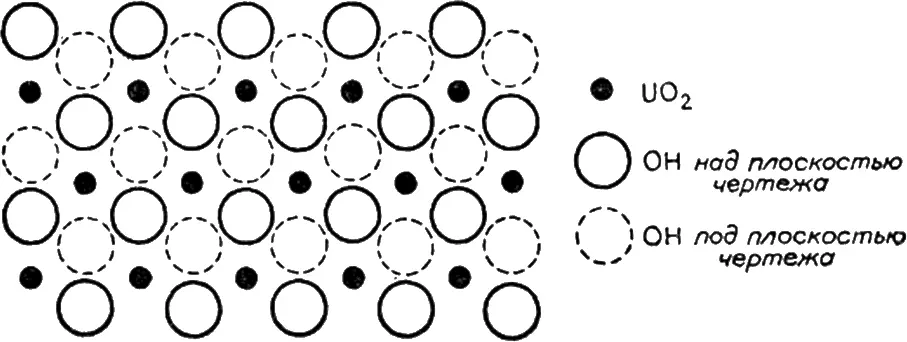
Рис. 1.9. Конфигурация слоя UO 2(OH) 2в кристалле UO 3· 2H 2O [7].
Проявление процесса оляции будет заключаться в уменьшении рН раствора в процессе выдержки. При титровании раствора соли щелочью рН немедленно повышается, но если оставить раствор стоять на некоторое время, то рН будет медленно понижаться. Это будет продолжаться до тех пор, пока добавленное количество щелочи не будет достаточно для осаждения гидроксида.Это явление связано с процессами гидролиза и оляции, в результате которых происходит выделение ионов Н +, приводящее к снижению рН. Таким образом можно добавить, не вызывая осаждения такое количество щелочи, которое, будучи прибавлено сразу, привело бы к образованию осадка.
Например, на кривой титрования 0, 05 моль/л раствора UO 2(NO 3) 21 моль/л раствором аммиака прерывание титрования на 15 часов при соотношении NH 3/U = 1, 67 привело к изменению значения рН от 4, 88 до 3, 70 (рис. 1.10).
Процессу оляции благоприятствует повышение концентрации и температуры, особенно повышение концентрации щелочи. Разбавление или охлаждение растворов оловых соединений очень медленно обращает процесс, т.е. уменьшается реакционная способность координированных ОН –групп.
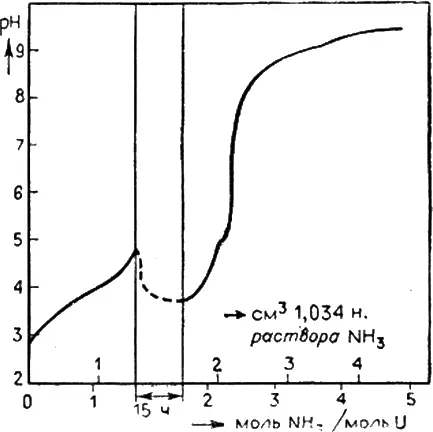
Рис. 1.10. Влияние прерывания на кривую титрования 0, 05 моль/л раствора UO 2(NO 3) 21 моль/л раствором аммиака [7].
Было показано, что растворы основных солей хрома при нагревании становятся более кислыми, причем растворимость солей уменьшается. Если растворы охладить, то спустя длительное время рН раствора принимает прежнее значение. (Эффект тот же, что и прибавлении щелочи.) При этом протекает процесс оксоляции, т.е. превращение оловых групп в оксо-группы путем отщепления ионов водорода.
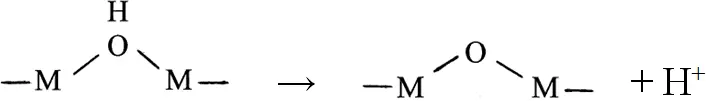
Несмотря на то, что процессы оляции и оксоляции обратимы, требуется достаточно длительное время, чтобы кислотность нагретого, а затем охлажденного раствора приняла прежнее значение. Деоксоляция необычайно медленный процесс. В общем, оловые соединения деполимеризуются с большей легкостью, чем оксосоединения, т.к. протоны легче взаимодействуют с оловыми группами, чем с оксогруппами.
Читать дальшеИнтервал:
Закладка: