Михаил Левицкий - Карнавал молекул. Химия необычная и забавная
- Название:Карнавал молекул. Химия необычная и забавная
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2019
- Город:Москва
- ISBN:978-5-0013-9101-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Левицкий - Карнавал молекул. Химия необычная и забавная краткое содержание
В книге рассказано о некоторых драматичных, а, порой, забавных поворотах судьбы как самих открытий, так и их авторов. Кроме того, читатель потренируется в решении занятных задач, что особенно приятно, когда рядом помещена подсказка, а потом и сам ответ.
В отличие от учебника в книге нет последовательного изложения основ химии, поэтому ее можно читать, начиная с любой главы.
Карнавал молекул. Химия необычная и забавная - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Для сравнительной оценки силы суперкислот водная среда не подходит, поэтому была выбрана иная шкала, она основана на их способности протонировать органические основания (например, анилин). В качестве точки отсчета взята 100 %-ная серная кислота. По этой шкале трифторметансульфоновая и фторсульфоновая кислоты в тысячу раз сильнее серной кислоты. Недостаток таких кислот состоит в том, что их анионы необычайно реакционноспособны и часто «вмешиваются» в процесс протонирования, приводя к побочным продуктам. Они столь агрессивны, что могут разъедать стекло. Тем не менее силу этих кислот удалось превзойти.
В 2006 г. американский ученый К.А. Рид из Калифорнийского университета совместно с российским ученым Е.С. Стояновым из Института катализа Сибирского отделения РАН получили еще более сильную кислоту – она превосходит серную кислоту в миллион раз. Это протонсодержащая кислота, у которой анион представляет собой каркас, собранный из атомов бора и атома углерода (молекула карборана), ко всем атомам бора присоединены атомы хлора с той же целью, с какой были введены атомы фтора в суперкислоты (рядом со структурной формулой на рис. 4.25 показана объемная модель аниона).
Авторы скромно назвали полученное соединение карборановой кислотой, хотя могли бы позволить себе яркое рекламное название, например экстрасуперкислота. Отрицательный заряд в ней расположен не у конкретного атома, а равномерно «размазан» по всему каркасу, что заметно снижает реакционную способность аниона, потому он пассивен, кроме того, сам каркас очень устойчив. Эту кислоту, как отмечают авторы, можно хранить в стеклянной таре. С ее помощью удалось протонировать при комнатной температуре органические соединения, такие как изобутен или толуол до соответствующих протонированных производных (рис. 4.26).
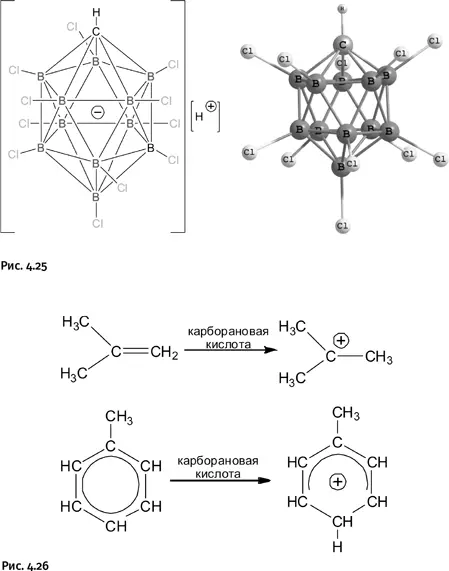
Благодаря тому что карборановый анион инертен и не затрагивает продукты реакции, полученный трет -бутильный катион (верхняя строчка показанной схемы) оказалось возможным выделить и хранить в виде кристаллического вещества, что ранее было недостижимо.
Авторы намечают протонировать этой кислотой атомы ксенона, полагая, что им удастся «расшевелить» даже такой необычайно инертный объект.
Новая «Царская водка»
Внутри каждого из нас царская душа,
каждый хочет, чтобы ему было все позволено,
но не хочет быть жертвой чужого произвола.
ЛУЦИЙ СЕНЕКА-МЛАДШИЙПроизводители спиртных напитков, желая привлечь покупателей, дают различным сортам водки звучные имена; самое яркое, пожалуй, «Царская водка», что предполагает необыкновенные вкусовые качества (рис. 4.27). Такую водку можно увидеть на прилавках магазинов, но химиков от этого названия буквально передергивает, поскольку они знают, что это словосочетание означает нечто совсем неаппетитное – едкая жидкость, растворяющая «царя металлов», т. е. золото.

Царская водка – не напиток
Царская водка появилась во времена алхимии, она представляет собой смесь трех объемных частей концентрированной соляной кислоты и одной объемной части концентрированной азотной. Такая смесь превращает в хлориды даже золото и платину, которые нерастворимы в каждой из этих кислот в отдельности.
Сама царская водка не просто смесь кислот, это продукт их взаимодействия, в результате чего получаются нитрозилхлорид NOCl и хлор (рис. 4.28).
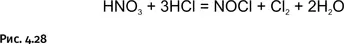
Еще древние алхимики знали, что царская водка должна быть свежеприготовленной. Все дело в том, что при длительном хранении из нее улетучивается хлор и она перестает работать.
Два реагента, образовавшиеся в царской водке, взаимодействуют с металлическим золотом Au, переводя его в хлорид AuCl 3(рис. 4.29).
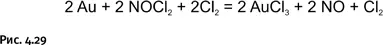
Образовавшийся хлорид золота присоединяет молекулу HCl, образуя комплекс – золотохлористоводородную кислоту H(AuCl 4). Обычно такой продукт называют хлорным золотом, он кристаллизуется из водного раствора с четырьмя молекулами воды H(AuCl 4) ·4Н 2О в виде светло-желтых кристаллов.
С платиной реакция протекает точно так же, только хлорид платины присоединяет не одну, а две молекулы HCl, давая платинохлористоводородную кислоту H 2(PtCl 6), которая при концентрировании раствора образует красно-бурые кристаллы состава H 2(PtCl 6)·6H 2O.
Сразу отметим, что термин «растворение» здесь и далее мы используем условно, так исторически сложилось – когда речь идет о царской водке, употребляют этот термин. Если происходит истинное растворение, то после удаления растворителя соединение получают в том же виде, в каком оно было до растворения. В тех случаях, которые мы обсуждаем, металлы не просто растворяются, а переходят в хлориды. Итак, это химическая реакция, подобная взаимодействию более активных металлов, например цинка или железа с соляной кислотой. Взаимодействие металлов с кислотами, приводящее к получению солей, исторически всегда было объектом внимания неорганической химии. Постепенно к реакциям, позволяющим переводить металлы в их соединения, подключилась и органическая химия.
Металлы и органические растворители
В 90-х гг. ХХ в. исследователями было обнаружено, что металлы можно «растворять» в органических растворителях. Внешне это выглядит, как «растворение» металла в кислоте, только вместо кислот используют органические соединения, что весьма необычно. Наиболее универсальной оказалась пара органических растворителей: диметилсульфоксид (ДМСО) Me 2S=O и четыреххлористый углерод CCl 4. Такая смесь способна растворять Co, Cr, Fe, Ni, Cu, Zn, Cd, Mo, W. Вместо ДМСО с таким же успехом можно использовать диметилформамид (ДМФА) Me 2N – C(O)H. В результате образуются комплексы хлорида металла с ДМФА, что показано на примере растворения меди. Состав такого комплекса можно изобразить компактно как (CuCl 2) 2(ДМФА) 4(рис. 4.30).
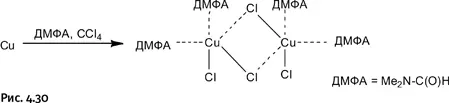
Принцип одновременного действия двух растворителей понятен: CCl 4 – галогенирующий агент, а ДМФА, образуя комплекс, удерживает полученное соединение в растворе.
Благородные металлы тоже не устояли. При действии на золото смеси диметилсульфоксида Me 2S=O и бутилбромида C 4H 9Br образуется AuBr 3. Итак, по существу это новая царская водка (рис. 4.31).
Читать дальшеИнтервал:
Закладка:









