Михаил Левицкий - Карнавал молекул. Химия необычная и забавная
- Название:Карнавал молекул. Химия необычная и забавная
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2019
- Город:Москва
- ISBN:978-5-0013-9101-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Левицкий - Карнавал молекул. Химия необычная и забавная краткое содержание
В книге рассказано о некоторых драматичных, а, порой, забавных поворотах судьбы как самих открытий, так и их авторов. Кроме того, читатель потренируется в решении занятных задач, что особенно приятно, когда рядом помещена подсказка, а потом и сам ответ.
В отличие от учебника в книге нет последовательного изложения основ химии, поэтому ее можно читать, начиная с любой главы.
Карнавал молекул. Химия необычная и забавная - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Само железо весьма мягкий материал, и древние мастера научились насыщать его углеродом для получения твердых сплавов, способных воспринимать закалку. Орудия труда и оружие изготовляли с помощью многократной горячей ковки, придававшей изделию необходимую форму. Позже нашли способы с помощью термической и химической обработки придавать изделиям из железных сплавов декоративный вид (оксидирование, называемое в быту воронением), что одновременно защищало поверхность от коррозии.
Почва – коварная среда
Рассмотрим кратко процессы, происходящие при коррозии металлических предметов. В результате атмосферной коррозии медные сплавыпокрываются тонкой пленкой оксидов: красного оксида меди Cu 2O и черного оксида CuO. Со временем пленка приобретает коричневый цвет, это так называемая естественная патина – темный прозрачный слой, придающий изделиям налет благородной старины, однако такое можно наблюдать при не очень длительном хранении предмета.
В отличие от атмосферной коррозии, при почвенной коррозии (именно с ней приходится иметь дело археологу) дело обстоит намного хуже. На предмете образуются коррозионные слои, наружный состоит из основных карбонатов меди (в зависимости от состава зеленого или синего цвета), покрытых остатками почвы и органических наслоений. Там же часто содержится основной хлорид меди СuCl(OH), а под ним – плотный красно-коричневый оксид меди Cu 2O, содержащий включения черного оксида CuO. Еще глубже расположены чешуйки восстановленной меди, это результат электрохимической коррозии, протекающей в почве.
Между слоем восстановленной меди и оксидным слоем находится самая опасная коррозионная составляющая – хлорид меди CuCl 2, чаще всего это соединение образуется при повышенной влажности от присутствия ионов хлора в засоленных почвах. Хлорид меди при взаимодействии с влагой гидролизуется, переходя в основной хлорид СuCl(OH). При этом образуется хлороводород HCl, который в присутствии кислорода и влаги начинает разрушать не затронутый коррозией слой металлической меди. На поверхности предмета появляются небольшие ярко-зеленые пятна рыхлого гигроскопичного вещества, постепенно очаги разрастаются, разрушение также идет вглубь металла, образуются каверны, поверхность становится изъязвленной. Этот процесс называют «бронзовой болезнью» – термин, используемый реставраторами.
Теперь перейдем к железным сплавам, они заметно менее коррозионностойки в сравнении с медными сплавами. При почвенной коррозии железных сплавов под действием кислорода и влаги образуются оксиды и гидроксиды железа Fe 2O 3·nH 2O желтовато-коричневого цвета, синеватый фосфат железа Fe 3(PO 4) 2·8H 2O, желтовато-серый карбонат FeCO 3.
Для предмета, находящегося в почве, сохраняется определенное равновесие между металлом и окружающей средой, но при извлечении его из археологического слоя это равновесие нарушается: меняется влажность и облегчается доступ кислорода, в результате увеличивается скорость коррозии. Ионы хлора, попавшие в объект из почвенной влаги, реагируя с металлом, образуют хлориды железа, которые, в свою очередь, при гидролизе выделяют хлороводород HCl, который взаимодействует с металлической поверхностью. Место коррозии все время перемещается, затрагивая новые участки сохранившегося металла, что приводит к активному разрушению предмета. Таким образом, реставрацию извлеченного предмета нельзя отложить на неопределенное время, необходимо как можно раньше приступить к обработке.
Не только восстановить, но и уберечь
Состав металла в археологических предметах в настоящее время подробно изучен с помощью микроскопического исследования участков протравленной поверхности, а также с использованием современных спектральных методов, которые позволяют провести анализ без взятия пробы. Эти сведения помогают провести более точную датировку таких предметов, кроме того, по содержанию примесных металлов можно определить состав использовавшихся в то время рудных месторождений. Широко известный радиоуглеродный метод, используемый для датировки остатков органического происхождения, в этом случае малоприменим, так как он «работает» только при наличии атомов углерода, и иногда он может быть полезен при определении возраста органических наслоений.
Если вопросы, касающиеся состава археологических предметов, в настоящее время успешно решают с помощью современных физических методов, то во всем, что относится к процедуре их восстановления после коррозии, протекавшей в течение столетий, еще существует много проблем.
Наука реставрации накопила громадное количество разнообразных приемов, позволяющих вернуть корродированным предметам вид, близкий к первоначальному. В большинстве случаев используют реагенты, широко применяемые для очистки и консервации металлов. Отдельные оригинальные методики удалось создать некоторым талантливым реставраторам, сочетавшим знание химии с искусством экспериментатора. Тем не менее многие из разработанных приемов хотя и позволяют на какое-то время достичь нужного результата, но сохраняют этот эффект ненадолго.
Первый этап работы с археологическим предметом – очистка от загрязнений, представляющих собой жировые наслоения, смешанные с частицами органических веществ и остатками почвы. Далее следует химическая очистка от продуктов коррозии.
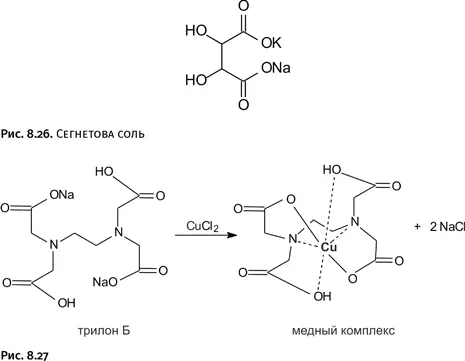
А теперь рассмотрим некоторые устоявшиеся методики. Для очистки медных изделийиспробовали много различных реагентов: щелочной раствор сегнетовой соли NaKC 4H 4O 6•4H 2O (рис. 8.26), фосфат натрия (он входит в состав бытового средства калгон для смягчения воды), сульфамидную кислоту HOS(O) 2NH 2. Все эти средства не удаляют красно-коричневый куприт Cu 2O. Широко используют препарат трилон Б – динатриевую соль этилендиаминтетрауксусной кислоты, при этом ион металла «укрывается» во внутренней полости молекулы, а металлическая поверхность не затрагивается (рис. 8.27).
Этот реагент растворяет практически все нерастворимые в воде продукты коррозии – оксиды, гидроксиды и карбонаты. Однако он заметно ослабляет сам металл, это так называемое «растравливание».
При электрохимических методах очистки существует опасность того, что поверхность покроется тонким слоем свежевосстановленной меди, имеющим яркую красноватую окраску. В результате старинный предмет приобретет вид недавно изготовленной поделки.
Читать дальшеИнтервал:
Закладка:









