Владимир Рюмин - Занимательная химия
- Название:Занимательная химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1936
- Город:Ленинград
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Владимир Рюмин - Занимательная химия краткое содержание
Хотя книга не преследует учебных целей, все же я думаю, что незнакомый с химией вынесет из нее начальные понятия об этой науке; знакомый же найдет в ней указания на то, как использовать свои познания для постановки опытов в более эффектном виде. Настоящая книжка имеет в виду читателей, умеющих соблюдать осторожность в обращении с некоторыми не вполне безопасными веществами. Как следует обращаться с ними, чтобы не повредить себе и другим, указано в особом дополнении в конце настоящей книги; читатель, даже совершенно незнакомый с химическими манипуляциями, найдет там необходимые указания к их выполнению.
Занимательная химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Во второй цилиндр лью одну за другой жидкости разных цветов, подкрашенные растительными и искусственными органическими красками; туда же вливаю немного чернил из чернильницы и, закрыв отверстие цилиндра стеклом, взбалтываю смесь, пока она не обесцветится. Впрочем, с обесцвечивающей способностью хлора мы с вами уже знакомы: мы пользовались ею в опытах-фокусах, с которых начали нашу беседу. Только тогда мы брали не газообразный хлор, а его раствор в воде - хлорную воду. Ее легко приготовить.
Погрузим трубку, отводящую газ из колбы, в сосуд с холодной водой, например, в перевернутую реторту (рис. 20). Желтоватые пузырьки газа исчезают, не дойдя до поверхности воды: газ успевает раньше раствориться.
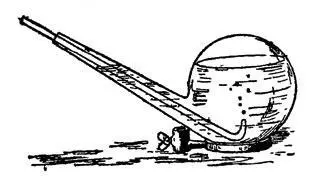
Рис. 20. Получение хлорной воды
Хлорная вода белит не хуже хлора (повторите опыт обесцвечивания цветов и красок); однако, в заводской практике для беления не всегда можно пользоваться газообразным хлором или его водяным раствором. Чаще для беления, а также для дезинфекции хлор берут в виде хлорной извести. В ней он связан химически, но связь эта непрочна, хлор из нее легко выделяется; оттого-то белильная известь и имеет его запах. Хлорную известь можно достать готовой; поэтому для химических фокусов, основанных на обесцвечивании хлором, вам нет надобности самим ее готовить, как мы это делаем сейчас, а можно заменить ее водой, настоенной на белильной извести.
Кстати, ее белящее действие вдвое сильнее, чем у газообразного хлора. Курьез заключается в том, что хлор не сам белит краски, - их обесцвечивает кислород, выделению которого в свободном состоянии способствует хлор. Сам же хлор является сильным разрушителем волокон пряжи и тканей. Оттого-то на предприятиях отбеленные хлором изделия отмываются раствором антихлора, то-есть гипосульфита, как мы уже о том говорили.
Вы заметили, как желтеют листы очень старых газет, какой ломкой становится бумага, на которой они напечатаны?
Это результат отбелки хлором бумажной массы.
Окраска хлором в синий цвет
Хлором можно не только белить, но и красить. При помощи хлора бесцветное можно сделать цветным.
В пробирке, которую я держу в руке, бесцветный жидкий клейстер. Опускаю в пробирку газоотводную трубку от прибора для получения хлора, - газ проходит через раствор, но не поднимается выше его уровня, раствор же, как видите, приобретает красивый фиолетово-синий цвет.
Клейстер был мною сварен из крахмала в растворе йодистого калия. Из этого последнего хлор вытеснил йод [11] Йод - элемент группы хлора, твердое тело; его спиртовой раствор - обычное средство лечения порезов, опухолей и др.
, который с крахмалом дает темно-синее окрашивание.
Попутно замечу, что это очень чувствительная реакция на крахмал, и (в упрощенном виде, когда берется прямо готовый йод) служит она для нахождения крахмала в качестве подмеси к творогу, какао, колбасам и пр.
Не забудьте об этой реакции: она еще послужит нам для одной химической шутки за чайным столом.
Окраска хлором в красный цвет
Многие, даже красильные мастера, вообще не слыхали, что хлором можно красить, но изучавшие химию знают, что он выделяет йод из соединений последнего и что йод окрашивает крахмал в синий цвет. Но даже и они не все знакомы с фактом, что хлором можно красить и в красный цвет.
Как это делается, сейчас покажу.
Беру один из стеклянных цилиндров с хлором и отливаю из него немного газа в другой, пустой (то-есть наполненный воздухом) цилиндр. Прикрываю последний сверху стеклом и несколько раз переворачиваю его вверх и вниз, чтобы хлор хорошенько смешался с воздухом. Обратите внимание, что хлора было взято так мало, что смесь газов осталась бесцветной. Опускаю в цилиндр влажную полоску фильтровальной бумаги и вынимаю ее оттуда окрашенной в розовый цвет. Повторяю опыт, прилив немного больше хлора, - бумажка принимает интенсивно красную окраску.
Бумагу я увлажнял раствором бромистого калия (применяется как лекарство при нервных болезнях), к которому была прибавлена капля щелочного раствора, флуоресцина. Хлор вытесняет из бромистого калия бром [12] Бром - элемент группы хлора, красно-бурая, дурно-пахнущая жидкость. Вся эта группа элементов с водородом дает кислоты, не содержащие кислорода (например, соляная кислота).
, а бром превращает флуоресцин в ярко-красный эозин, органическое вещество, обладающее весьма большой красящей способностью.
Эту его способность мы также используем в свое время для одного забавного химического фокуса.
Описанным путем в военное время можно обнаружить следы хлора в воздухе ранее, чем он дойдет до окопов, и тем предохранить воюющих от опасности отравления, дав им время надеть предохранительные маски.
Еще окраска хлором
Беру пробирку и, налив ее до половины водой, растворяю в ней кристаллик зеленого хлористого железа. Слабо-зеленоватое окрашивание раствора почти совсем незаметно. Погружаю в пробирку газоотводную трубку от аппарата для добычи хлора и пропускаю некоторое время газ через раствор. Жидкость принимает красно-желтоватый цвет: хлористое железо превратилось в хлорное.
Эта реакция противоположна действию водорода на хлорное железо. Хотя в данном случае кислород в реакции не участвовал, она все же относится к реакциям окисления.
Говоря о восстановлении железной соли водородом, я сказал, что она поможет нам выяснить одну из тайн строения веществ.
Постараюсь выполнить обещанное.
Железо дает с кислородом два окисла: закись - с меньшим содержанием кислорода и окись - с большим. Присоединение к закиси кислорода будет ее окислением, отнятие его от окиси - восстановлением. С хлором железо дает тоже два соединения, соответствующие закиси и окиси. Перевод одного и другого по аналогии также называется окислением и восстановлением.
Тайной же химического строения веществ является то обстоятельство, что элементы соединяются друг с другом в строго определенных весовых отношениях, и когда один из них присоединяется к другому в различных количествах, то эти количества находятся в простых кратных отношениях одно к другому. Так, в воде на одну весовую часть водорода приходится 8 весовых частей кислорода, а в перекиси водорода - 8X2, то-есть 16.
Пока довольно. Мы ведь решили больше развлекаться занимательными химическими опытами, а выводы из них делать лишь попутно и в небольших "порциях".
Горение без воздуха
Что такое горение? В элементарных учебниках говорится, что "горение есть энергичное соединение вещества с кислородом воздуха, сопровождаемое выделением тепла и пламени".
Читать дальшеИнтервал:
Закладка:










