Айзек Азимов - Энергия жизни. От искры до фотосинтеза
- Название:Энергия жизни. От искры до фотосинтеза
- Автор:
- Жанр:
- Издательство:Центрполиграф
- Год:2007
- Город:М.
- ISBN:978-5-9524-2590-3
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Айзек Азимов - Энергия жизни. От искры до фотосинтеза краткое содержание
В этой книге Азимов рассказывает о том, как люди научились использовать энергию — сумели заставить работать на себя огонь, воду, ветер, пар, электричество и солнце. Большое внимание уделено изобретениям, открывшим новые источники энергии, распахнувшие перед человечеством двери новой эпохи. Автор также увлекательно повествует о том, как вырабатывается энергия в живых организмах, какие процессы происходят на уровне молекул в органической и неорганической материи.
Энергия жизни. От искры до фотосинтеза - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
В 1925 году британский биохимик Д. Кейлин занимался изучением того, как размешанные в растворе взвеси истолченных тканей различных видов — от бактериальных до нервных тканей высших животных — поглощают свет. Он обнаружил около полудюжины разных полос поглощения и приписал их наличие предположительному существованию вещества, которое назвал «цитохром» (от греческих слов, означающих «клетка» и «цвет»). Дальнейшие исследования показали, что полосы поглощения существуют попарно, и каждая пара полос поглощения привязана к своему веществу. Естественно, они получили названия «цитохром a», «цитохром b» и «цитохром с». Со временем выяснилось, что даже такое деление не совсем точно, было вещество близкое к цитохрому a, но все же не полностью с ним идентичное, и оно получило название «цитохром a 3».
Единственным цитохромом, который удалось достаточно легко выделить из взвеси тканей, оказался цитохром с. Обнаружилось, что это сравнительно простой белок, молекулярный вес его — около 13 000, и каждая молекула этого вещества содержит один атом железа. Этот атом является частью гема, такого же гема, какой входит и в состав гемоглобина (см. главу 18). Дальнейшие исследования показали, что и в других цитохромах тоже содержится железо — и в каждом случае оно входило в состав либо гема, либо очень похожей на гем группы атомов.
Соответственно, цитохромы получили видовое название «гемоферменты». Каталаза, как я уже упоминал в предыдущей главе, тоже является примером гемофермента, но она не выполняет функций цитохромов. Гемоглобин — это гемосодержащий белок, но не гемофермент. Не все ферменты, в составе которых имеется железо, — гемоферменты. К примеру, в состав дегидрогеназы янтарной кислоты тоже входит атом железа, но не как часть гемовой группы.
Когда была установлена схема передачи водорода («дыхательная цепочка»), вскоре стало ясно, что цитохромы должны быть в нее где-то включены. Они присутствуют практически во всех клетках, за исключением разве что клеток некоторых «обязательно анаэробных» бактерий — то есть таких, которые могут жить только при отсутствии кислорода. Факт того, что в их клетках цитохромы отсутствуют в сочетании с тем, что эти бактерии не могут использовать кислород, сам по себе уже свидетельствует в пользу важности роли цитохромов в дыхательных цепочках.
И опять же, любое вещество, препятствующее деятельности цитохромов — а особенно колебаниям атома железа между двух- и трехвалентным состоянием, что прекращает передачу электрона, — препятствует и поглощению кислорода. Воздействие цианидных групп (—С=N) таких веществ, как синильная кислота (HCN) или цианистый калий (KCN), приводит к прочному застыванию атома железа в одном из состояний, в результате чего дыхание быстро и навсегда прекращается (именно поэтому цианиды так ядовиты).
О положении цитохромов в цепочке можно судить по окислительным потенциалам, приведенным в таблице 9. Очевидно, цитохромы стоят где-то после флавинов, принимают электроны от атомов водорода и передают их по одному путем колебания железа между двух- и трехвалентным ионным состоянием, от «b» к «c», от «c» к «a», от «a» к «a 3».
Возможно, при этом передаются и сами атомы водорода, хотя в этом отношении точных данных нет.
Однако где-то ведь цепочка должна закончиться! На каком-то этапе водород должен быть передан кислороду — и это этап цитохрома a 3. Окислительный потенциал системы «кислород/вода» равен +0,80, и он в конце концов берет свое. Поскольку цитохром a 3может использовать кислород в качестве получателя водорода, в результате чего образуется вода, а не перекись водорода (получается, вот он, фермент, катализирующий разрыв связи О—О!), то его можно назвать «оксидазой». На самом деле именно под этим названием цитохром a 3и известен по большей части — «цитохромоксидаза».
Все, получили воду, можно теперь расслабиться. Теперь дыхательная цепочка собрана до конца.
Опять возникает вопрос: почему же она оказывается такой длинной? Почему же требуется так много коферментов и простетических групп, чтобы перенести атомы водорода от субстрата к ферменту?
ДПН/ДПН∙2Н … - 0,32
ФАД/ФАД- 2Н … - 0,22
b(Fe 3+)/b(Fe 2+)* … - 0,05
c(Fe 3+)/c(Fe 2+)* … + 0,25
a(Fe 3+)/aFe 2+)* … + 0,29
a 3(Fe 3+)/a 3(Fe 2+* … + 0,30
* цитохромы
Как я уже говорил, при дегидрогенизации вещества уровень свободной энергии снижается на 35—70 килокалорий на моль вещества, но организм не может использовать высвобождающуюся энергию, если только не запасет ее в виде высокоэнергетических фосфатных связей. Насколько известно, в ходе одной реакции может образоваться только одна высокоэнергетическая связь. Поскольку запасти таким образом можно только 8 килокалорий на моль вещества, то перевод одной реакции дегидрогенизации в одну реакцию образования высокоэнергетической фосфатной связи означал бы потерю семи восьмых энергии.
Наличие длинной дыхательной цепочки позволяет живой ткани разбить процесс уменьшения свободной энергии на фрагменты, на каждом из которых можно создавать по одной высокоэнергетической фосфатной связи. В начале 50-х годов XX века достаточно убедительно было показано, что таким образом в среднем на основе одной реакции дегидрогенизации удается создать по три высокоэнергетических фосфатных связи. Таким образом, эффективность использования энергии достигает хотя бы 35 процентов.
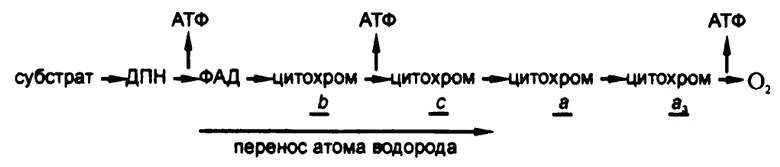
Естественно, возникает вопрос, а где же именно, на каком участке дыхательной цепочки формируются высокоэнергетические фосфатные связи. Для ответа на этот вопрос попытаемся действовать методом исключения.
Система с участием дегидрогеназы молочной кислоты производит три высокоэнергетические фосфатные связи на каждую потребляемую молекулу молочной кислоты. Однако система с участием дегидрогеназы янтарной кислоты произведет лишь две высокоэнергетические фосфатные связи на каждую потребляемую молекулу янтарной кислоты. Дегид-рогеназа янтарной кислоты — флавофермент, так что при дегидрогенизации янтарной кислоты из процесса выпадает этап пиридин-фермента. Поскольку этому выпадению соответствует потеря одной реакции образования высокоэнергетической фосфатной связи, то остается сделать вывод, что одна такая связь образуется именно при переходе от ДПН к ФАД.
Путем добавления в дыхательную систему различных химических веществ можно исключать из цепочки те или иные звенья и отмечать, сократится ли при этом количество образуемых высокоэнергетических фосфатных связей. Итоговые предположения об участках образования этих связей приведены на рис. 63.
Читать дальшеИнтервал:
Закладка:










