Андрей Несмеянов - Радиоактивные изотопы и их применение
- Название:Радиоактивные изотопы и их применение
- Автор:
- Жанр:
- Издательство:Военное Издательство Министерства обороны Союза ССР
- Год:1958
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Андрей Несмеянов - Радиоактивные изотопы и их применение краткое содержание
Широта научных проблем, изучаемых с помощью изотопов, неизмерима: здесь исследования целительных свойств лекарств и открытие загадки древних статуй, анализ глубоководных морских отложений и раскрытие тайны происхождения живого и неживого, обмен веществ в микроскопической клетке и величественные проблемы происхождения вселенной.
При помощи радиоактивных изотопов могут быть вскрыты интимнейшие механизмы биохимических процессов в растениях и животных. Излучение радиоактивного распада оказывается в руках исследователей одним из сильнейших рычагов искусственной переделки наследственной природы организмов. Используя эти средства, наука вплотную подошла к решению самых глубоких проблем биологии, связанных с объяснением важнейших физиологических процессов.
Даже такая, казалось бы далекая от атомной физики отрасль, как агрономия, уже не может обойтись без применения различных средств атомной техники.
Радиоактивные изотопы — это важный инструмент современной науки, умножающий человеческую власть над природой. subtitle
6 0
/i/55/718755/Grinya2003.png
0
/i/55/718755/CoolReader.png
Радиоактивные изотопы и их применение - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Менделеев открыл периодический закон в 1869 г. В то время о строении атома еще ничего не было известно, и Менделеев выразил свой закон так: «Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов». При расположении элементов в порядке возрастания их атомных весов в ряд через определенное число повторяются элементы со сходными свойствами. Если этот ряд элементов разделить на несколько строк так, чтобы возрастание атомных весов шло слева направо и сходные элементы оказались друг под другом в одном вертикальном столбце, то получится периодическая система элементов. Эту работу и выполнил в 1869 г. Д. И. Менделеев, выразив открытый им закон в виде таблицы.
Можно подумать, что Менделееву нетрудно было сделать это открытие, так как закон очень прост. На самом деле задача была чрезвычайно сложной. Лишь две трети элементов, имеющихся на Земле, были известны во времена Менделеева, и распределение их в порядке возрастания атомных весов не давало правильной повторяемости свойств. Но Менделеев, глубоко убежденный в справедливости найденного им закона, сумел правильно расположить все известные элементы, оставив свободными те клетки таблицы, которые должны были занять еще не найденные элементы.
Придавая основное значение периодической повторяемости химических свойств элементов, Менделеев в ряде случаев расположил элементы не в порядке возрастания атомных весов.
Используя периодический закон, Менделеев предсказал свойства еще не открытых элементов.
Все свободные клетки периодической системы впоследствии были заполнены новыми элементами, и предсказания русского ученого подтвердились.
Периодическая таблица Менделеева помогла многим великим открытиям XX века. Эти открытия показали важное значение закона, найденного великим ученым. Так, например, порядковый номер элемента в таблице оказался не просто очередным номером, он получил глубокий физический смысл.
3. Мир атомовРазмеры атомов и молекул и их веса ничтожно малы. Если их выражать в обычных единицах измерения — граммах и сантиметрах, то получатся цифры, совершенно неудобные для обращения. Так, вес атома кислорода равен 0,000 000 000 000 000 000 000 026 грамма.
Самый легкий атом — атом водорода — весит в 16 раз меньше атома кислорода, а атом калифорния, одного из самых тяжелых известных в настоящее время элементов, — всего в 15 раз тяжелее атома кислорода.
В состав молекул входит относительно небольшое количество атомов, поэтому и веса молекул выражаются такими же маленькими числами, как и веса атомов. Даже гигантские молекулы некоторых белковых веществ, которые в 1000 раз тяжелее атома кислорода, имеют очень маленький вес. Поэтому в самых небольших количествах вещества содержится грандиозное количество молекул и атомов. Например, в грамме железа содержится около 10 000 000 000 000 000 000 000 атомов. Но грамм железа — это кубик с ребром длиною всего в ½ сантиметра.
Нетрудно найти, что на линии длиной, равной одному сантиметру, вплотную друг к другу разместится около 100 миллионов атомов железа.
Чтобы еще лучше представить себе грандиозность числа атомов в самых небольших количествах вещества, рассмотрим такой пример. Если из трубы дома или завода, находящегося в Москве, вылетит 1 грамм сажи и равномерно распределится на всей площади, занимаемой городом, то на каждом квадратном сантиметре окажется по 500 миллиардов атомов углерода, из которого состоит сажа.
Обычно на практике пользуются системой так называемых атомных и молекулярных весов. По этой системе вес атома любого элемента выражается через вес атома кислорода, условно принятый равным 16 атомным единицам массы. Вес самого легкого атома — атома водорода — по этой системе весов приблизительно равен единице, а самого тяжелого природного элемента — урана — примерно 238. Молекула воды по этой системе имеет так называемый молекулярный вес, равный 18.
4. Открытие радиоактивностиВ конце прошлого столетия французский физик А. Беккерель обнаружил, что вещества, в состав которых входит уран, испускают какие-то лучи. Эти лучи, так же как и солнечные, действуют на фотографическую пластинку, вызывая засвечивание светочувствительного слоя. Но в отличие от солнечных новые лучи подобно лучам Рентгена оказывают свое действие на пластинку и в том случае, когда она завернута в черную бумагу.
Изучением лучей, открытых Беккерелем, занялись многие ученые. Особенно плодотворными были работы Марии Склодовской-Кюри и ее мужа Пьера Кюри. Они нашли, что лучи Беккереля испускаются только теми веществами, которые содержат уран или торий. Для обнаружения этих лучей Пьер Кюри построил специальный прибор, основанный на том, что под действием лучей Беккереля воздух становится проводником электрического тока. Прибор работает по схеме, показанной на рис. 1. Металлическая пластинка 1 присоединяется к отрицательному полюсу электрической батареи, а пластинка 2 — к положительному. Если излучение радиоактивного вещества проходит между пластинками 1 и 2 , то воздух делается проводником электрического тока, вся цепь оказывается замкнутой, и стрелка гальванометра 3 отклоняется. Чем интенсивнее излучение, тем больше отклоняется стрелка.
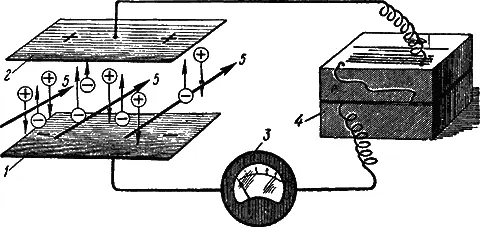
Мария Кюри установила, что интенсивность излучения была тем больше, чем больше урана находилось в веществе. Вскоре, однако, выяснилось, что урановая руда, так называемая урановая смолка, давала излучение в несколько раз более интенсивное, чем чистый металл уран, несмотря на то, что в урановой смолке содержалось лишь несколько процентов урана. Это явление говорило о том, что в урановой смолке есть какое-то вещество, способное к более сильному излучению, чем сам уран.
Поисками этого неизвестного вещества и занялись Мария и Пьер Кюри. В результате двухлетней работы им удалось обнаружить в урановой руде два новых вида атомов, т. е. два новых элемента — радий и полоний. Полоний получил свое имя в честь Польши — родины Марии Кюри, — а радий — за его излучение («радиус» в переводе с латинского — луч). Само излучение было названо радиоактивным, а элементы, способные к такого рода излучению, — радиоактивными. Радиоактивными элементами оказались уран, торий, радий и полоний.
5. РадийРадий испускает лучи, подобные урану, но излучение радия более интенсивное. Радий непрерывно выделяет тепло.
Читать дальшеИнтервал:
Закладка:










