Андрей Несмеянов - Радиоактивные изотопы и их применение
- Название:Радиоактивные изотопы и их применение
- Автор:
- Жанр:
- Издательство:Военное Издательство Министерства обороны Союза ССР
- Год:1958
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Андрей Несмеянов - Радиоактивные изотопы и их применение краткое содержание
Широта научных проблем, изучаемых с помощью изотопов, неизмерима: здесь исследования целительных свойств лекарств и открытие загадки древних статуй, анализ глубоководных морских отложений и раскрытие тайны происхождения живого и неживого, обмен веществ в микроскопической клетке и величественные проблемы происхождения вселенной.
При помощи радиоактивных изотопов могут быть вскрыты интимнейшие механизмы биохимических процессов в растениях и животных. Излучение радиоактивного распада оказывается в руках исследователей одним из сильнейших рычагов искусственной переделки наследственной природы организмов. Используя эти средства, наука вплотную подошла к решению самых глубоких проблем биологии, связанных с объяснением важнейших физиологических процессов.
Даже такая, казалось бы далекая от атомной физики отрасль, как агрономия, уже не может обойтись без применения различных средств атомной техники.
Радиоактивные изотопы — это важный инструмент современной науки, умножающий человеческую власть над природой. subtitle
6 0
/i/55/718755/Grinya2003.png
0
/i/55/718755/CoolReader.png
Радиоактивные изотопы и их применение - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Лучи от кусочка радия идут прямолинейно во все стороны. Они плохо проникают через свинец, и если радий находится на дне свинцовой коробки, в которой сделано узкое отверстие, то лучи распространяются из этого отверстия узким пучком. Если на пути пучка поставить фотографическую пластинку, то после проявления на ней получится одно маленькое пятно (рис. 2, а ). Если же лучи радия проходят сквозь электромагнитное поле, то они делятся на три составные части. Это легко обнаружить с помощью фотопластинки. Вместо одного пятна на ней после проявления появляются три: одно в центре, другое рядом с ним, а третье с другой стороны от центра (рис. 2, б ).
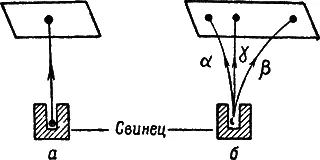
Три рода лучей радия были названы альфа- бета- и гамма-лучами (альфа-, бета- и гамма — названия трех первых букв греческого алфавита).
Как было установлено опытами с отклонением излучения радия в электромагнитном поле, альфа-лучи представляют собой поток положительно заряженных частиц, бета-лучи — поток отрицательно заряженных частиц, а гамма-лучи не несут никакого электрического заряда.
6. Строение атомаИсследование свойств радия и ряд других опытов привели ученых к заключению, что атомы являются сложными частицами, в состав их входят положительно заряженные частицы и электроны [2] Электроны — это составные части каждого атома, несущие отрицательный электрический заряд. Электрон приблизительно в 1850 раз легче атома водорода. Он представляет собою наименьшее (известное на сегодня) количество электричества — «атом электричества».
. Как же расположены они в атоме?
Оказывается, в центре атома находится положительно заряженное ядро очень малых размеров. Ядро окружено электронами. Так как атом в целом электрически нейтрален, то число окружающих его электронов равно заряду ядра.
Расстояния от ядра до электронов значительно больше размеров самого ядра. Если представить себе ядро увеличенным до размеров горошины, то электроны как бы окажутся на расстоянии 100 метров от ее центра.
Диаметр ядра атома имеет размер порядка 0,0001 ангстрема, а сам атом — от одного до пяти ангстремов [3] Ангстрем — единица длины, употребляемая для измерения размеров атомов и молекул, она равна одной стомиллионной доле сантиметра.
.
Электроны составляют лишь незначительную часть массы атома. Почти вся масса атома сосредоточена в ядре. Если бы мы смогли наполнить один кубический сантиметр ядрами какого-либо атома, то он весил бы приблизительно столько же, сколько величайшая гора Кавказа Эльбрус (около 100 000 000 тонн).
Атомы различных элементов отличаются друг от друга весом и зарядом ядра.
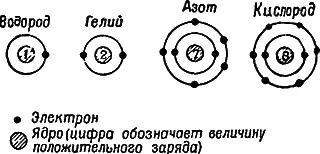
На рис. 3 показаны упрощенные схемы строения некоторых атомов. Электроны в атомах располагаются слоями. В результате, например, химической реакции атом может передать электроны из внешнего слоя другому атому. При этом электрическая нейтральность атомов нарушается. Такие заряженные частицы называются ионами. Атомы, потерявшие один или несколько электронов, становятся положительными ионами, а принявшие один или несколько электронов — отрицательными.
После открытия нейтронов советский физик Д. Д. Иваненко в 1932 г. сделал предположение, что ядро атома состоит из частиц двух видов — протонов и нейтронов. Предположение Иваненко было развито и обосновано Гейзенбергом и подтверждено всеми опытами, проведенными в дальнейшем с атомными ядрами. В настоящее время протонно-нейтронная теория является общепризнанной.
Протоны — это ядра атомов водорода; масса протона равна приблизительно одной атомной единице, и протон имеет положительный заряд. В качестве единицы заряда в атомной физике принята абсолютная величина заряда электрона. Заряд протона по абсолютной величине равен заряду электрона. Следовательно, можно сказать, что заряд протона равен единице.
Нейтроны имеют примерно такую же, как и протоны, массу, но не несут электрического заряда. Это электрически нейтральные частицы.
Протонно-нейтронная теория строения атома лежит в основе современной ядерной физики.
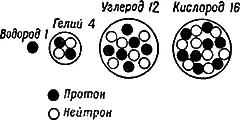
Так как веса протона и нейтрона в атомных единицах приблизительно равны единице, то округленный до целого числа вес атома в атомных единицах равен сумме числа нейтронов и протонов всего ядра. Это число называется массовым числом. Число же протонов в ядре равно порядковому номеру элемента в периодической системе. Таким образом, ядро атома углерода, имеющего массовое число 12 и заряд, равный 6 единицам, содержит 6 протонов и 6 нейтронов (рис. 4). Ядро атома урана с массовым числом 238 и зарядом 92 содержит 92 протона и 146 нейтронов.
Открытие Марией и Пьером Кюри полония и радия направило ученых на поиски других радиоактивных элементов. Эти поиски увенчались успехом: в рудах урана и тория были открыты новые радиоактивные элементы.
Многие из них по своим химическим свойствам оказались неотличимыми от ранее известных элементов. Так, в 1906 г. был обнаружен элемент ионий, который оказался сходным по свойствам с ранее известным элементом Ⅳ группы периодической системы торием. Все попытки отделить ионий от тория кончались неудачей.
В 1907 году было установлено, что вновь открытый элемент мезоторий химически неотличим от радия.
В последующие годы было обнаружено полное химическое сходство новых элементов радия В и радия D со свинцом. Атомы радия В и радия D имеют такой же заряд ядра, а значит, и такой же порядковый номер, как и атомы свинца, но отличаются от них своей массой. Такое же равенство зарядов и отличие в массах имело место у тория и иония, мезотория и радия.
Оказалось, что в некоторых клетках периодической системы Менделеева должно помещаться несколько видов атомов, имеющих одинаковый заряд ядра, но разную массу. Такие атомы получили название изотопов (изотоп по-гречески означает — занимающий то же место). Радий В и радий D стали называться изотопами свинца, мезоторий 1 — изотопом радия и т. д.
Читать дальшеИнтервал:
Закладка:










