Александр Китайгородский - Физика для всех. Движение. Теплота
- Название:Физика для всех. Движение. Теплота
- Автор:
- Жанр:
- Издательство:Наука
- Год:1974
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Александр Китайгородский - Физика для всех. Движение. Теплота краткое содержание
Авторы этой книги – лауреат Ленинской и Нобелевской премий академик Л.Д. Ландау и профессор А.И. Китайгородский – в доступной форме излагают начала общего курса физики.
Примечательно, что вопросы атомного строения вещества, теория лунных приливов, теория ударных волн, теория жидкого гелия и другие подобные вопросы изложены вместе с классическими разделами механики и теплоты. Подобная тесная связь актуальных проблем физики с ее классическими понятиями, их взаимная обусловленность и неизбежные противоречия, выводящие за рамки классических понятий, – все это составляет сущность современного подхода к изучению физики.
Новое, свежее изложение делает книгу полезной для самого широкого круга читателей.
Физика для всех. Движение. Теплота - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
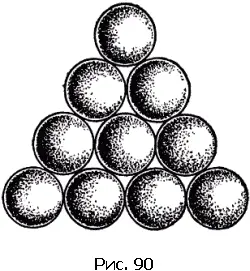
В описанных трех решетках кристаллизуется множество элементов:
Гексагональная плотнейшая упаковка..... Be, Co, Hf, Ti, Zn, Zr
Кубическая гранецентрированная........ Al, Cu, Co, Fe, Au, Ge, Ni, Ti
Кубическая объемноцентрированная ...... Cr, Fe, Li, Mo, Ta, Ti, U, V
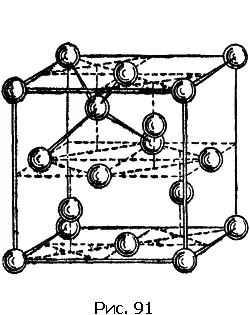
Из других структур упомянем лишь немногие. На рис. 91 изображена структура алмаза. Для этой структуры характерно то, что атом углерода алмаза имеет четыре ближайших соседа. Сопоставим это число с соответствующими числами описанных только что трех наиболее распространенных структур. Как видно из рисунков, в плотнейшей гексагональной упаковке у каждого атома 12 ближайших соседей, столько же соседей у атомов, образующих гранецентрированную кубическую решетку; в объемноцентрированной решетке у каждого атома 8 соседей.
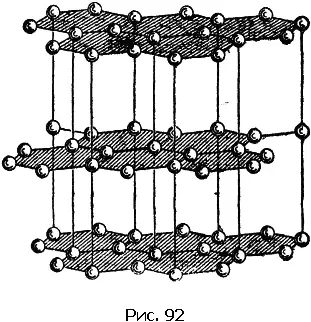
Несколько слов скажем о графите, строение которого показано на рис. 92. Особенность этой структуры бросается в глаза. Графит состоит из слоев атомов, причем атомы одного слоя связаны между собой сильнее, чем атомы соседних слоев. Это связано с величиной межатомных расстояний: расстояние между соседями в одном слое в 2,5 раза меньше кратчайшего расстояния между слоями. Наличие слабо связанных атомных слоев приводит к тому, что кристаллы графита легко расщепляются вдоль этих слоев. Поэтому твердый графит может служить смазочным материалом в тех случаях, когда невозможно применять смазочные масла, – например, при очень низких или очень высоких температурах. Графит – твердый смазочный материал.
Трение между двумя телами сводится, грубо говоря, к тому, что микроскопические выступы одного тела западают во впадины другого. Усилие, достаточное для того, чтобы расщепить микроскопический графитовый кристаллик, много меньше сил трения, поэтому наличие графитовой смазки значительно облегчает скольжение одного тела по другому.
Бесконечно разнообразны структуры кристаллов химических соединений. Крайними – в смысле различий – примерами могут служить структуры каменной соли и двуокиси углерода, изображенные на рис. 93 и 94.
Кристаллы каменной соли (рис. 93) состоят из чередующихся вдоль осей куба атомов натрия (маленькие темные шары) и хлора (большие светлые шары).
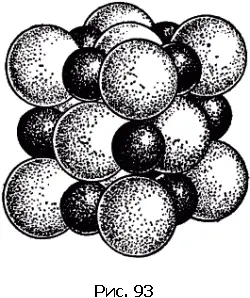
Каждый атом натрия имеет шесть равноотстоящих соседей другого сорта. То же относится и к хлору. Но где же молекула хлористого натрия? Ее нет; в кристалле отсутствует не только группа из одного атома натрия и одного атома хлора, но и вообще какая бы то ни была группа атомов не выделяется своим сближением среди других. Химическая формула NaCl не дает нам оснований говорить, что «вещество построено из молекул NaCl». Химическая формула указывает лишь, что вещество построено из одинакового числа атомов натрия и хлора.
Вопрос о существовании молекул у вещества решается структурой. Если в ней не выделяется группа близких атомов, то молекул нет. Кристаллы без молекул называются атомными.
Кристалл углекислого газа СO 2(сухого льда, который лежит в ящиках у продавщиц мороженого) – пример молекулярного кристалла (рис. 94).
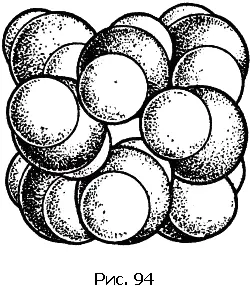
Центры атомов кислорода и углерода молекулы СO 2расположены вдоль прямой линии. Расстояние С–О равно 1,3 Å. А расстояние между атомами кислорода соседних молекул – около 3 Å. Ясно, что при таких условиях мы сразу же «узнаем» молекулу в кристалле.
Молекулярные кристаллы представляют собой плотные упаковки молекул. Чтобы это видеть, надо обрисовать контуры молекулы. Это и сделано на рис. 94.
XI. Температура

Термометр
Если привести в соприкосновение два тела, нагретых по-разному, то более нагретое будет охлаждаться, а холодное станет теплее. Про такие два тела говорят, что они обмениваются теплом; конечно, в жизни мы не называем обменом случай, когда один человек дает другому сто рублей, а другой берет их, но такая терминология принята в физике.
Как уже говорилось, теплообмен – это вид перехода энергии; мы называем более горячим то тело, которое отдает энергию. Мы ощущаем тело горячим, если оно нагревает руку, т.е. передает ей энергию. Наоборот, если тело ощущается холодным, то это значит, оно отнимает энергию у нашего тела.
Про тело, которое отдает тепло (т.е. путем теплообмена отдает энергию), мы говорим: его температура выше температуры того тела, которое забирает это тепло.
Наблюдая за тем, охлаждается или нагревается интересующий нас предмет в присутствии того или иного тела, мы найдем для этого предмета «свое место» в ряду нагретых тел. Температура – это своего рода метка, указывающая, для каких тел интересующий нас предмет будет дарителем, а для каких – получателем тепла.
Температуру измеряют термометрами.
В основу устройства термометров можно положить использование различных свойств тел, чувствительных к температуре. Чаще всего пользуются свойством тел расширяться при повышении температуры.
Если при соприкосновении с разными телами тело термометра будет изменять свой объем, это значит, что тела имеют разную температуру. Когда объем тела термометра больше – температура выше, а когда объем меньше – температура ниже.
Самые различные тела могут служить термометрами: и жидкие, как ртуть или спирт, и твердые – металлы, и газообразные. Но ведь разные тела расширяются по-разному, и ртутные, спиртовые, газовые и прочие градусы совпадать не будут. Конечно, всегда можно отметить на всех термометрах две основные точки – температуры таяния льда и кипения воды. Поэтому 0 и 100 градусов Цельсия все термометры всегда покажут одинаково. Но между 0 и 100 градусами тела будут расширяться не одинаково. Одно тело быстро расширяется между 0 и 50 градусами ртутного термометра и медленно на второй части этого интервала, а другое – наоборот.
Изготовив термометры с разными расширяющимися телами, мы обнаружим заметные расхождения в их показаниях, несмотря на то, что в основных точках показания будут совпадать. Более того, водяной термометр привел бы нас к такому открытию: если охлажденное до нуля тело положить на электроплитку, то его «водяная температура» сначала бы падала, а потом росла. Это происходит по той причине, что вода при нагревании сначала уменьшает свой объем и лишь потом ведет себя «нормально», т.е. увеличивает объем при нагревании.
Читать дальшеИнтервал:
Закладка:







