Enrique Alvarez - Масса атомов. Дальтон. Атомная теория
- Название:Масса атомов. Дальтон. Атомная теория
- Автор:
- Жанр:
- Издательство:Де Агостини
- Год:2014
- Город:М.
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Enrique Alvarez - Масса атомов. Дальтон. Атомная теория краткое содержание
Джон Дальтон является основоположником атомной теории и одним из создателей современной химии. Преподаватель скромной начальной школы Манчестера обратился к идеям, сформулированным за тысячу лет до него Демокритом и другими греческими философами, и предположил, что весь мир состоит из неделимых атомов и в результате их взаимодействия появляются элементы, которые, в свою очередь, образуют химические соединения. Несмотря на то что существование атомов вызывало серьезные споры вплоть до начала XX века — то есть и через 100 лет после публикации труда Дальтона, — именно работа этого просветителя, не получившего университетского образования, легла в основу концептуальной революции, изменившей лицо науки.
Масса атомов. Дальтон. Атомная теория - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Видимо, сэр Гемфри Дэви помог подготовить то выступление 1803 года в Lit & Phil, на котором Дальтон изложил свою атомную теорию. Отношения между двумя учеными сохранились на всю жизнь, и не случайно Дальтон вторую часть своего труда посвятил не только своему другу Уильяму Генри, но и эксцентричному Дэви.
Главным противником Дальтона был Клод Луи Бертолле (1748-1822), для которого новые выкладки и теории о газовых смесях были не больше чем "игрой воображения". Как мы увидим в следующей главе, французский ученый в соответствии с идеями Ньютона разработал теорию химического сродства. Также он был наставником и учителем Луи-Жозефа Гей-Люссака. Несомненно, заслугой Бертолле является определение главного слабого места атомной теории, так что несправедливо говорить о нем как о противнике Дальтона. Более того, когда Дальтон приехал во Францию, чтобы познакомиться с главными учеными страны — Бертолле и Гей-Люссаком, его приняли со всеми почестями.
Труд "Новая система химической философии" был опубликован в двух томах, первый состоял из двух частей. Первая часть первого тома появилась в 1808 году. Джон Дальтон посвятил работу профессорам и сотрудникам шотландских университетов Эдинбурга и Глазго, которые всегда оказывали ему теплый прием и вдохновляли его в научных изысканиях. В посвящении также упоминались члены Lit & Phil, поддерживавшие исследования Дальтона.
Первая часть, в свою очередь, делится на три главы. Первая посвящена теплу, вторая — строению тел, третья — химическому синтезу. Текст сопровождают четыре таблицы в конце книги. Самой известной является четвертая таблица, в которой Джон Дальтон привел произвольные обозначения выделенных им элементов. На первом месте 20 простых элементов, и здесь допущена лишь одна ошибка: окись кальция (известь, или негашеная известь, по-английски lime), формула которой — СаО. Она занимает восьмое место, и ее атомная масса равна 24.

Четвертая таблица, опубликованная впервой части первого тома "Новой системы химической философии" Дальтона, в которой он указывает атомную массу и произвольные обозначения выделенных им элементов.
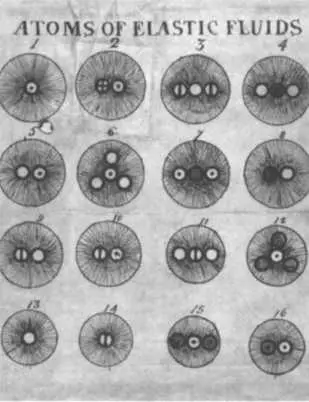
Седьмая таблица второй части первого тома, на которой изображен вид в профиль соединений упругих флюидов.

Бронзовая статуя Дальтона на улице Честер в Манчестере.
| номер | элемент | масса | номер | элемент | масса |
| 1 | водород | 1 | 11 | стронций | 46 |
| 2 | азот | 5 | 12 | барий | 68 |
| 3 | углерод | 5, 4 | 13 | железо | 38 |
| 4 | кислород | 7 | 14 | цинк | 56 |
| 5 | фосфор | 9 | 15 | медь | 56 |
| 6 | сера | 13 | 16 | свинец | 95 |
| 7 | магний | 20 | 17 | серебро | 100 |
| 8 | известь | 24 | 18 | платина | 100 |
| 9 | натрий | 28 | 19 | золото | 140 |
| 10 | калий | 42 | 20 | ртуть | 167 |
В той же таблице Дальтон выделил пять двойных соединений (номера 21-25): вода, аммиак, азотная кислота, этилен, окись углерода; четыре тройных соединения (номера 26-29): закись азота, азотная кислота и углеродный водород (метан); четыре четверных соединения (номера 30-33): кислородноазотная кислота, серная кислота, сероводород и спирт; одно пятерное соединение (азотистая кислота), одно шестерное (уксусная кислота) и два семерных (нитрат аммония и сахар).
Вторая часть первого тома увидела свет в ноябре 1810 года, она была посвящена сэру Гемфри Дэви (профессору химии Королевского института) и Уильяму Генри (в то время вице-президенту Lit & Phil). Дальтон добавил две новые главы: четвертая описывала простые вещества, а пятая — соединения двух элементов по правилу наибольшей простоты. В этой второй части тоже мало таблиц, в основном в ней даны подробные описания собственных опытов автора. В пятой таблице приведены те же обозначения, что и в предыдущей, четвертой, но она исправлена и дополнена. Опыты позволили Дальтону выделить 36 элементов и 24 соединения. Никель, олово, висмут, сурьма, мышьяк, кобальт, марганец, уран, вольфрам, титан, церий, alumina (алюминий?), silex (кремний?), иттрий, бериллий и цирконий собраны в первой группе. В шестой таблице, представляющей собой что-то вроде продолжения пятой, появляются обозначения 27 соединений. Седьмая таблица изображает вид частиц, составляющих упругие флюиды (газы), а также частицы азота и водорода с их тепловой атмосферой. Наконец, в восьмой таблице Дальтон представил атомы 16 упругих флюидов (газов).
В 1827 году ученый опубликовал второй том с описанием своих опытов по расчету атомной массы веществ. Удивительно, насколько точны полученные им результаты, несмотря на очевидную сложность исследований.
ГЛАВА 4
Рождение современной химии
Позабыть об алхимии было нелегко. Причиной тому были извечное стремление человека к богатству и соблазнительная возможность превращения материи. Даже великий Исаак Ньютон попал под чары алхимии. Однако постепенно, начиная с Роберта Бойля и заканчивая Антуаном Лавуазье, шел процесс упорядочивания элементов природы, одного за другим, опыт за опытом, и по мере того как секреты окружающего мира раскрывались, наука погружалась все глубже и глубже — до самого крошечного элемента, атома.
Бил Брайсон не без иронии написал, что если требуется определить момент, когда химия стала серьезной, уважаемой наукой, то нужно вернуться ко дню публикации в 1661 году книги Роберта Бойля "Химик-скептик*. До этого химия была лишь лихорадочной суетой в погоне за химерами. Некоторые даже в XVII веке утверждали, что смесь определенных элементов в определенных пропорциях может сделать человека невидимым. Знаменитый немецкий медик, алхимик, эрудит и искатель приключений Иоганн Бехер (1635-1682) был из числа таких фантазеров. Более того, он мог бы считаться одним из создателей теории флогистона, о которой мы уже упоминали. Бехер говорил, что когда потребляется одно вещество, высвобождается другое — terra pinguis. Эту теорию, согласно которой некая огненная субстанция наполняет все горючие вещества и высвобождается из них при горении, разделял другой немецкий физик, Георг Шталь (1659-1735).
Мы уже объясняли, что теория флогистона, как и другие необоснованные представления, была опровергнута Лавуазье и Ломоносовым. Но алхимия оставалась слишком соблазнительной, чтобы о ней быстро позабыли. В основе научных экспериментов все еще лежали вечные стихии Аристотеля. Прежде чем окончательно исчезнуть в самом необратимом смысле в 1682 году, Бехер вызвался объяснить классическую теорию. Для него земля и вода были основными элементами, в то время как железо и огонь появлялись при реакциях. Он предложил проанализировать основные элементы и классифицировать их согласно свойствам, что было неплохой идеей. Так Бехер выделил три типа земли, из которых главной была "горючая земля" — как он называл серу. В свою очередь, его соотечественник Шталь утверждал, что металлы состоят из извести и флогистона, последний выделяется при горении в виде огня, а в виде остатка мы получаем соль. Эта соль подтверждается ржавчиной, появляющейся на прокаленных металлах, и пеплом — в других случаях. И наоборот, если добавить ржавчину к углю, крайне богатому флогистоном, можно получить металл.
Читать дальшеИнтервал:
Закладка: