С. Егоров - Коллоидная химия. Шпаргалка
- Название:Коллоидная химия. Шпаргалка
- Автор:
- Жанр:
- Издательство:Array Литагент «Научная книга»
- Год:2009
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
С. Егоров - Коллоидная химия. Шпаргалка краткое содержание
Коллоидная химия. Шпаргалка - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
С капиллярной конденсацией связано явление несовпадения изотерм адсорбции и десорбции, иначе это явление называют сорбционным гистерезисом. Суть его заключается в том, что имеет место «запаздывание» десорбции, которая происходит при меньших по сравнению с адсорбцией давлениях. Одной из причин сорбционного гистерезиса при капиллярной конденсации может быть несовпадение формы и кривизны мениска адсорбата в порах при протекании процессов адсорбции и десорбции. Для вычисления кривизны мениска используют уравнение Томсона. Данное уравнение выводится следующим образом. Пусть радиус сферической поверхности раздела фаз равен r, давление насыщенного пара над плоской поверхностью равно p 0 , над выпуклой поверхностью – p . Предположим, что некоторое количество жидкости dm переносится путем с обратимого изотермического испарения при давлении р 0 с плоской поверхности в каплю радиусом r. Затем имеет место обратимая изотермическая конденсация при давлении р . Работа испарения и работа конденсации в этих условиях равны и противоположны по знаку, а общая работа переноса dW , совершаемая над системой, представляет собой работу сжатия пара:
dW 1= [ RT ln ( p 0/ p )] dm / M ,
где М – молярная масса.
Однако при переносе данного количества вещества увеличивается радиус капли на величину dr и ее поверхность на величину ds , следовательно, происходит работа увеличения поверхности:
dW 1= [ RT ln ( p 0/ p )] dm / M = — σds.
Преобразовав данное уравнение получим уравнение Томсона для выпуклой поверхности:
r = — 2σ v / [ RT ln p 0/ p ].
Уравнение Томсона для вогнутой поверхности имеет вид:
r = — 2σv / [ RT ln p / p 0].
Уравнение Томсона находит широкое применение при исследовании пористой структуры сорбентов. Объем адсорбата, заполнившего пространство пор адсорбента при капиллярной конденсации при определенном давлении (при этом имеет место изотермический процесс) считается равным объему пор, имеющих определенный размер (радиус). Кривую распределения объемов пор по радиусам определяют по экспериментального построения десорбционной ветви изотермы адсорбции. Последняя имеет следующий вид:
а = f ( p / p s), v = f ( r ), v = a / ρ , r = 2σ v / RT ln p / p s,
где p – давление пара над вогнутым мениском;
p s – давление насыщенного пара при данной температуре; r – плотность жидкости; a – величина адсорбции.
21. Зависимость растворимости от кривизны поверхности дисперсных частиц (закон Гиббса-Оствальда-Фрейндлиха)
Для выражения зависимости равновесия твердых частиц по отношению к жидкому раствору пользуются уравнением, аналогичным уравнению Томсона. Данная формула выведена В. Оствальдом и Г. Фрейндлихом. Запишем данное уравнение, учитывая, что в растворе мерой интенсивности перехода вещества в другую фазу является концентрация насыщенного раствора:
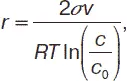
где с 0 – концентрация насыщенного раствора вещества, или его растворимость; с – концентрация вещества в растворе, равновесном с кристалликами размером r.
В отличие от капель, поверхность которых искривлена, поверхность кристаллов представляет собой совокупность плоских граней, однако аналогия данного уравнения объясняется тем, что доля поверхностных молекул, отличных по своим свойствам, несущих избыточную энергию, велика.
Следовательно, при растворении высокодисперсного вещества возможно получение раствора с концентрацией, превышающей его обычную растворимость. Такая система термодинамически неравновесна, что обусловливает перекристаллизацию вещества: появление и рост крупных кристаллов в пересыщенном растворе за счет растворения мелких.
Уравнение Оствальда-Фрейндлихапозволяет рассчитывать поверхностную энергию Гиббса на границе «твердое тело – жидкость», при этом растворимость представлена как функция размеров частиц.
Так, подтверждено, что для сульфата бария растворимость частиц размером r = 2 мкм равна 15,3 ммоль/л, а растворимость частиц с r = 0,3 мкм равна 18,2 ммоль/л. Однако значение поверхностной энергии и в том, и в другом случае будет одинаковым и будет равно 1250 × 10 –3Дж/м 2.
Высокодисперсные частицы отличаются от частиц крупных размеров также тем, что при повышении давления насыщенного пара имеет место некоторое понижение температуры их плавления. Например, уменьшение размера частиц салола до 8 мкм приводит к понижению температуры плавления от +42 до +38°С.
Такие данные позволяют составить представление о возможных значениях поверхностной энергии твердых тел. Особенности условий равновесия на искривленных поверхностях лежат в основе капиллярных явлений.
Форма поверхности раздела фаз способна изменяться под влиянием поверхностного натяжения, стремясь к такой форме, при которой площадь поверхности была минимальна.
При смачивании жидкостью стенок капилляра имеет место образование вогнутого мениска, при этом происходит подъем жидкости в капилляре для компенсации уменьшения давления. Иначе это процесс называют всасыванием. При несмачивании имеет место образование выпуклого мениска, вследствие чего происходит опускание жидкости в капилляре.
С этими явлениями связано возникновение пересыщений при образовании новой фазы.
Вначале происходит образование зародышевых частиц, которые имеют весьма малый размер. Концентрация раствора, равновесная по отношению к таким высокодисперсным агрегатам, заметно выше концентрации насыщенного раствора.
Таким образом, для образования мелких зародышевых частиц необходимо накопление избыточной энергии или создание пересыщенных состояний (пересыщенный пар при конденсации, пересыщенный раствор при кристаллизации), что сильно тормозит образование новой фазы.
22. Смачивание. Закон Юнга (силовой и энергетический выводы)
Смачивание– это поверхностное явление, заключающееся во взаимодействии жидкости с твердым телом при наличии одновременного контакта трех несмешивающихся фаз. Смачивание часто рассматривают как результат межмолекулярного (вандерваальсова) взаимодействия, однако во многих случаях (например, при соприкосновении жидких металлов с твердыми металлами) смачивание обусловлено скорее, образованием химических соединений, твердых и жидких растворов и диффузионными процессами в поверхностном слое смачиваемого тела.
Читать дальшеИнтервал:
Закладка:









