Коллектив авторов - Клинические аспекты спортивной медицины
- Название:Клинические аспекты спортивной медицины
- Автор:
- Жанр:
- Издательство:Array Литагент «СпецЛит»
- Год:2014
- Город:Санкт-Петербург
- ISBN:978-5-299-00594-3
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Коллектив авторов - Клинические аспекты спортивной медицины краткое содержание
Предназначено для специалистов по спортивной медицине, преподавателей и студентов вузов и техникумов медицинской и физкультурной направленности, врачей других медицинских специальностей.
Под редакцией В. А. Маргазина
Клинические аспекты спортивной медицины - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Форма моноцитов на мазках – округлая, под электронным микроскопом обнаруживаются различные цитоплазматические выпячивания. Ядро моноцитов – крупное (занимает до половины площади клетки на мазке), эксцентрично расположенное, бобовидной или подковообразной формы (реже – дольчатое), светлое (хроматин рассеян в виде мелких гранул), с одним или несколькими мелкими ядрышками. Цитоплазма моноцитов – слабобазофильная, содержит многочисленные мелкие митохондрии, короткие цистерны грЭПС, вариабельное число свободных рибосом, полисом, сравнительно крупный комплекс Гольджи. Цитоскелет моноцитов хорошо развит; множественные микрофиламенты, концентрирующиеся в периферических участках его цитоплазмы под плазмолеммой в области формирующихся псевдоподий обеспечивают его активные амебоидные движения. В цитоплазме присутствуют азурофильные гранулы (лизо сомы), сходные с таковыми в нейтрофилах и богатые гидролитическими ферментами.
Антимикробные системы моноцита включают лизоцим, лактоферрин, кислую фосфатазу, арилсульфатазу, катионные белки, миелпероксидазу, перекись водорода и другие биоокислители, а также токсический метаболит – окись азота (NO), которая синтезируется в цитоплазме при их активации.
Цитофизиология моноцитов и их роль в системе мононуклеарных фагоцитов. Моноциты активно выселяются в ткани из сосудистого русла, причем эта миграция усиливается под влиянием продуктов, выделяемых поврежденными тканями, микробами, а также под действием цитокинов. Моноциты обладают высокой активностью фагоцитоза и способны осуществлять иммунный фагоцитоз благодаря взаимодействию их плазмолеммы с опсонизированными микроорганизмами, которое опосредуется рецепторами к IgG и С3-компоненту комплемента. При фагоцитозе в моноцитах, как и в нейтрофилах, генерируются токсические биоокислители (перекись водорода, супероксидный и гидроксильный радикалы, синглетный кислород), а также окись азота. Моноциты, как и образующиеся из них макрофаги, способны также к нефагоцитарному уничтожению микрорганизмов путем воздействия на них микробоцидных веществ, секретируемых в межклеточное пространство.
Превращение моноцитов в макрофаги происходит в тканях под влиянием местных факторов микроокружения. Некоторые исследователи полагают, что до этого превращения моноциты способны несколько раз делиться. Образующиеся макрофаги обладают, наряду с общими свойствами, некоторыми частными отличиями, обусловленными ткане- и органоспецифическими особенностями их существования и функционирования.
Моноциты, мигрирующие в ткани, дают начало макрофагам соединительной ткани (гистиоцитам), ряду органоспецифических макрофагов – клеткам Купфера печени, альвеолярным макрофагам легкого, макрофагам костного мозга, селезенки, тимуса, лимфатических узлов, полостей тела (перитонеальным, плевральным, перикардиальным), центральной нервной системы (микроглии), остеокластам (рис. 1.2). Предполагают, что и специализированные макрофаги в тканях способны к делению, однако оно недостаточно для поддержания их популяций, которое осуществляется путем постоянного притока моноцитов из крови и их преобразования в макрофаги.
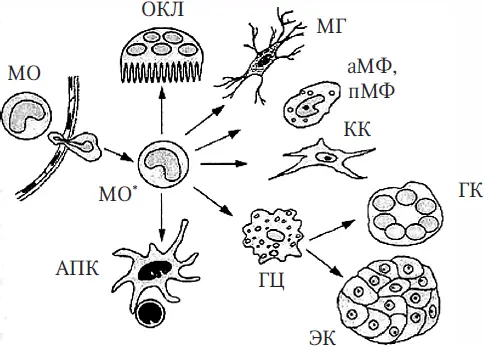
Рис. 1.2. Основные направления преобразования моноцитов в различные типы макрофагов и антиген-представляющие клетки:
АПК – антиген-представляющие клетки; МО – моноцит (в просвете кровеносного сосуда и мигрирующий через его стенку); МО *– моноцит в тканях, дифференцирующийся в АПК или один из видов макрофагов: гистиоцит (ГЦ), клетку Купфера (КК) синусоидов печени, альвеолярный макрофаг (аМФ), перитонеальный МФ (пМФ), клетку микроглии (МГ) и остеокласт (ОКЛ). В очаге воспаления ГЦ могут дать начало гигантской клетке (ГК) или эпителиоидным клеткам (ЭК)
Структурно-функциональные изменения моноцитов при их превращении в макрофаги :
– существенное увеличение размеров клетки (до 25–50 мкм), а также содержания в ее цитоплазме митохондрий, пиноцитозных пузырьков и, в особенности, лизосом; размеров комплекса Гольджи;
– преобразования плазмолеммы с формированием значительного числа складок, увеличением количества микроворсинок, нарастанием содержания рецепторов к IgG и С3-компоненту комплемента;
– повышение активности дыхательных и лизосомальных ферментов, одновременное снижение содержания пероксидазы;
– усиление подвижности, общей метаболической активности, адгезивных свойств, способности к пиноцитозу и фагоцитозу, общее возрастание микробицидности;
– изменения чувствительности к гормонам.
Фагоцитоз у макрофагов, как у моноцитов и нейтрофилов, сопровождается «респираторным взрывом». Он может осуществляться как неиммунный фагоцитоз (в отсутствие воздействия специфических факторов сыворотки) или как иммунный фагоцитоз (после опсонизации), благодаря наличию рецепторов к IgG и С3-компоненту комплемента на плазмолемме макрофага.
Макрофаги из различных органов и тканей обладают неодинаковыми свойствами, в частности, различиями в способности к уничтожению микробов; определенная специфика характерна и для отдельных клеток среди однотипных макрофагов.
Резистентность микроорганизмов к действию микробицидных механизмов макрофагов обеспечивается несколькими путями. Так, некоторые микробы, например возбудители туберкулеза (лат. Mycobacterium tuberculosis ) и токсоплазмоза (лат. Toxoplasma gondii ), избегают действия микробицидных механизмов и выживают в фагосомах макрофагов благодаря тому, что выделяют вещества, которые препятствуют слиянию лизосом с фагосомами. Другие (например, лейшмании) сохраняют жизнеспособность в фаголизосомах, так как обладают стенкой, резистентной к действию лизосомальных ферментов и низких зна чений рН, третьи (например, Trypanosoma cruzi) могут проникать из фагосом в гиалоплазму.
Активация макрофагов – процесс, обеспечивающий дальнейшее усиление их метаболической, локомоторной, фагоцитарной, антимикробной, противоопухолевой и секреторной способности – происходит при непосредственном контакте с микроорганизмами, а также под влиянием их продуктов или цитокинов – ИЛ-2, ИЛ-4, ФНО, ИФН-у, ФАТ, КСФ. Активированные макрофаги приобретают способность к уничтожению ряда микроорганизмов, которые могли выживать в фаголизосомах неактивированных клеток и даже разрушать их. Индукция выработки значительных количеств окиси азота усиливает цитотоксичность макрофагов по отношению к опухолевым клеткам и микроорганизмам. Макрофаги, не способные уничтожить фагоцитированные ими микроорганизмы, благодаря своей подвижности превращаются в их разносчиков и тем самым могут содействовать распространению инфекции по организму.
Читать дальшеИнтервал:
Закладка:










