Лариса Шалковская - Основы физиологии сердца
- Название:Основы физиологии сердца
- Автор:
- Жанр:
- Издательство:Литагент СпецЛит
- Год:2015
- ISBN:978-5-299-00608-7
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Лариса Шалковская - Основы физиологии сердца краткое содержание
Особое внимание уделено физиологическому обоснованию наиболее распространенных инструментальных методов исследования электрической активности, биомеханики, насосной и эндокринной функций сердца (электро-, фоно- и эхокардиография, электромагнитная и ультразвуковая флоуметрия), а также вопросам интерпретации данных клинической функциональной диагностики и фундаментальных экспериментальных исследований.
Пособие предназначено для студентов биологических и медицинских вузов, аспирантов, клинических ординаторов, широкого круга биологов, исследователей, преподавателей и практикующих врачей.
Основы физиологии сердца - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
В 1975 г. П. Крейнфилд предложил классифицировать кардиомиоциты по скорости развития фазы деполяризации потенциала действия на клетки с медленным и быстрым ответом. Соответственно, в сердце можно выделить два основных типа потенциалов действия – быстрый и медленный ответы.
Клетки с медленным ответом представлены в основном пейсмекерными клетками синоатриального узла и атриовентрикулярного соединения, а также специализированными клетками проводящей системы.
К клеткам с быстрым ответом относятся все сократительные кардиомиоциты, а также проводящие кардиомиоциты предсердий и некоторые элементы проводящей системы желудочков (волокна Пуркинье).
В «медленных» клетках в возникновении, а также поддержании потенциала действия основное участие принимает входящий через кальциевые каналы L-типа медленный ток I Ca2+ L. В возникновении же потенциала действия клеток с быстрым ответом ведущая роль принадлежит входящему натриевому току I Na+, протекающему через быстрые натриевые каналы. Однако для поддержания длительной (250–300 мс) деполяризации мембраны в клетках с быстрым ответом необходимы также активация кальциевых каналов L-типа и возникновение входящего тока I Ca2+ L. Блокада указанных каналов приводит к тому, что потенциал действия «быстрых» клеток становится коротким по продолжительности и сопоставим с таковым в скелетных мышцах (10–20 мс). Рассмотрим более подробно фазы потенциала действия «медленных» и «быстрых» клеток.
Клетки с медленным ответом.Для этого типа кардиомиоцитов характерны меньшая амплитуда потенциала действия и скорость его распространения по сравнению с «быстрыми» клетками. Фазы деполяризации и реполяризации потенциала действия «медленных» клеток протекают более плавно, чем в «быстрых» клетках (рис. 4).
Фаза быстрой деполяризации (0) характеризуется небольшой по сравнению с «быстрыми» клетками скоростью (до 20 В/с) нарастания и обеспечивается входящим током I Са2+ L. Пороговый потенциал, при котором активируется достаточное для обеспечения этого тока количество Са 2+-каналов L-типа, составляет около –40 мВ. Во время этой фазы отрицательный мембранный потенциал медленных клеток уменьшается до нуля, а затем происходит перезарядка мембраны (реверсия потенциала) до положительных значений, примерно +5… +10 мВ.
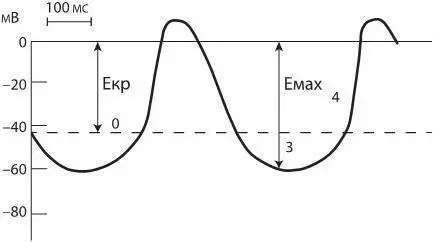
Рис. 4. Потенциал действия «медленных» клеток
Далее следует конечная реполяризация (3). По сравнению с «быстрыми» клетками в «медленных» клетках начальная быстрая реполяризация и фаза плато отсутствуют, а вершина потенциала действия сглажена (см. рис. 4). Величина мембранного потенциала в фазу конечной реполяризации определяется соотношением между усиливающимися выходящими токами ионов калия (I KS, I KRи I KUR) и уменьшающимся входящим током ионов кальция (I Са2+ L) на фоне медленной инактивации Са 2+-каналов L-типа. Завершается реполяризация достижением мембраной уровня максимального диастолического потенциала (–65…–50 мВ).
В пейсмекерных клетках синусового узла в результате спонтанной диастолической деполяризации (4) мембранный потенциал достигает порогового уровня и далее генерируется очередной потенциал действия. Следует подчеркнуть, что в пейсмекерах синоатриального узла скорость спонтанной диастолической деполяризации больше, чем в аналогичных кардиомиоцитах атриовентрикулярного соединения. Поэтому в условиях работающего сердца в пейсмекерных клетках атриовентрикулярного соединения эта фаза прерывается импульсом, приходящим от синоатриального узла, что и обусловливает возникновение в них потенциала действия. В изолированных клетках – водителях ритма атриовентрикулярного соединения спонтанная диастолическая деполяризация, развиваясь с меньшей скоростью, чем в синусовом узле, обеспечивает достижение критического уровня деполяризации и генерацию потенциалов действия, однако с меньшей частотой (40–60 в 1 мин), чем в синусовом узле (70–80 в 1 мин).
Исследования, проведенные в 1980–1990-х гг. с использованием методики patch-clamp , позволили установить, что возникновение спонтанной диастолической деполяризации в клетках – водителях ритма обусловлено сложным взаимодействием различных ионных токов в результате активации ионных каналов. Считается, что в пейсмекерных клетках синусового и атриовентрикулярного узлов уменьшение мембранного потенциала от его максимального отрицательного значения до критического уровня деполяризации обусловлено взаимодействием по крайней мере трех токов:
1) времязависимая задержка калиевой проводимости в результате инактивации каналов задержанного выходящего K +-тока, которая приводит к уменьшению выходящих калиевых токов I KSи I KR;
2) увеличение входящего натриевого тока I fчерез f-каналы;
3) усиление входящего тока ионов Ca 2+(I CaT) через каналы T-типа и «поддерживающего» кальциевого тока I st.
Можно полагать, что эти события происходят последовательно: вначале уменьшаются выходящие калиевые токи I KSи I KR, которые ранее обеспечивали фазу 3 (конечной реполяризации) потенциала действия пейсмекерной клетки; затем увеличивается входящий натриевый ток I f, и на заключительном этапе спонтанной диастолической деполяризации усиливаются входящие кальциевые токи I Ca2+ Tи I st. В результате мембранный потенциал клетки достигает критического уровня деполяризации (около –40 мВ), что приводит к активации кальциевых каналов L-типа, усилению входящего тока I Ca2+ Lи развитию фазы 0 (быстрой деполяризации) потенциала действия.
Как блокада кальциевых каналов T-типа (препарат верапамил), так и селективная блокада I f-каналов (препарат ивабрадин) приводят к снижению частоты генерации импульсов синусовым узлом и, следовательно, частоты сердечных сокращений. На этом эффекте основано применение некоторых (не всех!) антагонистов кальция для лечения аритмий. К брадикардии приводит также усиление выходящего калиевого тока, например, в ответ на применение агониста М-холинорецепторов – ацетилхолина. Более того, резкое усиление выходящего калиевого тока вызывает выраженную гиперполяризацию мембраны и может привести к прекращению спонтанной диастолической деполяризации в пейсмекерных клетках синусового узла, то есть остановке сердца. Эти данные доказывают роль взаимодействия торможения выходящих калиевых токов и усиления входящих – натриевого и кальциевого – в возникновении спонтанной диастолической деполяризации в пейсмекерных клетках синусового и атриовентрикулярного узлов.
Трансмембранный потенциал в покоящейся клетке намного менее негативен у клеток синоатриального и атриовентрикулярного узлов, чем у предсердных или желудочковых кардиомиоцитов. В этих условиях по крайней мере три ионных тока опосредуют медленную диастолическую деполяризацию: (1) входящий ток I f, вызванный гиперполяризацией; (2) входящий Ca 2+-ток I Ca; и (3) выходящий K +-ток I K.
Читать дальшеИнтервал:
Закладка: