Михаил Бармин - Общая и Неорганическая химия с примерами решения задач
- Название:Общая и Неорганическая химия с примерами решения задач
- Автор:
- Жанр:
- Издательство:Литагент Selfpub.ru (искл)
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Бармин - Общая и Неорганическая химия с примерами решения задач краткое содержание
Общая и Неорганическая химия с примерами решения задач - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
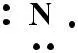
2P3 Px Py Pz

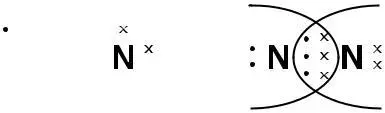
(N ≡ N )
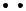
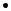

Такая связь, образовавшаяся путем обобществления электронов, называется ковалентной или гомеополярной или атомной.
В том случае, когда химическое соединение или молекула состоят из одинаковых атомов образуется неполярная ковалентная химическая связь.
При образовании молекул, состоящих из разных атомов, образуется ковалентная полярная связь, причем электронные пары смещаются в сторону более электроотрицательного атома. Для оценки полярной химической связи вводится величина дипольного момента, чем больше значение его, тем больше полярность связи ядрами. В результате проведенного расчета было установлено, что образование ковалентной химической связи возможно только лишь в том случае, если спины электронов ориентированы противоположно, т.е. ковалентная химическая связь представляет собой 2-х центровую, 2-х-электронную химическую связь с различной ориентацией спинов.
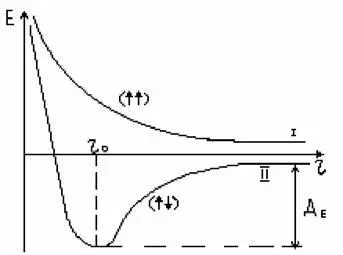
Е – энергия системы,
r – расстояние между ядрами, ДЕ – энергия диссоциации молекул Н, которую условно можно считать энергией образующейся химической связи
В случае кривой оси (I) не происходит образования химических связей. В случае противоположном (II) наблюдается образование минимума полной энергии, что свидетельствует об образовании ковалентной химической связи. r0 представляет собой межъядерное расстояние. Данный метод был распространен на различные химические соединения: органические, неорганические, комплексные соединения. Метод валентных связей является наглядным поскольку электронная пара может быть представлена в виде черты (валентность).
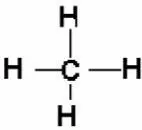
Многие свойства химических соединений объ-ясняются методом валентных связей, однако метод ВС не объясняет существование, напри-мер, ионов (Н 2 +) или молекул СО, NO
ВОЗБУЖДЕННЫЕ ВАЛЕНТНОСТИ АТОМОВ
Известно, что многие элементы способны участвовать в образовании нескольких типов химически связей. Это происходит при возбуждении атома и при переходе электрона на сво-бодные вакантные орбитали (p, d, f ).
При столкновении двух атомов Cl c различными ориентациями спинов ē происходит образование соединений с вален-тностью, равной 1.
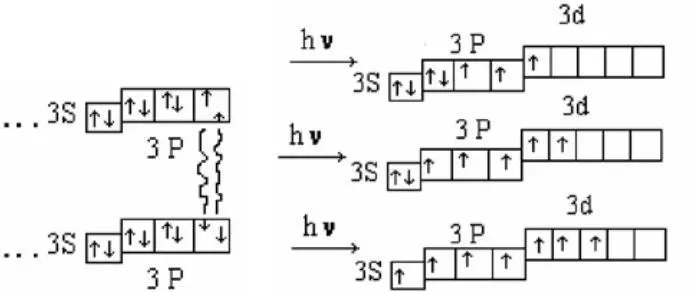
Таким образом, в рамках метода валентных связей и объясняется возможность образования возбужденных валентностей атомов Cl. По этой же схеме происходит образование возбужденных состояний других атомов.
НАСЫЩАЕМОСТЬ И НАПРАВЛЕННОСТЬ СВЯЗЕЙ В
ПРОСТРАНСТВЕ
Важным свойством химических связей является ее насыщаемость и направление в пространстве, что характеризует строение молекулы. Насыщение химических связей объясняется с позиций запрета Паули. Направление химических связей объ-
ясняется пространственной ориентацией электронных атомных орбиталей. В зависимости от ориентации атомных орбиталей происходит условное деление на орбитали σ и π
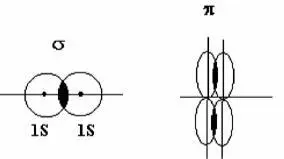
Условное обозначение выбирается относительно элементов симметрии. Если элементом симметрии является ось симметрии, такая связь называется σ-связью. Если элементы симметрии – плоскость, то такая связь получила название π-связи.
H 2O NH 3
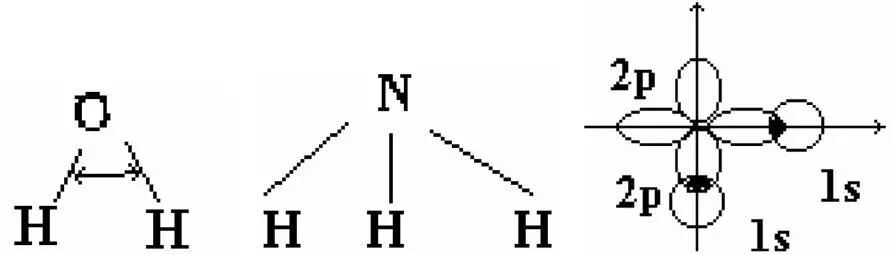

HOH = 104°3

HNH = 107°

HOH =104° 30'
Следовало ожидать, что значение валентных углов для этих молекул должны быть равны 90°. Однако, экспериментальные данные показали, что значения этих углов равны (см. выше). Объяснение этого расхождения впервые было получено Поли-нгом введением гипотезы гибридизации.
ГИБРИДИЗАЦИЯ ОРБИТАЛЕЙ
Рассмотрение понятия гибридизации орбиталей, лучше всего понять на примере: бериллия, бора, углерода
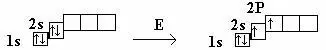
4Be 1S22S2
Be → Be*
ΔΕ = 323 кДж/моль
Атом Be, поглощая энергию, переходит в возбужденное состояние. При образовании химических связей происходит смешивание по форме и энергии электронных орбиталей. В результате об-разуется смешанная (гибридная) электронная орбиталь.
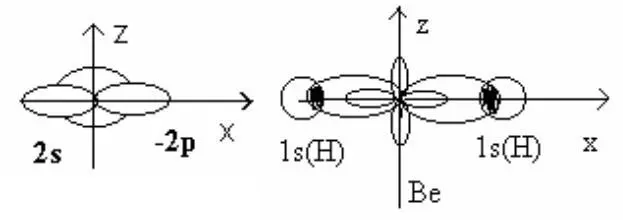
Произошло образование новой sp –гибридной орбитали.
При смешивании по форме и энергии двух орбиталей s– и p-типа наблюдается выигрыш в энергии, т.е. понижение энергии по сравнению с s– и р-орбиталями.
При образовании химических связей между s– и p-гибрид-ными орбиталями и 1 S орбиталями для атома Н в случае обра-зования гибрида ВеН 2вероятность перекрывания электронных орбиталей также увеличивается, что проводит к дальнейшему понижению энергии. Таким образом, при гибридизации и при образовании химических связей, энергия возбуждения компенсируется; общая энергия возбуждения молекул становится меньше по сравнению с энергией изолированных атомов на величину энергии химической связи.
ПРОСТРАНСТВЕННАЯ ОРИЕНТАЦИЯ
Пространственное направление гибридных sp-орбиталей та-ково, что в результате образуется линейная структура молекулы.
5B 1s22s22p1
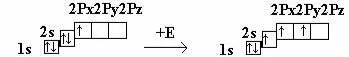
sp2 -гибридизация
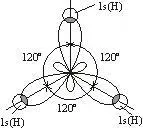
три Sp2 -гибридизационных атомных орбит образуют плоскостную структуру
Читать дальшеИнтервал:
Закладка:










