Михаил Бармин - Общая и Неорганическая химия с примерами решения задач
- Название:Общая и Неорганическая химия с примерами решения задач
- Автор:
- Жанр:
- Издательство:Литагент Selfpub.ru (искл)
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Бармин - Общая и Неорганическая химия с примерами решения задач краткое содержание
Общая и Неорганическая химия с примерами решения задач - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Механизмы реальных реакций являются сложными, В соответствии с этим постановка показателя степени стехиометрических коэффициентов реакции неправомерна.
На практике для определения кинетических параметров, определяются значения концентрации некоторых реагентов. Сумма показателей кинетических коэффициентов для уравне-ния скорости химических реакций определяет порядок реак-ции. Однако в химии встречаются реакции нулевого, первого, второго и значительно реже – третьего порядка. Порядок реакции может быть дробным, что определяется механизмом реакции.
В химической кинетике важным является понятие молеку-лярности реакции. Под молекулярностью реакции понимают количество молекул, участвующих в элементарном акте процесса. В зависимости от этого различают мономолекулярные реакции, когда в элементарном акте химического процесса участвует 1 молекула (процесс разложения). Димолекулярные реакции, когда в химическом процессе участвуют две молекулы. Тримолекулярные реакции, когда в элементарном акте участвуют 3 молекулы. Эти химические реакции являются до-
статочно редкими. Реакций с более высокой молекулярностью не встречается.
Зависимость скорости химических реакций от температуры
Впервые Вант-Гофф экспериментально показал, что нагре-вание на 10°С дает увеличение скорости химических реакций в
2-4 раза, т.е.
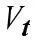
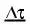

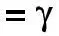
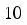
,
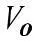
где γ – коэффициент Вант-Гоффа, равен 2 ÷ -4 Показатель степени – число температурных скачков по 10° Кинетическая энергия равна
Ek = mV2/2 = 3/2 KT
где К – постоянная Больцмана, Т – абсолютная температура
при нагреве на 10°.
mV12/2 = 3/2 KT1
= 3/2 K • 273
V
mV22/2 = 3/2 KT2
= 3/2 K • 283
2/V 2 = 283/273 = 1,04; V
/V = 1,02
2
1
2
1
Таким образом, при увеличении температуры на 10° скорость химических реакций увеличивается на 2 %, а не на 200-400, как это следует из уравнения Вант-Гоффа.
Ответ на этот вопрос был впервые дан Аррениусом. Он предположил, что не все соударения приводят к образованию продуктов реакций, а существуют так называемые активные соударения.
Как показано на рис., на оси ординат количество молекул, обладающих определенной энергией столкновения, на оси абсцисс – энергия соударения. При температуре Т, активными яв-ляются такие молекулы, для которых энергия соударения много больше энергии Eа, получившей название энергии активации.
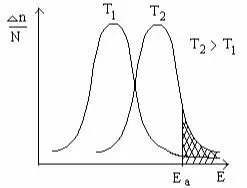
Для температуры Т2 эта зависимость аналогична. В этом слу-чае резко возрастает количество активных молекул, что в конечном итоге к приводит к увеличению скоростей химических реакций, Аррениус на основании теоретических и эксперимен-тальных данных показал, что постоянная скорости химических реакций зависит от температуры и определяется по уравнению:
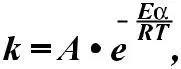
где – А – фактор соударений, характеризующий частоту активных соударений; е – основание натурального логариф-ма = 2.71, Еа – энергия активации, R – газовая постоянная, T – абсолютная температура.
На основании этого уравнения с высокой степенью точнос-ти можно определить константу k, а следовательно и саму V. Однако, не для всех случаев соблюдается совпадение теорети-ческих значений константы скорости химическиx реакций с экспериментальным определением.
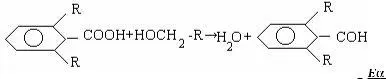
где Р – стерический фактор, Р ≤ 1 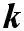
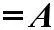

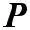

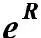
 В этом уравнений Р – стерический фактор учитывает объем
В этом уравнений Р – стерический фактор учитывает объем
заместителей в реагирующих молекулах. Чем больше заместитель, тем меньше становится вероятность атаки реакционного центра, тем больше наблюдается расхождений между расчетными и экспериментальными значениями скоростей. Стери-ческии фактор «Р» определяется экспериментально.
Понятие об активированном комплексе (о переходном состоянии)
При взаимодействии реагентов возможны образования различных промежуточных продуктов реакции, причем скорость этих реакций может существенно отличаться. Кроме того, из промежуточных продуктов реакции при столкновении, могут проходить процессы, параллельные основной реакции. Таким образом, все совокупности данных о строении исходных реагентов, промежуточных продуктов реакции и конечных во времени характеризует механизм химической реакции. При изучении механизма химических реакций используются различные экспериментальные и теоретические методы.
В настоящее время наибольшие успехи были получены с помощью теории абсолютных скоростей реакций и теории активированного комплекса. Теория абсолютных скоростей реакции основывается на классической теории взаимодействия двух частиц. В теории активированного комплекса предпола-гается образование на промежуточной стадии так называемого переходного состояния или активизированного комплекса.
H2 + J2 < = > 2HJ
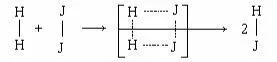
τ = 10– 8 с
При столкновении двух частиц А и В при образовании акти-вированного комплекса, возможно перекрывание электронных оболочек, что приводит к ослаблению старых химических связей
образованию новых химических связей. Образовавшееся таким образом переходное состояние является термодинамическим неустойчивым и возможно разрушение его с образование как исходных реагентов, так и продуктов реакции (см. график). Следует отметить, что не каждое активное столкновение можно привести к образованию активированного комплекса, а только такие со-ударения, при которых осуществляется максимальное перекры-вание электронных оболочек взаимодействующих атомов.
Таким образом, для проведения химического процесса, т.е. для образования активированного состояния, следует затра-
тить необходимое количество энергии, которое получило назва-
ние энергии активации – Ea, которая представляет собой разницу между энергиями образования активированного комплекса
Читать дальшеИнтервал:
Закладка:










