Лев Николаев - Металлы в живых организмах
- Название:Металлы в живых организмах
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1986
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Лев Николаев - Металлы в живых организмах краткое содержание
Металлы в живых организмах - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
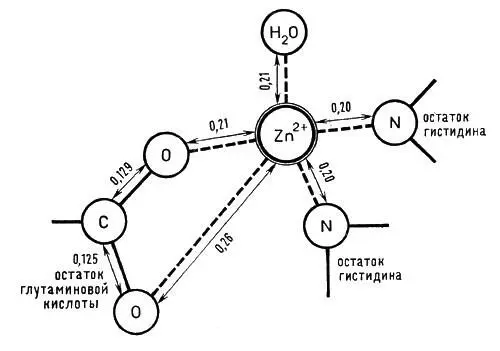
Рис. 5. Строение активного центра фермента карбоксипептидазы (расстояния между атомами даны в нанометрах)
Цинк удается заместить на ионы других металлов: кобальт(II), марганец(II), никель(II), причем получаются активные карбоксипептидазы. Относительная легкость такой замены и образование активных соединений с другими ионами — характерный признак многих случаев активации; здесь специфичность металла менее выражена, чем, например, в гемовых комплексах.
Все эти ионы способствуют связыванию субстрата (т. е. полипептидных белковых цепей) с активными центрами, кроме того, ион металла оттягивает на себя электроны кислорода карбонильной группы С=O (в пептидной связке СО-NH), в результате чего двойная связь между С и О поляризуется и облегчается ее реакция с водой, приводящая к разрыву С-N связи:
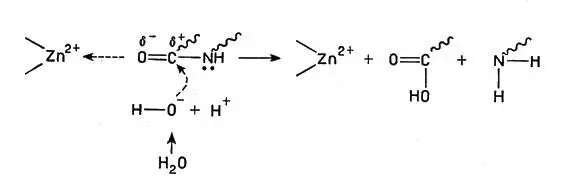
Ион металла оттягивает на себя электроны кислорода карбонильной группы С=O
(волнистая линия — полимерная молекула белка).
Ионы цинка, как мы уже упоминали, входят в состав еще одного фермента, функции которого тесно связаны с дыханием, — карбонангидразы. Этот фермент был выделен из эритроцитов человека и животных и оказался белковым соединением с молекулярной массой около 30000. На одну молекулу фермента приходится один атом цинка. В зависимости от источника получения молекулярная масса несколько колеблется, поэтому считают, что существует несколько видов карбонангидразы (изоферменты).
Карбонангидраза катализирует процессы гидратации диоксида углерода, т. е. образование иона НСО 3 -, и процессы дегидратации, связанные с выделением диоксида углерода вследствие разложения аниона угольной кислоты. Первый процесс совершается в клетках, отдающих СО 2как продукт своей жизнедеятельности, а второй — в альвеолах легких, где выделение СО 2должно происходить в надлежащем темпе.
Обе реакции можно записать так:
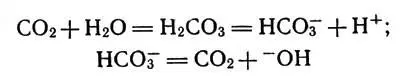
Карбонангидраза катализирует процессы гидратации диоксида углерода и процессы дегидратации
Первая представляет гидратацию СO 2, вторая — разложение иона НСО 3 -.
Роль иона цинка еще не выяснена окончательно. Вероятно, ион цинка катализирует разложение НСО 3 -в результате образования комплекса, претерпевающего быстрый распад:
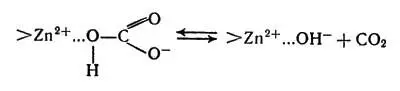
Ион цинка катализирует разложение НСО 3 -в результате образования комплекса, претерпевающего быстрый распад
Прямая реакция соответствует разложению бикарбонатов и протекает в легочных альвеолах, а обратная соответствует связыванию СO 2в клетках.
Ион цинка находится глубоко в центральной части белковой молекулы и связан с белком, насколько можно судить, с помощью трех гистидиновых остатков.
Киназы. Мы убедились, что для работы биологических машин необходимы переносы электронов и кислорода; дело, однако, этим не ограничивается. Ферменты клетки не перемешаны в беспорядке — важнейшие из них фиксированы в определенных зонах различных органелл (митохондрий, рибосом и др.), и перестройка молекул пищевых веществ, как уже упоминалось, идет строго согласованно и в нужной последовательности.
Для такой работы необходимо иметь средства, чтобы переносить и другие группы — особенно те, которые существенно изменяют запас энергии в молекуле и таким образом изменяют ее реакционную способность. Ферменты, катализирующие переносы фосфатной группы PO 3 2-от молекулы аденозинтрифосфорной кислоты к другим молекулам, называются киназами (от греч. kineo — "двигаю, перемещаю").
Аденозинтрифосфорная кислота, сокращенно обозначенная АТФ, является одним из самых важных биологически активных соединений. Подвергаясь гидролизу, эта кислота отщепляет одну молекулу фосфорной кислоты (Ф), образуя аденозиндифосфорную кислоту (АДФ); при этом выделяется относительно много энергии. При образовании АТФ из АДФ и Ф энергия соответственно поглощается. Ниже приведено уравнение гидролиза АТФ [3] В формулах АТФ и креатинфосфата (см. ниже) волнистая линия обозначает химическую связь, богатую энергией, так называемую макроэргическую связь. Открытые концы вертикальных линий (связей) указывают положения атомов водорода.
(и обратный процесс):
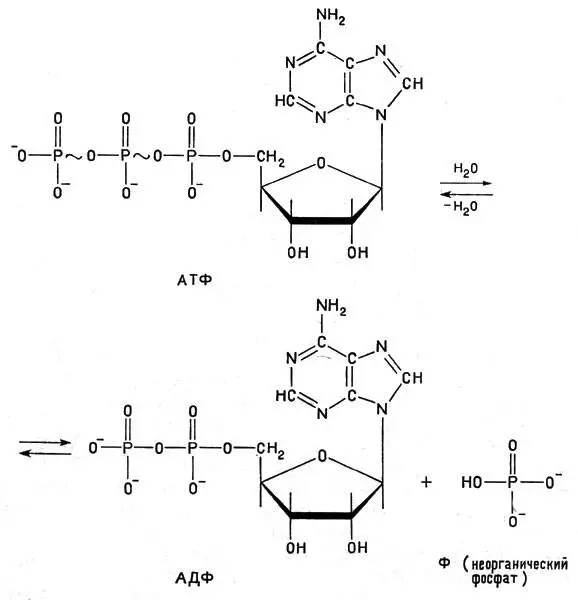
Уравнение гидролиза АТФ (и обратный процесс)
Если АТФ реагирует с какой-либо другой молекулой, например с молекулой глюкозы, то, передавая ей фосфатную группу, она передает молекуле и значительный запас энергии (заряжает молекулу глюкозы энергией):
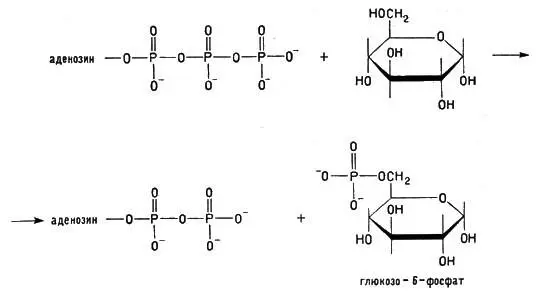
Реакция АТФ с молекулой глюкозы
Вот почему АТФ в клетках выполняет функции аккумулятора энергии.
Именно такого типа реакции, происходящие с переносом фосфата от АТФ на другой субстрат, и катализируются киназами. Киназы активируются ионами металлов, чаще всего магнием, а также кальцием и марганцем. Специфичность в этих случаях менее выражена, и указанные ионы можно иногда заменить на ионы кобальта или цинка. Но все ионы металлов, необходимые для работы киназ, двузарядны (степень окисления +2). Молекулярные массы киназ около 1000000, но неодинаковы у различных ферментов этой группы.
Ион металла, по-видимому, связывает АТФ и белок; доказано, что ионы металлов-активаторов образуют с АТФ комплексы. Способ связывания иона металла не всегда удается точно определить, хотя это важная сторона вопроса. Так, например, ион кальция активирует киназы, если он связан с белком-ферментом (Ф) через субстрат реакции:
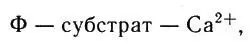
Ион кальция активирует киназы, если он связан с белком-ферментом (Ф) через субстрат реакции
но тормозит реакцию, если связан непосредственно с белком:
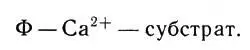
Ион кальция тормозит реакцию, если связан непосредственно с белком
Кроме того, ионы металлов, как активные частицы, способны вступать в реакции комплексообразования и с молекулами субстрата — того вещества, на которое переносится группа РО 3 2-. По-видимому, основным этапом действия киназ является образование комплекса металл — АТФ, который, фиксируясь на белке, отдает фосфатный остаток субстрату.
Читать дальшеИнтервал:
Закладка: