БСЭ БСЭ - Большая Советская Энциклопедия (ФО)
- Название:Большая Советская Энциклопедия (ФО)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (ФО) краткое содержание
Большая Советская Энциклопедия (ФО) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
При температурах выше 2000°C Ф. реагирует с углеродом с образованием карбида PC 3– вещества, не растворяющегося в обычных растворителях и не взаимодействующего ни с кислотами, ни со щелочами. При нагревании с металлами Ф. образует фосфиды.
Ф. образует многочисленные фосфорорганические соединения.
Получение. производство элементарного Ф. осуществляется электротермическим восстановлением его из природных фосфатов (апатитов или фосфоритов) при 1400–1600 °С коксом в присутствии кремнезёма (кварцевого песка):
2Ca 3(PO 4) 2+ 10C + n SiO 2= P 4+ 10CO + 6CaO× n SiO 2
Предварительно измельченная и обогащенная фосфорсодержащая руда смешивается в заданных соотношениях с кремнезёмом и коксом и загружается в электропечь. Кремнезём необходим для снижения температуры реакции, а также увеличения ее скорости за счет связывания выделяющейся в процессе восстановления окиси кальция в силикат кальция, который непрерывно удаляется в виде расплавленного шлака. В шлак переходят также силикаты и окислы алюминия, магния, железа и др. примеси, а также феррофосфор (Fe 2P, FeP, Fe 3P), образующийся при взаимодействии части восстановленного железа с Ф. Феррофосфор, а также растворённые в нём небольшие количества фосфидов марганца и др. металлов по мере накопления удаляются из электропечи с целью последующего использования при производстве специальных сталей.
Пары Ф. выходят из электропечи вместе с газообразными побочными продуктами и летучими примесями (CO, SiF 4, PH 3, пары воды, продукты пиролиза органических примесей шихты и др.) при температуре 250–350 °С. После очистки от пыли содержащие фосфор газы направляют в конденсационные установки, в которых при температуре не ниже 50 °С собирают под водой жидкий технический белый Ф.
Разрабатываются методы получения Ф. с применением газообразных восстановителей, плазменных реакторов с целью интенсификации производства за счёт повышения температур до 2500–3000 °С, т. е. выше температур диссоциации природных фосфатов и газов-восстановителей (например, метана), используемых в качестве транспортирующего газа в низкотемпературной плазме.
Применение. Основная масса производимого Ф. перерабатывается в фосфорную кислоту и получаемые на её основе фосфорные удобрения и технические соли ( фосфаты ) .
Белый Ф. используется в зажигательных и дымовых снарядах, бомбах; красный Ф. – в спичечном производстве. Ф. применяется в производстве сплавов цветных металлов как раскислитель. Введение до 1% Ф. увеличивает жаропрочность таких сплавов, как фехраль, хромаль. Ф. входит в состав некоторых бронз, т.к. повышает их жидкотекучесть и стойкость против истирания. Фосфиды металлов, а также некоторых неметаллов (В, Si, As и т.п.) используются при получении и легировании полупроводниковых материалов. Частично Ф. применяется для получения хлоридов и сульфидов, которые служат исходными веществами для производства фосфорсодержащих пластификаторов (например, трикрезилфосфат, трибутилфосфат и др.), медикаментов, фосфорорганических пестицидов, а также применяются в качестве добавок в смазочные вещества и в горючее.
Техника безопасности. Белый Ф. и его соединения высокотоксичны. Работа с Ф. требует тщательной герметизации аппаратуры; хранить белый Ф. следует под водой или в герметически закрытой металлической таре. При работе с Ф. следует строго соблюдать правила техники безопасности.
Л. В. Кубасова.
Ф. в организме. Ф. – один из важнейших биогенных элементов, необходимый для жизнедеятельности всех организмов. Присутствует в живых клетках в виде орто- и пирофосфорной кислот и их производных, а также входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, фосфорных эфиров углеводов, многих коферментов и др. органических соединений. Благодаря особенностям химического строения атомы Ф., подобно атомам серы, способны к образованию богатых энергией связей в макроэргических соединениях; аденозинтрифосфорной кислоте (АТФ), креатин фосфате и др. (см. Окислительное фосфорилирование ) . В процессе биологической эволюции именно фосфорные соединения стали основными, универсальными хранителями генетической информации и переносчиками энергии во всех живых системах. Др. важная роль соединений Ф. в организме заключается в том, что ферментативное присоединение фосфорильного остатка ( 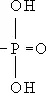 ) к различным органическим соединениям ( фосфорилирование ) служит как бы «пропуском» для их участия в обмене веществ, и, наоборот, отщепление фосфорильного остатка (дефосфорилирование) исключает эти соединения из активного обмена. Ферменты обмена Ф. – киназы, фосфорилазы и фосфатазы. Главную роль в превращениях соединений Ф. в организме животных и человека играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D.
) к различным органическим соединениям ( фосфорилирование ) служит как бы «пропуском» для их участия в обмене веществ, и, наоборот, отщепление фосфорильного остатка (дефосфорилирование) исключает эти соединения из активного обмена. Ферменты обмена Ф. – киназы, фосфорилазы и фосфатазы. Главную роль в превращениях соединений Ф. в организме животных и человека играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D.
Содержание Ф. (в мг на 100 г сухого вещества) в тканях растений – 230–350, морских животных – 400–1800, наземных – 1700–4400, у бактерий – около 3000; в организме человека особенно много Ф. в костной ткани (несколько более 5000), в тканях мозга (около 4000) и в мышцах (220–270). Суточная потребность человека в Ф. 1–1,2 г (у детей она выше, чем у взрослых). Из продуктов питания наиболее богаты Ф. сыр, мясо, яйца, зерно бобовых культур (горох, фасоль и др.). Баланс Ф. в организме зависит от общего состояния обмена веществ. Нарушение фосфорного обмена приводит к глубоким биохимическим изменениям, в первую очередь в энергетическом обмене. При недостатке Ф. в организме у животных и человека развиваются остеопороз и др. заболевания костей, у растений – фосфорное голодание (см. Диагностика питания растений ) . Источником Ф. в живой природе служат его неорганические соединения, содержащиеся в почве и растворённые в воде. Из почвы Ф. извлекается растениями в виде растворимых фосфатов. Животные обычно получают достаточное количество Ф. с пищей. После гибели организмов Ф. вновь поступает в почву и донные отложения, участвуя т. о. в круговороте веществ. Важная роль Ф. в регуляции обменных процессов обусловливает высокую чувствительность многих ферментных систем живых клеток к действию фосфорорганических соединений. Это обстоятельство используют в медицине при разработке лечебных препаратов, в сельском хозяйстве при производстве фосфорных удобрений, а также при создании эффективных инсектицидов. Многие соединения Ф. чрезвычайно токсичны и некоторые из фосфорорганических соединений могут быть причислены к боевым отравляющим веществам (зарин, зоман, табун). Радиоактивный изотоп Ф. 32P широко используют в биологии и медицине как индикатор при исследовании всех видов обмена веществ и энергии в живых организмах (см. Изотопные индикаторы ) .
Читать дальшеИнтервал:
Закладка:
