Михаил Никитин - Происхождение жизни. От туманности до клетки
- Название:Происхождение жизни. От туманности до клетки
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2016
- Город:Москва
- ISBN:978-5-9614-4350-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Никитин - Происхождение жизни. От туманности до клетки краткое содержание
Происхождение жизни. От туманности до клетки - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
На первом шаге сквален-монооксигеназа катализирует присоединение кислорода к концевой двойной связи сквалена, образуя сквален-2,3-эпоксид. Для этой реакции требуется молекулярный кислород, хотя и в очень малой концентрации. Затем ланостерол-синтаза катализирует восстановление эпоксида, при этом неустойчивый продукт восстановления – радикал сквалена – перестраивает двойные связи в замкнутые кольца, образуя ланостерол (рис. 18.6). Ланостерол дает начало всем другим стероидам путем модификации боковых групп.
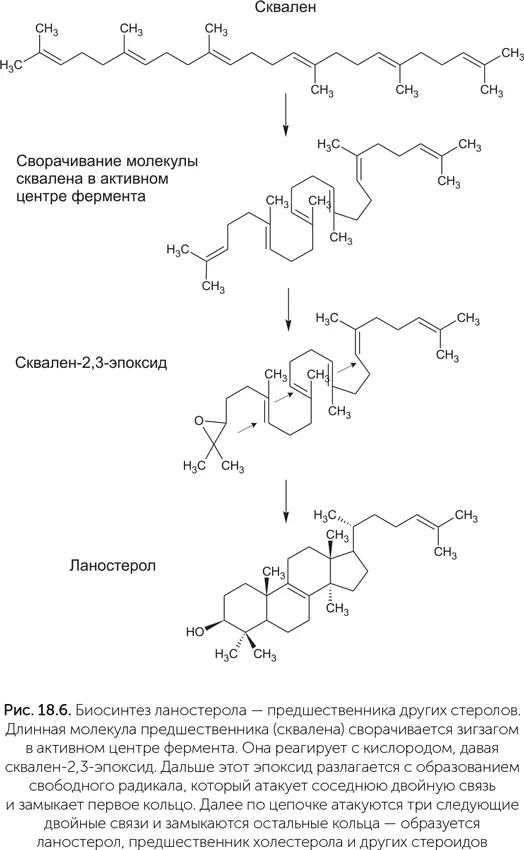
Из-за крайней важности стеролов для эукариотической клетки происхождение ферментов их биосинтеза внимательно исследовалось. Сходные ферменты, синтезирующие те же стеролы, были обнаружены у некоторых гамма-протеобактерий, например Methylococcus capsulatus (Lamb et al., 2007), у Gemmata obscuriglobus из планктомицетов (Pearson et al., 2003) и у ряда микобактерий, например Plesiocystis pacifica и Stigmatella aurantiaca. Однако подробное исследование показало, что все эти ферменты бактерий получены горизонтальным переносом от эукариот уже после расхождения линий растений и животных (Desmond, Gribaldo, 2009). Первый шаг биосинтеза стеролов – присоединение кислорода к сквалену – мог быть поначалу одним из способов защиты от молекулярного кислорода, и лишь потом нашлось применение полученному сквален-2,3-эпоксиду.
Большая часть эукариотических генов бактериального происхождения, не принадлежавших предкам митохондрий и пластид, кодирует защитные, рецепторные, транспортные, сигнальные и регуляторные белки. Сюда относятся, например, белки теплового шока Hsp90, белки устойчивости к тяжелым металлам TerC и Ttg2 и др. Что интересно, белки, которые у эукариот обеспечивают взаимодействие между компонентами клетки, у бактерий нужны для связей между разными клеткам в сообществе. Например, Tim44 эукариот необходим для транспорта белков через внутреннюю мембрану митохондрий из цитоплазмы, а его бактериальные родственники экспортируют белки из клеток во внешнюю среду. Это свидетельствует о том, что при возникновении эукариотической клетки под одной мембраной оказались уже отработанные системы связи клеток в сообществе.
В целом можно сказать, что те белки эукариот, которые получены от других бактерий (не предков митохондрий и пластид), не имеют какого-то одного источника. Скорее, они были получены от множества разных бактерий путем горизонтального переноса генов. Гипотезы, в которых до симбиоза с протеобактериями было слияние клеток какой-то другой бактерии с археей, не поддерживаются этими геномными данными.
Архейный предок эукариот
Хотя участие какой-то археи в происхождении эукариот давно стало очевидно, выделить конкретную группу архей, к которой мог относиться предок эукариот, оказалось не так просто. Многие компоненты эукариотной клетки были найдены у отдельных видов архей, но это были разные виды, относящиеся к разным крупным группам архей. Так обстоит дело, например, с цитоскелетными белками тубулинами. Давно известны белки FtsZ, отдаленно похожие по последовательности на тубулин и широко распространенные у бактерий и архей. Они собираются в пластины и трубки и необходимы для деления прокариотических клеток. В 2012 году были найдены артубулины – близкие родственники тубулина – у двух видов архей рода Nitrosoarchaeum , принадлежащих к группе Thaumarchaeota . Их функция пока неизвестна (Yutin, Koonin, 2012).
Аналогично у бактерий и архей широко распространены белки, отдаленно сходные с актином; их называют MreB. Они собираются в тонкие нити и участвуют в перетяжке делящейся бактериальной клетки. Другие дальние белковые родственники актина кодируются плазмидами (маленькими независимыми молекулами ДНК у бактерий) и служат для их расхождения при делении клетки. В 2009 году у нескольких видов группы Crenarchaeota были обнаружены кренактины, весьма похожие на актин эукариот (Ettema et al., 2011). Кренактины образуют нити, которые придают клеткам палочковидную форму, часто с разветвлениями. По своей последовательности кренактины близки не только к актинам, но и к белкам Arp2/Arp3 (Actin-related proteins), которые у эукариот образуют разветвления актиновых нитей. В некоторых случаях совместная полимеризация актина и Arp2/Arp3 на внутренней стороне клеточной мембраны достаточна для отшнуровки фагоцитозного пузырька (Yutin et al., 2009).
Наряду с артубулинами у Thaumarchaeota обнаружились гены еще одной эукариотической системы – ESCRT-III (endosomal sorting complex required for transport). Эта группа белков связана с мембранами комплекса Гольджи, эндоплазматического ретикулума и вакуолей; она участвует в сортировке содержимого мембранных пузырьков. В клетках Thaumarchaeota белки этого комплекса необходимы для деления клеток, работая вместо отсутствующего у них FtsZ (Makarova et al., 2010).
В геноме Caldiarchaeum subterranum , прочитанном в 2010 году, были обнаружены гены важной для эукариот системы убиквитиновой модификации белков. Эта система пришивает убиквитин – маленький белок – к различным клеточным белкам. Убиквитин служит обычно меткой для уничтожения белков. Кроме собственно убиквитина (Ub) в нее в минимальном варианте входит три фермента – Е1, Е2 и Е3, катализирующие разные стадии присоединения Ub. У бактерий известны отдаленные родственники Е1 и Е2, но их функции не связаны с убиквитином, они катализируют включение серы при синтезе витамина В 1и молибденовых кластеров ферментов.
Меченые убиквитином белки обычно разрушаются в протеасомах – специальных белковых комплексах для выборочного уничтожения дефектных и ненужных белков. Функциональное ядро протеасомы состоит из 28 белковых молекул, собранных в четыре кольца из семи субъединиц; кроме того, в ее работе принимают участие дополнительные регуляторные субъединицы. Протеасомы были известны ранее у некоторых бактерий ( Mycobacterium tuberculosum ) и архей ( Haloferax volcanii ), но убиквитиновой системы у этих видов нет. Протеасомы есть и у Caldiarchaeum subterranum, они похожи на эукариотические также по наличию белка RPN11, который опознает убиквитиновые метки на белках (Nunoura et al., 2011).
Почти все, что мы знаем об устройстве и образе жизни бактерий и архей, ученые узнали, выращивая и изучая микробов в лаборатории. Те микробы, для которых не удалось подобрать условия выращивания, долго оставались неизвестными. В XXI веке появились методы метагеномики – анализа всей ДНК, содержащейся в природной пробе (вода, почва, ил). Метагеномика позволяет оценить разнообразие микробов в пробе без культивирования. Используя метагеномный способ, ученые быстро выяснили, что микробное разнообразие в природе огромно. Более 99 % видов микробов, которые есть в природе, никогда не вырастали в лаборатории, и до появления метагеномики об их существовании можно было только догадываться. Хуже того, половина крупных групп бактерий и архей не имеет ни одного культивируемого представителя и известна только по метагеномным данным. Ученые подозревали, что среди них скрываются и близкие родственники эукариот.
Читать дальшеИнтервал:
Закладка:







