Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
2. При действии избытка воды на 10 г некоторого металла из главной подгруппы II группы выделилось 5,6 (н.у.) газа. О каком металле идет речь?
3. В концентрированный раствор щелочи вносят 2,7 г алюминия. Найдите объем (в литрах, н.у.) собранного газа.
4. На сжигание 0,64 г металла расходуется 12 мл (н.у.) кислорода. Какой металл был взят?
5. Металлическая пластинка массой 50 г после пребывания в соляной кислоте уменьшилась на 1,68 % (по массе), при этом выделилось 0,336 л (н.у.) газа. Из какого металла изготовлена пластинка?
6. При нагревании 139,2 г оксида металла (I) выделилось 6,72 л (н.у.) газа. Оксид какого металла был использован?
7. После обработки равномолярной смеси Mg + Zn избытком едкого натра (конц.) образовалось 4,48 л (н.у.) газа. Рассчитайте массу (в граммах) исходной смеси.
8. Установите объем (в литрах, н.у.) хлора, вступившего в реакцию со щелочью в горячем растворе, если образовалось 0,46 моль хлорид-ионов.
9. Вычислите объем (в литрах, н.у.) полученного газа, если в реакцию с кипящей серной кислотой (конц.) вступило O,5 моль фторида кальция.
10. Сероводород (4,48 л при н.у.) смешали с избытком диоксида серы. Какова масса (в граммах) твердого продукта этой реакции?
11. Поглощение 5,6 л (н.у.) сероводорода раствором нитрата висмута (III) приводит к выпадению осадка средней соли. Найдите массу (в граммах) этого осадка.
12. Раствор гидроксида цезия поглотил 17,92 л (н.у.) диоксида серы с образованием средней соли. Вычислите массу (в граммах) щелочи, истраченной на реакцию.
13. Прокалили 99,3 г нитрата свинца (II). Определите суммарный объем (в литрах, н.у.) полученных газов.
14. В избыток воды внесено 3,75 моль оксида фосфора (V). Какая масса (в граммах) продукта образовалась?
15. Прокаливанием 192 г карбоната аммония получена смесь двух газов и вода. Установите общий объем (в литрах, н.у.) смеси.
16. Внесено 14 г аморфного кремния в концентрированный раствор едкого натра. Рассчитайте объем (в литрах, н.у.) собранного газа.
17. Какой объем в литрах (н.у.) хлора потребуется для получения из метана 4 моль хлороформа?
18. Найдите количество бромэтана (моль), вступившее в реакцию с натрием, если образовалось 237 л (н.у.) органического продукта.
19. Ацетилен обесцвечивает бромную воду с образованием 3,46 г конечного продукта. Определите объем (мл, н.у.) затраченного алкина.
20. Каталитическая реакция дегидрирования 49 г метилциклогексана приводит к получению гомолога бензола. Вычислите объем (в литрах, н.у.) образовавшегося одновременно газа.
21. Этанол с плотностью 0,8 г/мл затрачен на получение 44,8 л (н.у.) дивинила. Установите расход (мл) спирта.
22. На восстановление 10 кмоль этаналя в соответствующий спирт используют водород. Найдите его затраченный объем (м 3, н.у.).
23. Рассчитайте объем (в литрах, н.у.) газа, полученного при спиртовом брожении 5 моль глюкозы.
24. При сгорании природной аминокислоты (с одной группой NH 2в молекуле) в кислороде получена смесь N 2+ СO 2общим объемом 0,56 л (н.у.) и плотностью по водороду 20,4. Определите массу (мг) взятой кислоты.
15.4. Тепловой эффект реакции
Вычислите тепловой эффект (кДж) реакции полной нейтрализации гидроксида натрия серной кислотой, если в расчете на 10 г щелочи выделяется 16,25 кДж теплоты.
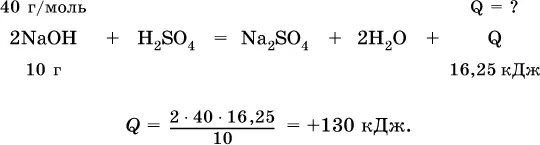
1. В реакции между железом и хлором на 11,2 л (н.у.) окислителя приходится выделение 132 кДж теплоты, следовательно, в расчете на 0,5 моль железа выделится количество теплоты (кДж), равное
1) +198
2) +148,5
3) +99
4) +49,5
2. Триоксид серы массой 280 г вносят в воду, протекает реакция с тепловым эффектом +73 кДж. Количество теплоты (кДж) в условиях опыта равно
1) +204,4
2) +255,5
3) +408,8
4) +511
3. Термическое разложение нитрата калия привело к выделению 4,48 л (н.у.) газа. Тепловой эффект реакции равен -282 кДж, следовательно, сопровождающее процесс количество теплоты (кДж) составляет
1) -56,4
2) -112,8
3) -225,6
4) -282
4. Сожжено 10 л (н.у.) аммиака на воздухе (тепловой эффект реакции +1532 кДж). По условию опыта количество теплоты составит
1) +171
2) +342
3) +766
4) +855
5. Термическое разложение карбоната кальция с тепловым эффектом -179 кДж привело к получению 33,6 г твердого остатка. В этих условиях поглощенное количество теплоты (кДж) равно
1) -537
2) -214,8
3) -375,9
4) -107,4
6. При термическом разложении дихромата аммония протекает экзотермическая реакция, в которой на 1,4 моль образовавшейся воды приходится +106 кДж; следовательно тепловой эффект реакции (кДж) равен:
1) +505
2) +404
3) +303
4) +606
7. Реакция сгорания угарного газа в кислороде сопровождается экзо-эффектом +566 кДж. Количество теплоты (кДж), приходящееся на 224 г угарного газа, равно
1) +1132
2) +2264
3) +283
4) +566
8. Тепловой эффект реакции полного сгорания ацетилена в кислороде равен +2596 кДж. При сгорании 2 л (н.у.) этого газа выделяется количество теплоты (кДж)
1) +29
2) +58
3) +116
4) +232
9. В термическом разложении метана с образованием ацетилена и 560 л (н.у.) водорода тепловой эффект реакции равен -376 кДж. Количество поглощенной теплоты (кДж) в условиях опыта составляет
1) -2256
2) -752
3) -1128
4) -376
10. При полном сгорании бутадиена-1,3 в кислороде на 0,5 моль затраченного окислителя выделяется +18 кДж теплоты, следовательно, на 0,5 моль вступившего в реакцию алкадиена приходится количество теплоты (кДж), равное
1) +49,5
2) +99
3) +148,5
4) +198
15.5. Масса (объем, количество вещества) продукта по реагенту в избытке или с примесями
Избыток и недостаток реагентов.Количества, массы и объемы (для газов) реагентов не всегда берутся стехиометрическими, т. е. в соответствии с уравнениями реакции. Чаще один из реагентов берется в избытке, а следовательно, другой реагент оказывается в недостатке. Избыток реагента участвовать в реакции не будет.
Для реакции a A + b B = c C + d D определение реагентов, взятых в избыткеи в недостатке, проводят по неравенству (А – в недостатке, В – в избытке):
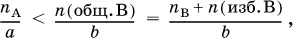
где n (общ. В) – общее (взятое с избытком) количество реагента В, п B– стехиометрическое (необходимое для реакции) количество В, n (изб. В) – избыточное количество В, причем
Внимание!Расчет получаемых количеств (масс, объемов) продуктов проводят по реагенту в недостатке.
Степень чистоты вещества.Химические вещества никогда не бывают идеально чистыми, они всегда содержат в себе примеси.
Читать дальшеИнтервал:
Закладка:










