Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
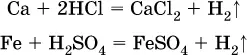
Исключения:металлы Ti и Sn реагируют только с НCl (конц.):
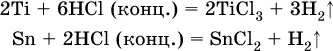
и не реагируют с H 2SO 4(разб.). Металл Pb, восстановительная активность которого почти равна таковой для водорода, не реагирует с НCl (разб., конц.) и H 2SO 4(разб.).
Металлы, стоящие в ряду напряжений правееводорода – Cu, Hg, Ag, Pt и Au, в принципе не вступают во взаимодействие с НCl и H 2SO 4(разб.) и не вытесняют из них водорода.
Внимание!Из распространенных кислот в реакции с вытеснением водорода не вступают азотная кислота HNO 3(ни концентрированная, ни разбавленная) и серная кислота H 2SO 4(конц.);
3) будет ли протекать реакция замещения между металлом и сольюдругого металла в ее растворе; чем левее находится металл в ряду напряжений, тем легче он переходит в состояние катиона и восстанавливает все металлы, стоящие справа от него(положение металлов относительно водорода не имеет значения). Так, Fe вытесняет металлы Cd – Au (по ряду слева направо) из растворов их солей.
Примеры:
а)
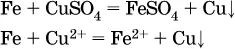
б)
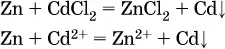
в)
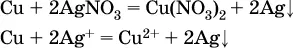
В этих реакциях не используют металлы Li – Na (левая часть ряда), которые будут реагировать не с солями других металлов в растворе, а с водой.
14.4. Электролиз расплава и раствора
Электролизом называется окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через растворы или расплавы электролитов.
На отрицательно заряженном электроде — катоде происходит электрохимическое восстановлениечастиц (атомов, молекул, катионов), а на положительно заряженном электроде — аноде идет электрохимическое окислениечастиц (атомов, молекул, анионов).
Примеры электролиза расплавов:
а)
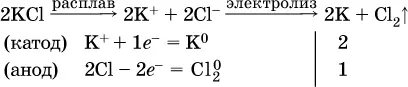
б)
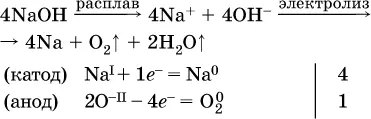
Электролиз воды проводится всегда в присутствии инертногоэлектролита (для увеличения электропроводности очень слабого электролита – воды):
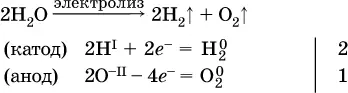
В зависимости от инертного электролита электролиз проводится в нейтральной, кислотной или щелочной среде (например, в присутствии K 2SO 4, H 2SO 4или КОН).
При выборе инертного электролита необходимо учесть, что никогда не восстанавливаются на катоде в водном растворе катионы металлов, являющихся типичными восстановителями (например, Li +, К +, Са 2+, Na +, Mg 2+, Al 3+), и никогда не окисляется на аноде кислород О -IIанионов оксокислот с элементом в высшей степени окисления (например, ClO 4 -, SO 4 2-, NO 3 -, РО 4 3-, CO 3 2-); вместо них окисляется вода.
Примеры электролиза растворов солей:
а)
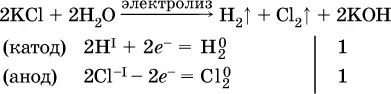
(на аноде окисляются анионы Cl -, а не кислород О -IIмолекул Н 2O, так как электроотрицательность хлора меньше, чем у кислорода, и следовательно, хлор отдает электроны легче, чем кислород);
б)
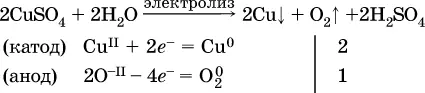
(на катоде восстанавливаются катионы Cu 2+, а не водород Н Iмолекул Н 2O, так как медь стоит правее водорода в ряду напряжений, т. е. легче принимает электроны, чем Н Iв воде; подробнее см. 5.3).
Подчеркнем еще раз, что электролиз – это окислительно-восстановительная реакция, которая протекает под действием и при участии электрического тока. Уравнения электрохимических реакций отражают те процессы, которые без помощи электрического тока протекать не могут.
1. В уравнении реакции
CuS + HNO 3(конц.) → CuSO 4+ NO 2↑ +… коэффициент у формулы окислителя равен
1) 1
2) 4
3) 8
4) 11
2. В уравнении реакции
К 2Cr 2O 7+ НCl → CrCl 3+ Cl 2↑ +… коэффициент у формулы восстановителя – это
1) 14
2) 10
3) 6
4) 2
3―4. В уравнении реакции
3. Al + V 2O 5→ Al 2O 3+ V
4. MgC 2+ Cl 2→ MgCl 2+ СCl 4
сумма коэффициентов равна
1) 8
2) 13
3) 18
4) 24
5—6. В уравнении реакции
5. КMnО 4+ Н 2O + K 2SO 4→ MnO 2↓ + K 2SO 4+ KOH
6. KI + H 2O + Cl 2→ KIO 3+ HCl
сумма коэффициентов равна
1) 9
2) 10
3) 13
4) 14
7. Укажите соответствие между веществом (формула подчеркнута) и его функцией в реакции.
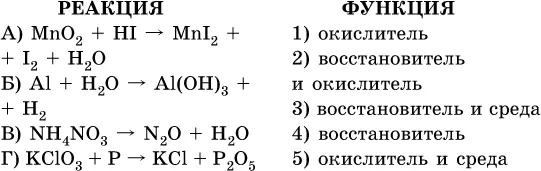
8. При электролизе расплава смеси гидроксида и хлорида калия набор продуктов на электродах – это
1) Н 2, O 2
2) К, O 2
3) K, Cl 2
4) Н 2, Cl 2
9. При электролизе раствора нитрата ртути (II) набор продуктов на электродах – это
1) Hg, O 2
2) H 2, O 2
3) Hg, N 2
4) H 2, N 2
10. Установите соответствие между веществом и продуктом, образующимся на катоде при электролизе раствора

11. Установите соответствие между веществом и продуктом, образующимся на аноде при электролизе раствора

12—14. Используя метод электронного баланса, составьте уравнение реакции по указанной схеме. Определите окислитель и восстановитель.
12. Mn(NO 3) 2+ HNO 3+ РЬO 2 → HMnO 4+ Pb(NO 3) 2+…
13. Zn + H 2SO 4+ HNO 3(разб.) → ZnSO 4+ NO +…
14. K 2Cr 2O 7+ HCl + C 2H 5OH → CrCl 3+ CH 3C(H)O +…
15. Решение расчетных задач
15.1. Массовая доля растворенного вещества. Разбавление, концентрирование и смешивание растворов
Массовая доля растворенного вещества В
(ω в) – это отношение массы вещества В ( т в) к массе раствора ( m (р)):
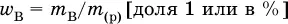
При решении ω ввыражается всегда в долях единицы (например, ω в = 0,01), в ответе – часто в процентах ( ω в=1 %).
Читать дальшеИнтервал:
Закладка:










