Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
И протекторы, и катодная защита применимы в средах, хорошо проводящих электрический ток, например в морской воде. В частности, протекторы широко применяются для защиты подводных частей морских судов. Ясно, что убытки, вызванные коррозией корпуса морского судна и связанные с его простоем и ремонтом, очень велики и во много раз превышают стоимость протекторов,
Глава XVII. ПЕРВАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
Металлы главной подгруппы первой группы — литий, натрий, калий, рубидий, цезий и франций — называются щелочными металлами. Это название связано с тем, что гидроксиды двух главных представителей этой группы — натрия и калия — издавна были известны под названием щелочей. Из этих щелочей, подвергая их в расплавленном состоянии электролизу, Г. Дэви в 1807 г. впервые получил свободные калий и натрий.
Во внешнем электронном слое атомы щелочных металлов имеют по одному электрону. Во втором снаружи электронном слое у атома лития содержатся два электрона, а у атомов остальных щелочных металлов — по восемь электронов.
Таблица 30. Некоторые свойства щелочных металлов
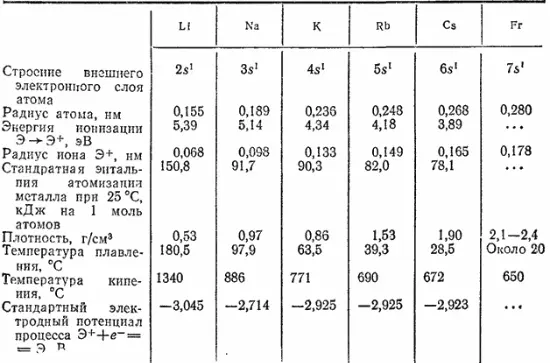
Имея во внешнем электронном слое только по одному электрону, находящемуся на сравнительно большом удалении от ядра, атомы этих элементов довольно легко отдают этот электрон, т. е. характеризуются низкой энергией ионизации (табл. 30). Образующиеся при этом однозарядные положительные ионы имеют устойчивую электронную структуру соответствующего благородного газа (ион лития — структуру атома гелия, ион натрия — атома неона и т. д.). Легкость отдачи внешних электронов характеризует рассматриваемые элементы как наиболее типичные представители металлов: металлические свойства выражены у щелочных металлов особенно резко.
Одинаковое строение не только наружного, но и предпоследнего электронного слоя атомов всех щелочных металлов, кроме лития, обусловливает большое сходство свойств этих элементов. В то же время увеличение заряда ядра и общего числа электронов в атоме при переходе сверху вниз по подгруппе создает некоторые различия в их свойствах. Как и в других группах, эти различия проявляются главным образом в увеличении легкости отдачи валентных электронов и усилении металлических свойств с возрастанием порядкового номера.
197. Щелочные металлы в природе. Получение и свойства щелочных металлов.
Вследствие очень легкой окисляемости щелочные металлы встречаются в природе исключительно в виде соединений. Натрий и калий принадлежат к распространенным элементам: содержание каждого из них в земной коре равно приблизительно 2% (масс.). Оба металла входят в состав различных минералов и горных пород силикатного типа. Хлорид натрия содержится в морской воде, а также образует мощные отложения каменной соли во многих местах земного шара. В верхних слоях этих отложений иногда содержатся довольно значительные количества калия, преимущественно в виде хлорида или двойных солей с натрием и магнием. Однако большие скопления солей калия, имеющие промышленное значение, встречаются редко. Наиболее важными из них являются соликамские месторождения в СССР, страссфуртские в ГДР и эльзасские — во Франции. Залежи натриевой селитры находятся в Чили. В воде многих озер содержится сода. Наконец, огромные количества сульфата натрия находятся в заливе Кара-Богас-Гол Каспийского моря, где эта соль в зимние месяцы толстым слоем осаждается на дне.
Значительно меньше, чем натрий и калий, распространены литий, рубидий и цезий. Чаще других встречается литий, но содержащие его минералы редко образуют большие скопления. Рубидий и цезий содержатся в небольших количествах в некоторых литиевых минералах.
Все известные изотопы франция радиоактивны и быстро распадаются. Первым был открыт изотоп 223Fr; его существование было установлено французской исследовательницей М. Пере в 1939 г.
- 545 -
Он образуется при распаде актиния и в ничтожном количестве встречается в природе. В настоящее время небольшие количества франция получают искусственно.
Натрий и литии получают электролизом расплавов их соединений, калий — восстановлением из расплавов КОН или КСl натрием, рубидий и цезий — восстановлением из их хлоридов кальцием.
Все щелочные металлы кристаллизуются в кубической объем-ноцентрированной решетке. Они обладают металлическим блеском, который можно наблюдать на свежем разрезе металла. На воздухе блестящая поверхность металла сейчас же тускнеет вследствие окисления.
Щелочные металлы характеризуются незначительной твердостью, малой плотностью и низкими температурами плавления и кипения. Наименьшую плотность имеет литий, самую низкую температуру плавления — франций (см.табл. 30).
Приведенные в табл. 30 данные показывают, что в большинстве случаев свойства щелочных металлов закономерно изменяются при переходе от лития к цезию. В основе наблюдающихся закономерностей лежит возрастание массы и радиуса атома в подгруппе сверху вниз. Рост массы приводит к возрастанию плотности. Увеличение радиуса обусловливает ослабление сил притяжения между атомами, что объясняет снижение температур плавления и кипения и уменьшение энергии атомизации металлов, а также уменьшение энергии ионизации атомов при переходе от лития к цезию. Однако стандартные электродные потенциалы щелочных металлов изменяются в ряду Li - Cs не так правильно. Причина этого, подробно рассмотренная в § 100, заключается в том, что величины электродных потенциалов связаны с несколькими факторами, различно изменяющимися при переходе от одного элемента подгруппы к другому.
Щелочные металлы принадлежат к числу наиболее активных в химическом отношении элементов. Их высокая химическая активность обусловлена в первую очередь низкими значениями энергии ионизации их атомов — легкостью отдачи ими валентных электронов. При этом энергия ионизации уменьшается при переходе от лития к цезию (табл. 30). Ясно, что химическая активность при этом возрастает.
Все щелочные металлы энергично соединяются с кислородом. Рубидий и цезий самовоспламеняются на воздухе; литий, натрий и калий загораются при небольшом нагревании. Характерно, что только литий, сгорая, образует нормальный оксид Li 2O, остальные же щелочные металлы превращаются в пероксидные соединения: Na 2O 2, KO 2, RbO 2, CsO 2.
Не менее энергично, чем с кислородом, взаимодействуют щелочные металлы с галогенами, особенно с хлором и фтором.
- 546 -
В ряду напряжений щелочные металлы стоят далеко впереди водорода и вытесняют водород из воды; при этом образуются сильные основания, например:
Читать дальшеИнтервал:
Закладка:








