Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
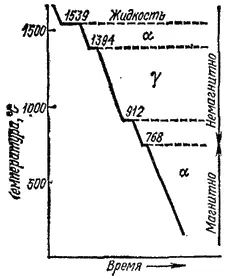
Рис. 167. Кривая охлаждения железа.
При температурах ниже 912 и выше 1394°C энергия Гиббса α-железа меньше энергии Гиббса γ-железа, а в интервале 912-1394°C больше.
Температуры фазовых превращений железа хорошо видны на кривой охлаждения в виде остановок — горизонтальных площадок (см. рис. 167). Как видно, кроме площадок, отвечающих перечисленным точкам, на кривой охлаждения имеется еще одна остановка — при 768°C. Эта температура связана не с перестройкой решетки, а с изменением магнитных свойств α-железа. При температурах выше 768°C железо немагнитно, а ниже 768°C — магнитно. Немагнитное α-железо иногда называют β-железом, а модификацию α-железа, устойчивую при температурах от 1392°C до плавления, — δ-железом.
Железо — серебристый пластичный металл. Оно хорошо поддается ковке, прокатке и другим видам механической обработки. Механические свойства железа сильно зависят от его чистоты — от содержания в нем даже весьма малых количеств других элементов.
Твердое железо обладает способностью растворять в себе многие элементы. В частности, растворяется в железе и углерод. Его растворимость сильно зависит от кристаллической модификации железа и от температуры. В α-железе углерод растворяется очень незначительно, в γ-железе — гораздо лучше. Раствор в γ-железе термодинамически устойчив в более широком интервале температур, чем чистое γ-железо. Твердый раствор углерода в α-железе называется ферритом, твердый раствор углерода в γ-железе - аустенитом.
Содержанию в железе 6,67% (масс.) углерода отвечает химическое соединение — карбид железа, или цементит, Fe 3C.
- 654 -
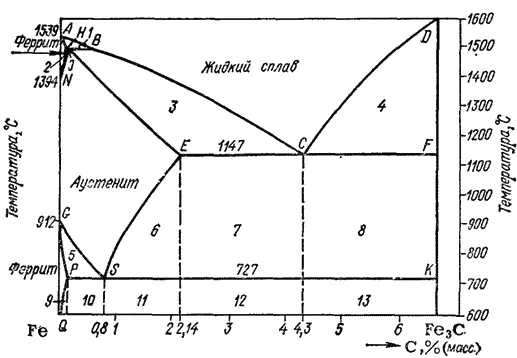
Рис. 168. Диаграмма состояния системы железо — углерод.
Это вещество имеет сложную кристаллическую структуру и характеризуется высокой твердостью (близка к твердости алмаза) и хрупкостью. При температуре около 1600°C цементит плавится.
Механические свойства феррита и аустенита зависят от содержания в них углерода. Однако при всех концентрациях углерода феррит и аустенит менее тверды и более пластичны, чем цементит.
Диаграмма состояния системы железо — углерод, дающая представление о строении железоуглеродных сплавов, имеет очень большое значение. С ее помощью можно объяснить зависимость свойств сталей и чугунов от содержания в них углерода и от термической обработки. Она служит основой при выборе железоуглеродных сплавов, обладающих теми или иными заданными свойствами. На рис. 168 приведена часть диаграммы состояния системы Fe-C, отвечающая содержанию углерода от 0 до 6.67%, или, что то же самое, от чистого железа до карбида Fe 3C. Это самая важная часть диаграммы, поскольку практическое применение имеют сплавы железа, содержащие не более 5% углерода.
Диаграмма состояния системы Fe-C сложнее, чем рассмотренные в главе XVI основные типы диаграмм состояния металлических систем. Однако все ее точки, кривые и области подобны тем, которые были описаны в § 195. Особенности ее обусловлены уже упомянутыми обстоятельствами: существованием двух модификаций кристаллического железа, способностью обеих этих модификаций образовывать твердые растворы с углеродом, способностью железа вступать в химическое соединение с углеродом, образуй цементит.
- 655 -
Левая ось диаграммы соответствует чистому железу, правая — карбиду Fe 3C(цементиту). Точки А и D показывают температуру плавления железа и карбида, точки G и N — температуры превращений α и γ-железа друг в друга.
Линия ABCD — это кривая температур начала кристаллизации жидких сплавов, линия AHJECF — кривая температур начала плавления твердых сплавов. Все линии, лежащие ниже последней кривой, отвечают равновесиям между твердыми фазами.
Область, лежащая выше линии ABCD, отвечает жидкому сплаву. Области, примыкающие к левой вертикали, соответствуют твердым растворам углерода в железе: линия AHN ограничивает область твердого раствора углерода в α-железе при высоких температурах (область высокотемпературного феррита), линия NJESG ограничивает область твердого раствора углерода в γ-железе (область аустенита), линия GPQ — область твердого раствора углерода в α-железе при низких температурах (область низкотемпературного феррита). Перечисленным областям соответствуют гомогенные системы: структура как расплава, так и твердых растворов однородна в каждой из этих фаз.
Остальным областям диаграммы отвечают гетерогенные системы — смеси кристаллов двух фаз или кристаллов и расплава.
Рассмотрим важнейшие превращения, происходящие при медленном охлаждении расплавов различных концентраций. Это поможет нам разобраться в том, какие сплавы соответствуют областям гетерогенности диаграммы.
Пусть мы имеем расплав, содержащий 0.8% углерода. Его кристаллизация начнется в точке 1 (рис. 169). При охлаждении расплава до температуры, отвечающей этой точке, будут выпадать кристаллы аустенита; их состав отвечает точке 2. Расплав при этом обогащается углеродом, и его состав изменяется по линии ВС. Состав кристаллов в процессе кристаллизации изменяется по кривой JE. Когда состав кристаллов достигнет точки 3, кристаллизация закончится. Как всегда при образовании твердого раствора, одновременно идет процесс диффузии в твердой фазе, в результата чего при медленном охлаждении состав всех кристаллов получается одинаковым.
Далее, образовавшийся аустенит охлаждается без превращения до точки S (рис. 168). Эта точка (температура 727°C) показывает минимальную температуру устойчивого существования аустенита. При 272°C происходит его эвтектоидный распад. Образующийся эвтектоид состоит из чередующихся мелких пластинок феррита и цементита.
- 656 -
На изломе он при рассматривании под микроскопом напоминает перламутр. Поэтому эта структура — эвтектоидная смесь феррита и цементита — получила название перлит.
Если исходный расплав содержит не 0.8% углерода, а несколько меньше, например 0.7%, то образующийся при кристаллизации аустенит начнет распадаться не при 727°C, а при более высокой температуре (точка 1 на рис. 170). Превращение начнется с выделения кристаллов феррита (точка 2 на рис. 170), содержание углерода в котором очень мало. Вследствие этого остающийся аустенит обогащается углеродом и при дальнейшем охлаждении его состав изменяется по кривой GS. По достижении точки S начинается эвтектоидное превращение при постоянной температуре, по окончании которого сталь будет состоять из феррита и перлита. Из сказанного вытекает, что области 3 на диаграмме (см. рис. 168) соответствует смесь жидкого сплава с кристаллами аустенита, области 5 — смесь кристаллов феррита и аустенита и области 10 — смесь перлита с кристаллами феррита.
Читать дальшеИнтервал:
Закладка:








