Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Вступая в окислительно-восстановительные реакции, KMnO 4(ион MnO 4 -) может восстанавливаться в различной степени. В зависимости от pH среды продукт восстановления может представлять собою ион Mn 2+(в кислой среде), MnO 2(в нейтральной или в слабощелочной среде) или ион MnO 4 2-(в сильнощелочной среде).
Проиллюстрируем эти три случая реакциями взаимодействия KMnO 4с растворимыми сульфитами. Если к подкисленному серной кислотой фиолетовому раствору KMnO 4прибавить сульфит калия K 2SO 3, то жидкость становится почти бесцветной, так как образующаяся соль марганца (II) имеет бледно-розовую окраску. Реакция выражается уравнением

или в ионно-молекулярной форме:
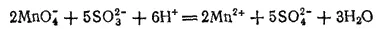
- 645 -
При действии сульфита калия на нейтральный раствор перманганата калия тоже происходит обесцвечивание раствора, но, кроме того, выпадает бурый осадок диоксида марганца и раствор приобретает щелочную реакцию
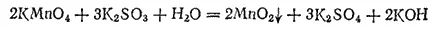
или в ионно-молекулярной форме:
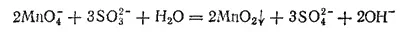
При большой концентрации щелочи и малом количестве восстановителя образуются ионы манганата согласно уравнению:
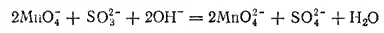
Как энергичный окислитель перманганат калия широко применяют в химических лабораториях и производствах; он служит также прекрасным дезинфицирующим средством.
При нагревании в сухом виде перманганат калия уже при температуре около 200°C разлагается согласно уравнению:
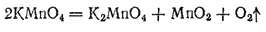
Этой реакцией иногда пользуются в лаборатории для получения кислорода.
Соответствующая перманганатам свободная марганцовая кислота HMnO 4в безводном состоянии не получена и известна только в растворе. Концентрацию ее раствора можно довести до 20%. Это очень сильная кислота, в водном растворе полностью диссоциированная на ионы: ее кажущаяся степень диссоциации в 0,1 н. растворе равна 93%.
Оксид марганца (VII), или марганцовый ангидрид, Mn 2O 7может быть получен действием концентрированной серной кислоты на перманганат калия:
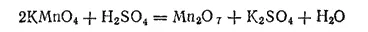
Марганцовый ангидрид — зеленовато-бурая маслянистая жидкость. Он очень неустойчив: при нагревании или при соприкосновении с горючими веществами он со взрывом разлагается на диоксид марганца и кислород.
232. Рений (Rhenium).
Рений не образует самостоятельных минералов. В ничтожных количествах он содержится в молибденовых рудах и некоторых редких минералах. Общее содержание рения в земной коре составляет 0,0000001% (масс.).
Рений был открыт только в 1925 г., однако существование его было предсказано еще в 1871 г. Менделеевым, который назвал его двимарганцем.
В свободном состоянии рений — светло-серый металл. Плотность его равна 21,0 г/см 3, температура плавления около 3190°C.
- 646 -
Он не растворяется в соляной и в плавиковой кислотах, азотная и горячая концентрированная серная кислоты растворяют его с образованием рениевой кислоты HReO 4.
Рений и его сплавы с вольфрамом и молибденом применяются в производстве электрических ламп и электровакуумных приборов; они имеют больший срок службы и являются более прочными, чем вольфрам. Из сплавов вольфрама с рением изготовляют термопары, которые можно использовать в интервале температур от 0 до 2500°C. Жаропрочные и тугоплавкие сплавы рения с вольфрамом, молибденом, танталом применяются для изготовления некоторых ответственных деталей. Рений и его соединения служат катализаторами при окислении аммиака, окислении метана, гидрировании этилена.
Рений образует несколько оксидов, из которых наиболее стойким и характерным для рения является оксид рения (VII), или рениевый ангидрид, Re 2O 7(желтовато-бурые пластинки). При взаимодействии его с водой получается бесцветный раствор рениевой кислоты HReO 4, соли которой называются перренатами. В отличие от марганцовой кислоты и ее солей, окислительные свойства для рениевой кислоты и перренатов не характерны.
Глава XXII. ВОСЬМАЯ ГРУППА ПЕРИОДИЧЕСКОЙ СИСТЕМЫ
БЛАГОРОДНЫЕ ГАЗЫ
233. Общая характеристика благородных газов.
Главную подгруппу восьмой группы периодической системы составляют благородные газы — гелий, неон, аргон, криптон, ксенон и радон. Эти элементы характеризуются очень низкой химической активностью, что и дало основание назвать их благородными, или инертными, газами. Они лишь с трудом образуют соединения с другими элементами или веществами; химические соединения гелия, неона и аргона не получены. Атомы благородных газов не соединены в молекулы, иначе говоря, их молекулы одноатомны.
Благородные газы заканчивают собой каждый период системы элементов. Кроме гелия, все они имеют в наружном электронном слое атома восемь электронов, образующих очень устойчивую систему. Также устойчива и электронная оболочка гелия, состоящая из двух электронов. Поэтому атомы благородных газов характеризуются высокими значениями энергии ионизации и, как правило, отрицательными значениями энергии сродства к электрону.
В табл. 38 приведены некоторые свойства благородных газов, а также их содержание в воздухе. Видно, что температуры сжижения и затвердевания благородных газов тем ниже, чем меньше их атомные массы или порядковые номера: самая низкая температура сжижения у гелия, самая высокая — у радона.
- 647 -
Таблица 38. Некоторые свойства благородных газов и их содержание в воздухе

До конца XIX века полагали, что воздух состоит только из кислорода и азота. Но в 1894 г. английский физик Дж. Рэлей установил, что плотность азота, полученного из воздуха (1,2572 г/л ), несколько больше, чем плотность азота, полученного из его соединений (1,2505 г/л ). Профессор химии У. Рамзай предположил, что разница в плотности вызвана присутствием в атмосферном азоте примеси какого-то более тяжелого газа. Связывая азот с раскаленным магнием (Рамзай) или вызывая действием электрического разряда его соединение с кислородом (Рэлей), оба ученых выделили из атмосферного азота небольшие количества химически инертного газа. Так был открыт неизвестный до того времени элемент, названный аргоном. Вслед за аргоном были выделены гелий, неон, криптон и ксенон, содержащиеся в воздухе в ничтожных количествах. Последний элемент подгруппы — радон — был открыт при изучении радиоактивных превращений.
Читать дальшеИнтервал:
Закладка:








