Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Рис. 61. Кристаллические решетки хлорида натрия (а) и хлорида цезия (б).
- 155 -
В кристаллах обеих этих солей, а также других ионных соединений все связи каждого иона с ближайшими ионами противоположного знака равноценны. Отсюда следует, что понятие о молекуле неприменимо к кристаллическим веществам с ионной связью. Также неприменимо это понятие и к кристаллам с атомной или смешанной атомно-ионной структурой. В таких веществах, как алмаз, карборунд SiC, имеющих атомную решетку, или как ZnS, Al 2O 3обладающих промежуточной атомно-ионной структурой, все связи каждого атома с ближайшими соседними атомами равноценны.
51. Реальные кристаллы.
Описанная в § 50 внутренняя структура кристалла, характеризующаяся строгой пространственной периодичностью, представляет собой известную идеализацию. Исследование строения реальных кристаллов показало, что во всяком кристалле эта периодичность всегда несколько нарушена. В реальных кристаллах наблюдаются дефекты структуры. Число этих дефектов и их тип оказывают влияние на некоторые свойства кристаллических веществ. В ряде случаев это влияние очень сильно, а некоторых из таких структурно-чувствительных свойств имеют очень большое практическое значение.
Дефекты структуры реальных кристаллов разнообразны. Прежде всего различают точечные, линейные и поверхностные дефекты. Простейшие и в то же время важнейшие точечные дефекты — это незанятые узлы решетки, или вакансии, и атомы, находящиеся в междуузлиях. Существование таких дефектов связано с тем, что отдельные атомы или ионы решетки имеют энергию, превышающую ее среднее значение при данной температуре. Такие атомы колеблются интенсивнее других и могут переместиться с одного места на другое, например, из узла решетки в междуузлие. Вышедший из узла атом называется дислоцированным, а незаполненное место, где он ранее находился, — вакансией. В любой момент соседний с вакансией атом может перейти на ее место, освободив новую вакансию. Таким образом, вакансии переходят с одного места на другое. Точечные дефекты оказывают очень большое влияние на свойства полупроводниковых материалов.
Линейные дефекты структуры называются дислокациями. Простейший вид дислокации — краевая дислокация. Она представляет собой край одной из атомных плоскостей, обрывающейся внутри кристалла. Дислокации возникают как в процессе роста кристаллов, так и при местных механических, тепловых и других воздействиях на кристаллы (см., например, рис. 142, а, б на стр 521). На рис. 62 изображена краевая дислокация (линия АВ), возникшая в результате сдвига части кристалла по плоскости ABCD в направлении, указанном стрелкой.
Подобно точечным дефектам, дислокации подвижны. Их подвижность особенно велика в случае металлических кристаллов.
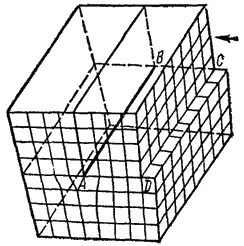
Рис. 62. Схема краевой дислокации.
Механические свойства металлов сильно зависят от плотности дислокаций (т. е. от числа в единице объема) и от их способности к перемещению по кристаллу (см. стр. 520, 521).
Поверхностные дефекты, наблюдаемые на поверхности кристаллического тела или на границе кристаллов между собою, представляют комбинации большого числа различных точечных и линейных дефектов.
52. Аморфное состояние вещества.
Среди твердых тел встречаются такие, в изломе которых нельзя обнаружить никаких признаков кристаллов. Например, если расколоть кусок обыкновенного стекла, то излом его окажется гладким и, в отличие от изломов кристаллов, ограничен не плоскими, а овальными поверхностями. Подобная же картина наблюдается при раскалывании кусков смолы, клея и некоторых других веществ. Такое состояние вещества называют аморфным.
Различие между кристаллическими и аморфными телами особенно резко проявляется в их отношении к нагреванию. В то время как кристаллы каждого вещества плавятся при строго определенной температуре и при той же температуре происходит переход из жидкого состояния в твердое, аморфные тела не имеют определенной температуры плавления. При нагревании аморфное тело постепенно размягчается, начинает растекаться и, наконец, становится совсем жидким. При охлаждении оно также постепенно затвердевает.
В связи с отсутствием определенной температуры плавления аморфные тела обладают и другой особенностью: многие из них подобно жидкостям текучи, т. е. при длительном действии сравнительно небольших сил постепенно изменяют свою форму. Например, кусок смолы, положенный на плоскую поверхность, в теплом помещении за несколько недель растекается, принимая форму диска.
В отношении внутреннего строения различие между кристаллическим и аморфным состояниями вещества состоит в следующем. Упорядоченное расположение частиц в кристалле, отражаемое элементарной ячейкой, сохраняется на больших участках кристаллов, а в случае хорошо образованных кристаллов — во всем их объеме. В аморфных телах упорядоченность в расположении частиц наблюдается только на очень малых участках. Кроме того, в ряде аморфных тел даже эта местная упорядоченность носит лишь приблизительный характер.
Это различие можно коротко сформулировать следующим образом: структура кристаллов характеризуется дальним порядком, структура аморфных тел — ближним.
Аморфное состояние характерно, например, для силикатных стекол (§ 182). Некоторые вещества могут находиться как в кристаллическом, так и в аморфном состоянии. Например, диоксид кремния SiO 2встречается в природе в виде хорошо образованных кристаллов кварца, а также в аморфном состоянии (минерал кремень). При этом кристаллическое состояние всегда более устойчиво. Поэтому самопроизвольный переход вещества из кристаллического состояния в аморфное невозможен, а обратное превращение— самопроизвольный переход из аморфного состояния в кристаллическое — возможно и иногда наблюдается. Примером такого превращения служит расстеклование — самопроизвольная кристаллизация стекла при повышенных температурах, сопровождающаяся разрушением его.
53. Жидкости.
Жидкое состояние является промежуточным между газообразным и кристаллическим. По одним свойствам жидкости близки к газам, по другим — к твердым телам. С газами жидкости сближает прежде всего их изотропность и текучесть; последняя обусловливает способность жидкости легко изменять внешнюю форму. Однако высокая плотность и малая сжимаемость жидкостей приближает их к твердым телам.
Способность жидкостей легко изменять свою форму говорит об отсутствии в них жестких сил межмолекулярного взаимодействия. В то же время низкая сжимаемость жидкостей, обусловливающая способность сохранять постоянный при данной температуре объем, указывает на присутствие хотя и не жестких, но все же значительных сил взаимодействия между частицами.
Читать дальшеИнтервал:
Закладка:






