Эрик Роджерс - Физика для любознательных. Том 1. Материя. Движение. Сила
- Название:Физика для любознательных. Том 1. Материя. Движение. Сила
- Автор:
- Жанр:
- Издательство:Мир
- Год:1969
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Эрик Роджерс - Физика для любознательных. Том 1. Материя. Движение. Сила краткое содержание
Физика для любознательных. Том 1. Материя. Движение. Сила - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
По всей трубке вверх поднимается очень тонкий слой жидкости, возможно, толщиной в одну молекулу, а за ним ползет основная масса жидкости, образуя искривленный мениск. Силы F 1и F 2для случаев малого и большого краевого угла схематически изображены на фиг. 124.
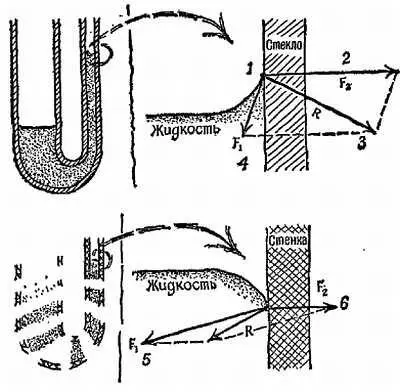
Фиг. 124. Молекулярные силы, краевой угол и капиллярность.
1— рассматриваемая молекула; 2— притяжение стекла; 3— равнодействующая сил притяжения; 4, 5— притяжение соседей в жидкости; 6— притяжение стенки.
Поверхность жидкости располагается перпендикулярно равнодействующей R сил притяжения, действующих на ее молекулы. Это является результатом короткодействующих сил, которые проявляются при столкновениях с другими молекулами. Когда краевой угол равен нулю, стеклянная стенка, вероятно, на всем протяжении покрыта тонким слоем жидкости толщиной в несколько молекул. Мениск всползает по этому слою жидкости.
Рисунки весьма упрощены, так как на них не учтена сила тяжести.
Вещества, облегчающие смачивание: мыла и моющие средства
Очень часто, когда нужен малый краевой угол, природа дает нам большой. Овечья шерсть, например, не смачивается водой; это мешает обработке отары растворами при дезинсекции. С обеденной посуды вода скатывается, как со спины утки, и даже на чайных стаканах порой остаются несмачиваемые отпечатки пальцев. А новые посудные полотенца, поступающие со склада с ужасной восковой отделкой! Нам необходимы молекулы-посредники, которые образовывали бы промежуточный слой и уменьшали бы краевой угол между водой и жирными тарелками, покрытыми воском волокнами одежды и т. д. Сейчас эту роль выполняют моющие средства, предшественником которых было мыло. Мыло действует на жир с помощью поверхностного натяжения, помогая воде заползать под жир и отрывать его частички, которые смываются в виде эмульсии (скопление мелких частиц жира, взвешенных в воде). Один конец молекулы мыла имеет сродство к воде вследствие химического или электрического притяжения [76] «Это высокий парень с жирной головой, который любит шлепать ногами по воде».
, а другой конец инертен к воде, но легко присоединяется к жиру. В то время как «жирные» концы образуют облако вокруг частиц жира, «водяные» концы выступают наружу и притягивают воду. Современные синтетические мыла или стиральные порошки обычно облегчают смачивание. Их молекулы действуют как посредники и уменьшают краевой угол. Они проникают в любую щель между жиром и тарелкой, облегчая попадание туда воды.
Вообразим себя в роли физиков-судомоек, которые приходят к группе химиков и говорят: «Пожалуйста, разработайте и пустите в производство вещество, которое было бы пригодно в качестве моющего средства. Оно должно иметь следующие свойства:
1) его молекулы должны притягиваться к жиру (или, для других целей, — к текстильным волокнам);
2) его молекулы должны также притягиваться к воде;
3) оно должно довольно легко растворяться в воде, чтобы его молекулы могли плавать и достигать границы вода/жир, где необходима их помощь.
P. S. Производство этого средства должно быть недорогим».
Современные химики-органики ответят: «Это легко сделать». Чтобы прицепиться к воску или к жиру, молекулы должны иметь длинную углеводородную цепь, подобную следующей [77] Химики обозначают атом водорода буквой Н, углерода буквой С и т. д. и соединяют их связями, чтобы показать, как построены молекулы. Подобные «картинки» основаны на химических экспериментах и рассуждениях; они полезны и заслуживают доверия.
»:
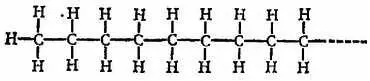
но не слишком длинную, иначе она не будет растворяться в воде.
Воски и жиры имеют аналогичную цепную структуру, и они должны притягивать такие цепи. Затем это вещество на одном из концов должно иметь нечто обладающее сродством к воде, например атом натрия. Годится любая группа, которая будет отделяться в воде, освобождая электрический заряд, поскольку молекулы воды несут на концах заряды + и — и будут скапливаться вокруг других зарядов.
Такого рода молекулы были сконструированы и изготовлены, и сейчас мы покупаем их в больших количествах в хозяйственных магазинах. Ниже приведены примеры обычного мыла и синтетического стирального порошка подобной структуры [78] В каждом случае атом натрия отделяется в воде в виде иона Na + . В результате остальная часть молекулы мыла приобретает отрицательный заряд и превращается в длинный отрицательный ион.
).
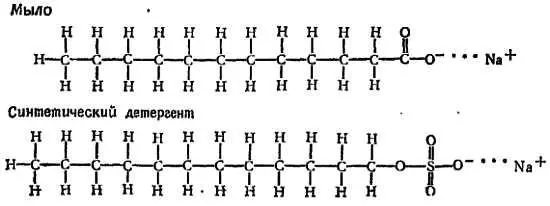
К числу таких веществ относится также применяемый в фотографии и исследовательской работе аэрозоль. Его молекула представляет собой длинную цепь с воскообразными концами и «притягивающим воду» атомом натрия в середине:
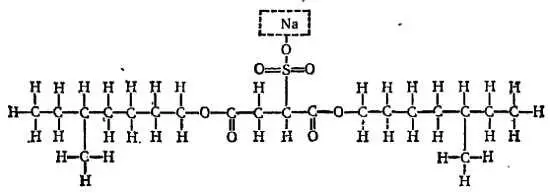
ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
Опыт 13.На покрытое воском стекло наносят каплю чистой воды (фиг. 125). Концом спички добавляют раствор моющего средства и следят за изменением краевого угла.
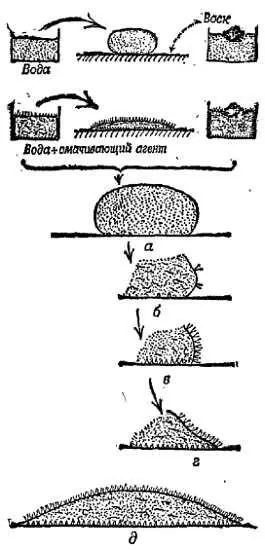
Фиг. 125. Действие смачивающего агента.
Длинные молекулы показаны линией с точкой, которая обозначает группу, имеющую сродство к воде. Молекулы смачивающего агента аэрозоля показаны не в масштабе, а увеличены во много раз. а— на столе, покрытом воском, образуется небольшая лужица; б— добавляется смачивающий агент; в— молекулы смачивающего агента собираются на поверхности инертными концами наружу; г— капля воды покрыта молекулами смачивающего агента и испытывает сильное притяжение к покрытому воском столу; д— краевой угол сильно уменьшается, и вода растекается по столу.
Опыт 14.Новое посудное полотенце с воскообразной поверхностью разрезают на два куска и растягивают на наклонном столе. На один кусок выливают крепкий раствор красителя. Краситель впитывается с трудом, большая его часть стекает. Затем на другой кусок выливают остаток красителя, к которому добавлено небольшое количество моющего средства.
Действие мыла и моющих средств. Когда раствор моющего средства попадает на покрытую воском поверхность, его молекулы скапливаются вокруг воска, причем их «жирные» концы направлены в сторону воска, а «водяные» — наружу. Эти внешние концы создают оболочку, которая притягивает воду, и этим облегчают смачивание. (Аэрозоль, молекула которого имеет удвоенную длину, прикрепляется к воску, жиру или целлюлозе обоими концами и поднимает имеющую сродство к воде середину, подобно выгнувшей спину гусенице; выпяченные «спины» создают притягивающую воду оболочку.)
Читать дальшеИнтервал:
Закладка:










