А. Березовчук - Физическая химия: конспект лекций
- Название:Физическая химия: конспект лекций
- Автор:
- Жанр:
- Издательство:Конспекты, шпаргалки, учебники «ЭКСМО»b4455b31-6e46-102c-b0cc-edc40df1930e
- Год:2009
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
А. Березовчук - Физическая химия: конспект лекций краткое содержание
Данное учебное пособие предназначено для студентов химических факультетов высших учебных заведений педагогического и технического направления. Изложены основные концепции и процессы, составляющие современную физическую химию. Материал соответствует государственному стандарту. Пособие рекомендовано в помощь студентам при подготовке к экзаменам.
Физическая химия: конспект лекций - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Березовчук А.В.
Физическая химия: конспект лекций
Введение
Физическая химия– наука, объясняющая химические явления и устанавливающая их закономерности на основе общих принципов физики.
Общая задача физической химии– предсказание временного хода химического процесса и конечного результата на основании данных о строении и свойствах молекул.
Термин «физическая химия» предложен М. В. Ломоносовым. Им же был прочитан первый курс по собственной книге «Введение в физическую химию». В 1860 г. Н. Н. Бекетов впервые вводит физическую химию в качестве особой учебной дисциплины, читает курс лекций в Харьковском университете, создает кафедру физической химии. В 1887 г. В. Оствальд в Лейпцигском университете организует кафедру физической химии. Он же выпускает первое периодическое издание по физической химии. Годом ранее И. А. Каблуков читает курс в Московском университете. К концу XIX в. определились три основных раздела физической химии: химическая термодинамика, химическая кинетика и электрохимия.
В настоящее время физическая химия полностью сформировалась как наука, включающая в себя химическую термодинамику (термохимию, фазовое равновесие), дополняющую химическую кинетику катализом, а также создала разнообразные физико-химические методы анализа.
ЛЕКЦИЯ № 1. Идеальный газ. Уравнение состояния реального газа
1. Элементы молекулярно-кинетической теории
Науке известно четыре вида агрегатных состояний вещества: твердое тело, жидкость, газ, плазма. Переход вещества из одного состояния в другое называют фазовым переходом.Вода, как известно, существует в трех агрегатных состояниях: в жидком (вода), твердом (лед), газообразном (пар). Это различие между тремя агрегатными состояниями определяется межмолекулярным взаимодействием и степенью сближения молекул.
Газ– агрегатное состояние вещества, в котором молекулы движутся хаотически, расположены на большом расстоянии друг от друга. В твердыхтелах расстояния между частицами малы, сила притяжения соответствует силе отталкивания. Жидкость– агрегатное состояние, промежуточное между твердым и газообразным. В жидкости частицы расположены близко одна к другой и могут перемещаться друг относительно друга; жидкость, как и газ, не имеет определенной формы.
Каждое из этих состояний можно описать набором некоторых параметров: например, состояние газа достаточно полно описывается тремя параметрами: объем, давление, температура.
Комбинация трех параметров, достаточно легко измеряемых, уже с середины ХVII века, когда были созданы барометры и термометры, хорошо описывает состояние газовой системы. Именно поэтому изучение сложных многоатомных систем началось с газов. У истоков наук химии и физики стоял Р. Бойль.
2. Уравнение состояния идеального газа
Изучение эмпирических газовых законов (Р. Бойль, Ж. Гей-Люссак) постепенно привело к представлению об идеальном газе, поскольку обнаружилось, что давление данной массы любого газа при постоянной температуре обратно пропорционально объему, занимаемому этим газом, и термические коэффициенты давления и объема с высокой точностью совпадают для различных газов, составляя, по современным данным, 1/273 град –1. Придумав способ графического представления состояния газа в координатах «давление – объем», Б. Клапейрон получил объединенный газовый закон, связывающий все три параметра:
PV = BT ,
где коэффициент В зависит от вида газа и его массы.
Только через сорок лет Д. И. Менделеев придал этому уравнению более простой вид, записав его не для массы, а для единицы количества вещества, т. е. 1 кмоля.
PV = RT , (1)
где R – универсальная газовая постоянная.
Физический смысл универсальной газовой постоянной. R – работа расширения 1 кмоля идеального газа при нагревании на один градус, если давление не меняется. Для того, чтобы понять физический смысл R , представим себе, что газ находится в сосуде при постоянном давлении, и мы повысим его температуру на Δ T , тогда
PV 1 = RT 1, (2)
и
PV 2 = RT 2. (3)
Вычитая из (3) уравнение (2), получим
P ( V 2– V 1) = R ( T 2– T 1).
Если правая часть уравнения равна единице, т. е. мы нагрели газ на один градус, тогда
R = P Δ V
Поскольку P = F / S , а Δ V равно площади сосуда S , умноженной на высоту подъема его поршня Δ h , имеем
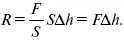
Очевидно, что справа получим выражение для работы, и это подтверждает физический смысл газовой постоянной.
3. Кинетическая теория газов
Очень плодотворным в середине XIX века оказалось представление о молекулярном строении вещества. Когда была принята гипотеза А. Авогадро о том, что в киломоле любого вещества содержится одно и то же количество структурных единиц: 6,02 x 10 26кмоля = 6,02 x 10 23моля, поскольку молярная масса воды M(H 2O) = 18 кг/кмоль , следовательно, в 18 литрах воды находится столько же молекул, сколько в 22,4 м 3водяного пара. Это позволяет легко понять, что расстояние между молекулами газообразной воды (пара) значительно больше, в среднем на один порядок, чем в жидкой воде. Можно предположить, что это выполняется для любого вещества. Считая, что в газах молекулы движутся хаотически, можно вывести так называемое основное уравнение кинетической теории:

где Na – 6,02 x 10 26кмоль = 6,02 x 10 23моль – число Авогадро;
V M – молекулярный объем = 22,4 м 3;
m – масса одной молекулы;
v – скорость молекулы.
Преобразуем уравнение (4):
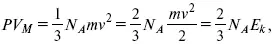
где E k – энергия одной молекулы.
Видно, что справа стоит полная кинетическая энергия всех молекул. С другой стороны, сравнивая с уравнением Менделеева – Клапейрона, видим, что это произведение равно RT.
Это позволяет выразить среднюю кинетическую энергию молекулы газа:
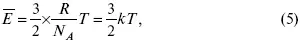
где к = R / Na – постоянная Больцмана, равная 1,38 ґ 10– 23кДж/кмоль. Зная кинетическую энергию молекулы, можно рассчитать ее среднюю скорость
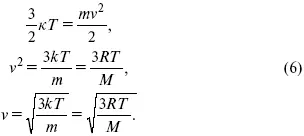
Около 1860 г. Д. К. Максвелл вывел функцию, описывающую распределение молекул газа по скоростям. Эта функция имеет на графике вид характерной кривой с максимумом около наиболее вероятной скорости примерно 500 м/с. Важно заметить, что существуют молекулы со скоростями, превышающими этот максимум. С другой стороны, уравнение (6) позволяет сделать вывод об увеличении доли молекул с большими скоростями при нагревании газа. Спустя почти 60 лет гениальная догадка Д. К. Максвелла была подтверждена в опытах О. Штерна .
Читать дальшеИнтервал:
Закладка:










