Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир
- Название:Абсолютный минимум. Как квантовая теория объясняет наш мир
- Автор:
- Жанр:
- Издательство:Питер
- Год:2015
- Город:Санкт-Петербург
- ISBN:978-5-496-01069-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир краткое содержание
Физика — это сложнейшая, комплексная наука, она насколько сложна, настолько и увлекательна. Если отбросить математическую составляющую, физика сразу становится доступной любому человеку, обладающему любопытством и воображением. Мы легко поймём концепцию теории гравитации, обойдясь без сложных математических уравнений. Поэтому всем, кто задумывается о том, что делает ягоды черники синими, а клубники — красными; кто сомневается, что звук распространяется в виде волн; кто интересуется, почему поведение света так отличается от любого другого явления во Вселенной, нужно понять, что всё дело — в квантовой физике. Эта книга представляет (и демистифицирует) для обычных людей волшебный мир квантовой науки, как ни одна другая книга. Она рассказывает о базовых научных понятиях, от световых частиц до состояний материи и причинах негативного влияния парниковых газов, раскрывая каждую тему без использования специфической научной терминологии — примерами из обычной повседневной жизни. Безусловно, книга по квантовой физике не может обойтись без минимального набора формул и уравнений, но это необходимый минимум, понятный большинству читателей. По мнению автора, книга, популяризирующая науку, должна быть доступной, но не опускаться до уровня читателя, а поднимать и развивать его интеллект и общий культурный уровень. Написанная в лучших традициях Стивена Хокинга и Льюиса Томаса, книга популяризирует увлекательные открытия из области квантовой физики и химии, сочетая представления и суждения современных учёных с яркими и наглядными примерами из повседневной жизни.
Абсолютный минимум. Как квантовая теория объясняет наш мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Как отмечалось в главе 11 и ранее в этой главе, углерод образует четыре связи. В метане он создаёт четыре электронные пары, совместно используемые с четырьмя атомами водорода. Каждый атом H вкладывает один электрон. Поэтому углерод должен иметь четыре неспаренных электрона для образования этих связей. Каждый неспаренный электрон углерода может объединиться с одним электроном водорода и образовать связывающую пару электронов. Чтобы иметь четыре неспаренных электрона, углерод «поднимает» 2 s -электрон на 2 p -орбиталь, как это показано в нижней части рис. 14.4. У изолированного атома углерода такая конфигурация не возникает, если только не передать ему значительное количество энергии. Для атома углерода перемещение 2 s -электрона на 2 p -орбиталь — это переход к конфигурации с повышенной энергией. Однако в случае, когда атомы образуют молекулы, электроны и ядра различных атомов влияют друг на друга. Представьте себе четыре атома H, приближающихся к атому C. Теперь система стремится перейти в низшее энергетическое состояние для всех пяти атомов. Образование четырёх связей уменьшает эту энергию сильнее, чем её повышает переход 2 s -электрона на 2 p -орбиталь.
Гибридные атомные орбитали: линейные молекулы
Итак, мы разобрались, каким образом углерод образует четыре связи, необходимые для молекулы метана. Но почему она имеет тетраэдрическую форму? Три 2 p -орбитали — это p x , p yи p z. Эти три орбитали перпендикулярны друг другу, то есть для любой их пары угол между ними составляет 90°. Если бы три атома H были связаны с 2 p -орбиталями, то угол между связями должен был составлять 90°. Далее, 2 s -орбиталь сферическая. 1 s -орбиталь четвёртого атома H должна была бы объединиться с углеродной 2 s -орбиталью. Если бы больше ничего не происходило, то ясно, что использование 2 s -орбитали и трёх 2 p -орбиталей углерода не привело бы к появлению у метана четырёх совершенно идентичных C−H-связей в тетраэдрической конфигурации. Кроме того, каким образом углерод образует треугольную молекулу формальдегида или линейную молекулу углекислого газа O=C=O? Во всех этих конфигурациях — тетраэдрической, треугольной и линейной — углеродные связи задействуют всё те же 2 s - и 2 p -орбитали.
В формальдегиде и углекислом газе имеются двойные связи, которых мы вскоре коснёмся. Чтобы разобраться в важных свойствах атомных орбиталей, которые могут придавать молекулам линейную, треугольную или тетраэдрическую форму, мы рассмотрим химические связи в гидриде бериллия BeH 2, бора́не BH 3и метане CH 4. Бериллий и бор в молекулах BeH 2и BH 3не имеют замкнутой оболочки, как у инертного газа неона, поэтому они химически очень активны. Создать эти молекулы можно, но они будут реагировать буквально со всем, с чем вступают в контакт, образуя новые молекулы, в которых Be и B имеют замкнутые конфигурации оболочек. Здесь мы рассматриваем их лишь как удобные примеры.
Бериллий имеет два электрона сверх замкнутой электронной конфигурации гелия. У отдельного атома эти два электрона спарены на 2 s -орбитали. Они являются валентными электронами бериллия. В молекуле BeH 2каждый атом H имеет по одному электрону на 1 s -орбитали. Чтобы бериллий образовал две пары электронных связей, по одной для каждого атома H, он должен поднять один из 2 s -электронов на 2 p -орбиталь, которую мы примем за 2 p z, как показано в верхней части рис. 14.5.
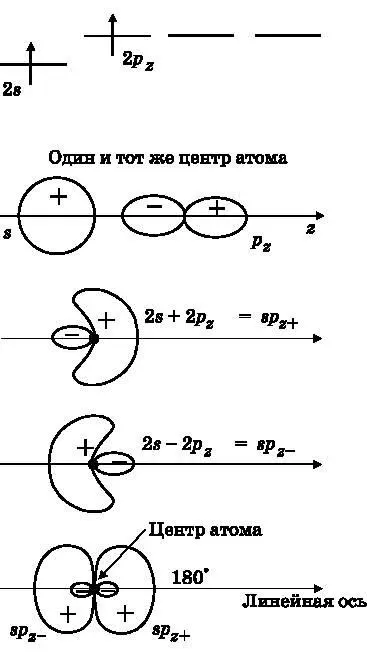
Рис. 14.5. Вверху: валентные электроны Be, один из которых перешёл на 2p z -орбиталь. Ниже: 2s- и 2p z -орбитали Be, показанные по отдельности. Ниже: сумма 2s- и 2p z -орбиталей даёт гибридную атомную орбиталь sp z + . Ниже: разность 2s и 2p z -орбиталей даёт гибридную орбиталь sp z− . Внизу: две гибридные орбитали бериллия направлены в противоположные стороны вдоль оси z
Ниже на этом рисунке 2 s- и 2 p z-орбитали схематически показаны по отдельности. В действительности они имеют общий центр, совпадающий с ядром Be. Эти орбитали являются волнами амплитуды вероятности электрона. Волны могут складываться и вычитаться, порождая новые волны. Начнём с двух атомных орбиталей — 2 s и 2 p z; далее путём сложения и вычитания получим две новые атомные орбитали, называемые гибридными орбиталями. Когда волны складываются, получаются области конструктивной и деструктивной интерференции, поскольку лепестки волн амплитуды вероятности имеют знак. На третьем сверху изображении на рис. 14.5 показана сумма 2 s - и 2 p z-орбиталей. Она называется sp -гибридизированной орбиталью и обозначается sp z+, поскольку является гибридом, полученным из s -орбитали и 2 p z-орбитали, а её большой положительный лепесток направлен в положительную сторону оси z .
На втором снизу изображении на рис. 14.5 показана разность 2 s - и 2 p z-орбиталей. Один из способов представить себе это состоит в том, чтобы просто отразить 2 p z-орбиталь с верхнего изображения, так чтобы её положительный лепесток смотрел влево, а не вправо, и после этого выполнить сложение. Мы обозначили эту гибридную орбиталь sp z−, поскольку её большой положительный лепесток направлен в отрицательную сторону оси z . Эта орбиталь имеет такую же форму, как sp z+, но ориентирована в противоположную сторону. На нижнем рисунке схематически изображены гибридные атомные орбитали в том виде, в каком они присутствуют в атоме Be. Имеется одно ядро бериллия с двумя гибридными орбиталями, ориентированными по направлениям + z и − z соответственно.
Образуя молекулу BeH 2, бериллий будет использовать две гибридные атомные орбитали для формирования электронных пар на молекулярных орбиталях, связывающих его с двумя атомами водорода. Эти связи схематически изображены на рис. 14.6. В верхней части рисунка показаны два атома водорода: H a и H b , приближающиеся к атому Be. Электроны атомов водорода находятся на 1s-орбиталях 1 s a и 1 s b . У бериллия имеются две гибридные атомные орбитали: sp z−и sp z+, направленные в сторону 1 s -орбиталей водорода. В средней части рисунка схематически показано перекрытие атомных орбиталей. Водородная 1 s a -орбиталь слева образует связывающую МО с гибридной атомной орбиталью sp z−бериллия. Это связывающая МО будет содержать два электрона: один от водорода и один из двух валентных электронов бериллия. Водородная 1 s b -орбиталь справа образует связывающую МО с гибридной атомной орбиталью sp z+. Электрон атома H b и другой валентный электрон атома Be образуют ещё одну ковалентную связь. Это будут σ-связи, поскольку электронная плотность вдоль линии, соединяющей ядра, отлична от нуля. В результате получается линейная молекула BeH 2, изображённая в нижней части рисунка.
Читать дальшеИнтервал:
Закладка:










