Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир
- Название:Абсолютный минимум. Как квантовая теория объясняет наш мир
- Автор:
- Жанр:
- Издательство:Питер
- Год:2015
- Город:Санкт-Петербург
- ISBN:978-5-496-01069-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир краткое содержание
Физика — это сложнейшая, комплексная наука, она насколько сложна, настолько и увлекательна. Если отбросить математическую составляющую, физика сразу становится доступной любому человеку, обладающему любопытством и воображением. Мы легко поймём концепцию теории гравитации, обойдясь без сложных математических уравнений. Поэтому всем, кто задумывается о том, что делает ягоды черники синими, а клубники — красными; кто сомневается, что звук распространяется в виде волн; кто интересуется, почему поведение света так отличается от любого другого явления во Вселенной, нужно понять, что всё дело — в квантовой физике. Эта книга представляет (и демистифицирует) для обычных людей волшебный мир квантовой науки, как ни одна другая книга. Она рассказывает о базовых научных понятиях, от световых частиц до состояний материи и причинах негативного влияния парниковых газов, раскрывая каждую тему без использования специфической научной терминологии — примерами из обычной повседневной жизни. Безусловно, книга по квантовой физике не может обойтись без минимального набора формул и уравнений, но это необходимый минимум, понятный большинству читателей. По мнению автора, книга, популяризирующая науку, должна быть доступной, но не опускаться до уровня читателя, а поднимать и развивать его интеллект и общий культурный уровень. Написанная в лучших традициях Стивена Хокинга и Льюиса Томаса, книга популяризирует увлекательные открытия из области квантовой физики и химии, сочетая представления и суждения современных учёных с яркими и наглядными примерами из повседневной жизни.
Абсолютный минимум. Как квантовая теория объясняет наш мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
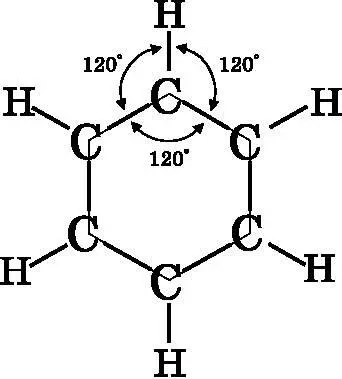
Рис. 18.1. Геометрия молекулы бензола C 6 H 6 . Бензол имеет форму правильного плоского шестиугольника
Где находятся двойные связи?
На рис. 18.2 изображены две возможные структуры с двойными связями. В обоих случаях каждый атом углерода образует четыре связи. Углерод образует три σ-связи — одну с водородом и по одной с двумя соседними атомами углерода. Каждый атом углерода участвует в двойной связи с одним из соседних атомов углерода. Диаграммы, изображённые справа и слева, идентичны, за исключением расположения двойных связей.
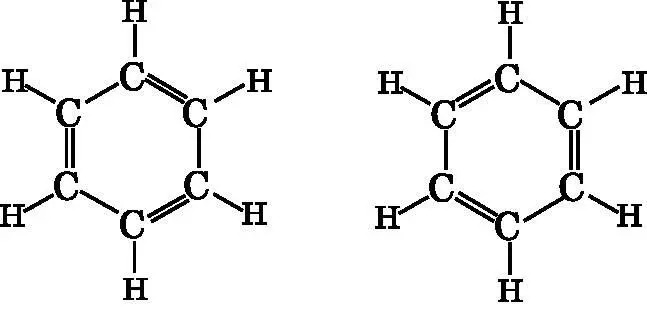
Рис. 18.2. Две возможные конфигурации двойных связей в бензоле. В обеих все атомы углерода образуют по четыре связи
Два момента, относящиеся к связям в молекуле бензола, отражены на рис. 18.2 неверно. При обсуждении двойных связей в главе 14 была приведена табл. 14.1, из которой видно, что двойные углерод-углеродные связи значительно короче одиночных. Двойная связь в этилене имеет длину 1,35 Å против 1,54 Å для одиночной связи в этане. Так что если в бензоле двойные и одиночные связи чередуются, то в нём должны чередоваться короткие и длинные углерод-углеродные звенья. Однако эксперименты убедительно показывают, что бензол является правильным шестиугольником и все углерод-углеродные связи в нём имеют одинаковую длину.
Если закрыть глаза на то, что диаграмма подразумевает неравную длину связей, то вторая проблема состоит в выяснении, какая из двух диаграмм верна — правая или левая? Нет никаких причин предпочесть одну другой. В первых попытках объяснения предполагалось, что связи постоянно переключаются между конфигурациями на правой и левой диаграммах. В результате такого перескакивания получается своего рода усреднённая структура. Эта идея является шагом в правильном направлении, но подлинный ответ, который впоследствии оказался применимым ко многим типам систем, касается природы образующихся молекулярных орбиталей.
Делокализация пи-связей
На рис. 18.3 схематически изображены атомные орбитали, участвующие в образовании молекулярных орбиталей бензола. Сверху нарисованы гибридные атомные орбитали, служащие для создания σ-связей. Каждый атом углерода использует три гибридные sp 2-орбитали для образования трёх σ-связей — одной с атомом водорода и по одной для двух соседних атомов углерода. Образование этих трёх sp 2-гибридизированных атомных орбиталей оставляет каждому атому углерода по одной избыточной p -орбитали. В верхней части рис. 18.3 за плоскость xy принята плоскость, содержащая атомы (плоскость страницы). Тогда у каждого атома углерода остаётся неиспользованная p z-орбиталь, расположенная перпендикулярно плоскости страницы. Эти орбитали изображены в нижней части рисунка. Положительные и отрицательные лепестки орбиталей расположены над и под плоскостью кольца. На этой диаграмме длина связи между атомами углерода преувеличена, а ширина p z-орбиталей приуменьшена, чтобы сделать изображение более понятным. В действительности же p z-обитали перекрываются, что в более реалистичных пропорциях показано на рис. 14.15.
Эти шесть атомных p z-орбиталей объединяются и образуют молекулярные орбитали. Без нарушения принципа Паули эти атомные орбитали могут содержать максимум 12 электронов. Поэтому шесть атомных орбиталей образуют суперпозицию и дают шесть молекулярных орбиталей (МО), которые также могут вмещать максимум 12 электронов. Эти МО не связаны с конкретным атомом или даже конкретной парой атомов. Они растянуты на всю систему из шести атомов углерода.
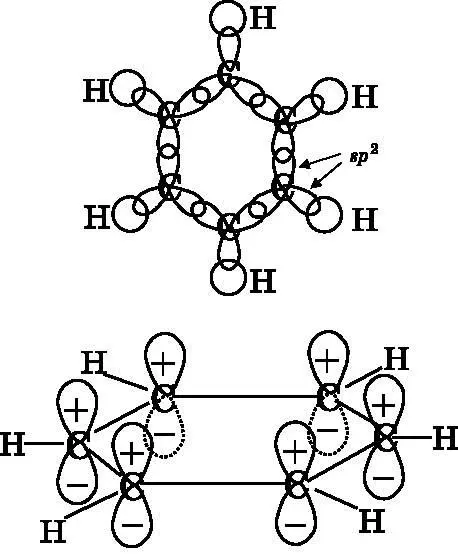
Рис. 18.3. Вверху: бензол и σ- связи. Каждый атом углерода образует три связи, используя три sp 2 -орбитали, лежащие в плоскости xy. У каждого атома углерода остаётся pz-орбиталь, перпендикулярная плоскости бензольного кольца. Внизу: p z -орбитали углерода имеют положительные и отрицательные лепестки, которые расположены над и под плоскостью кольца. Длина связей здесь преувеличена, а ширина лепестков, наоборот, приуменьшена для того, чтобы иллюстрация стала понятнее. Лепестки соседних p z -орбиталей перекрываются
Обсуждая молекулу водорода в связи с рис. 12.6, мы выяснили, что две атомные орбитали в ней объединяются и образуют две молекулярные орбитали — связывающую и разрыхляющую. В главе 13 мы разбирались с более крупными двухатомными молекулами, такими как F 2, O 2и N 2. У этих элементов каждый атом имеет три p -орбитали, а шесть атомных орбиталей при объединении дают шесть π-МО — три связывающие и три разрыхляющие (см. рис. 13.5). Некоторые из этих двухатомных π-МО будут вырожденными, то есть обладающими одинаковой энергией.
Связывающие и разрыхляющие молекулярные орбитали
В бензоле шесть атомных p z-орбиталей объединяются и образуют три связывающие МО и три разрыхляющие МО, как показано на рис. 18.4. Шесть 2 p z-орбиталей углерода, по одной у каждого атома, обладают одинаковой энергией. Это обозначено шестью близко расположенными линиями в левой части рис. 18.4. Они объединяются и образуют шесть МО с энергетическими уровнями, изображёнными в правой части рисунка. Энергия трёх из этих МО ниже, чем у атомных p z-орбиталей, — это связывающие МО. Другие три МО обладают энергией более высокой, чем у атомных орбиталей, — это разрыхляющие МО.
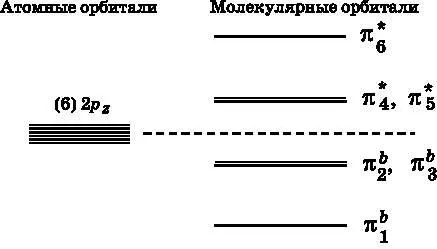
Рис. 18.4. Слева: бензол содержит шесть атомов углерода, каждый с 2p z -орбиталью. Они обладают одинаковой энергией, что обозначено шестью близко расположенными линиями. Справа: шесть p z -орбиталей объединяются и образуют шесть молекулярных π-орбиталей: три связывающие (b) и три разрыхляющие ( * )
На рис. 18.5 изображены энергетические уровни связывающих и разрыхляющих орбиталей с размещёнными на них шестью электронами, по одному от каждого атома углерода. Мы помещаем электроны на низший доступный в соответствии с принципом Паули энергетический уровень. Принцип Паули (см. главу 11) утверждает, что на одной орбитали могут находиться не более двух электронов и что они должны иметь противоположные спины (один ориентирован вверх, другой — вниз). Первые два электрона занимают МО с наименьшей энергией. Следующие две МО имеют одинаковую энергию, что изображено двумя близко расположенными линиями. Каждую из этих МО занимают два электрона. Эти три МО, заполненные шестью электронами, являются π-связывающими. π-разрыхляющие МО остаются пустыми.
Читать дальшеИнтервал:
Закладка:










