Михаил Бармин - Общая и Неорганическая химия с примерами решения задач
- Название:Общая и Неорганическая химия с примерами решения задач
- Автор:
- Жанр:
- Издательство:Литагент Selfpub.ru (искл)
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Бармин - Общая и Неорганическая химия с примерами решения задач краткое содержание
Общая и Неорганическая химия с примерами решения задач - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Основные положения теории э.д.:
электролиты в водных растворах диссоциируют (распадаются) на ионы;
под действием электрического тока (+) заряженные ионы движутся к катоду, (-) заряженные (анионы) – к аноду;
диссоциация – обратимый процесс.
Впоследствии эта теория была развита в работах Каблукова и Кистяковского. На основании химической теории растворов Менделеева Каблуков впервые выдвинул гипотезу о гидратации ионов. Рассматривая механизм электролитической диссоциации следует остановиться на 2-х механизмах взаимодействия в растворе, I-ион дипольное взаимодействие, II-диполь-диполь-ное взаимодействие.
Рассмотрим процесс электролитической диссоциации на примере иондипольного взаимодействия
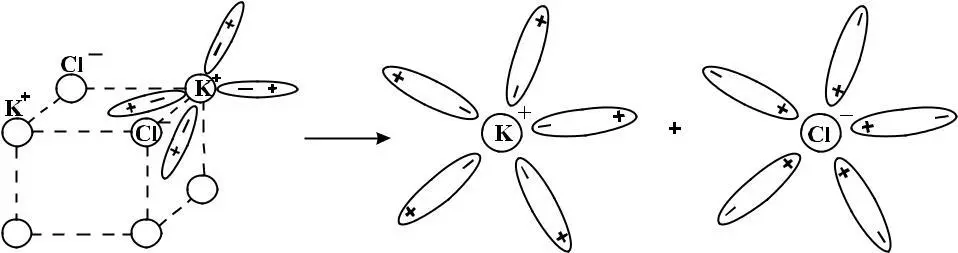
При помещении в водный раствор кристаллического ион-нопостроенного соединения полярные молекулы воды ориентируются противоположными концами относительно ионов кристалла. Происходит ослабление ионной связи с последующим разрывом. Следующий процесс заключается в образовании относительно (+) или (-) заряженных ионов, сольватных оболочек. При сольватации происходит образование слабых межмолекулярных химических связей.
Таким образом, сольватация или гидратация представляют собой основную причину электролитической диссоциации. Отсюда становится понятным физический смысл изотоничес-кого коэффициента: число ионов на которые распадается элек-тролит
HCl
H + + Cl -
i → 2
CaCl 2
Ca 2+ + 2Cl -
i → 3
Типы диссоциации. Сила электролита
Степенью э.д. называется отношение числа молекул, диссо-циирующих в растворе к общему числу молекул.
α = n/N, где n – число диссоциирующих молекул; N – общее число молекул в растворе
Условно считают, что если α > 30 % – то сильный электролит; α ÷ 2-30 % – электролит средней силы; α < 2 % – слабый электролит.
Существует зависимость между степенью э.д. и значением
изотонического коэффициента:
i = 1 + α (k – 1); где k – число ионов
Степень диссоциации зависит от:
природы и полярности растворителя (чем больше полярность тем выше степень диссоциации)
от природы и полярности вещества
от температуры (с повышением температуры степень диссоциации изменяется (уменьшается для сильных электролитов; для слабых – проходит через максимум)
от концентрации (с повышением концентрации степень диссоциации уменьшается)
при добавлении одноименных ионов степень диссоциации уменьшается в соответствии с принципом Ле-Шателье

СH3COOH <=====> CH3COO– + H + CH3COO-
Сильные электролиты:
все растворимые соли, щелочи, минеральные кислоты:
HNO3, H2SO4, HCl, HBr, HJ, HClO4, HClO3, HMпO4
Слабые электролиты: слабые минеральные кислоты: HF,
HCN, H2CO3, H2SiO3↓, H3PO4, HNO2, H2SO3, HClO2, HClO, HN3 и др., органические кислоты (муравьиная, уксусная), ор-
ганические амиды, гидроксид аммония (NH4OH). Fe(OH)2, Fe(OH)3, Cu(OH)2, Zn(OH)2, органические спирты, фенолы, вода, нерастворимые соли (ВаSО4, AgCl), сульфиды, СаСО3
Константы диссоциации
СH3COOH CH3COO– + H+
[CH3COO~] [Н+] Кдис.= –
[CH3COOH]
Константа равновесия представляет собой константу электролитической диссоциации. Константа диссоциации зависит: от природы и полярности растворителя, от природы электролита, от температуры, НО НЕ ЗАВИСИТ от концентрации раствора
1) H2CO3
H+ + HCO3
~
K1
~ 4 • 10-7
2) НСО 3
H+ + CO3
2-
K2
~ 5 • 10-11
К1 > K2 в 8000 раз
Процесс э. д. двух, трех-, и более основных кислот, а также
> К2
К3 > …
общем случае константа э.д. по двум стадиям может быть записана следующим образом:многокислотныхоснованийидет ступенчато, причем К
H2CO3 <======> 2H+ + CO32~ Kдис = K1 • K2 = [H+] 2[CO3-2]

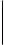
К равн .

[H2CO3]
Таким образом, в общем случае, для ступенчатого процесса э.д., общая константа равняется произведению констант по стадиям:
К = K1 • K2 • K3 … для H3PO4 K1 = 6 • 10-3 K2 = 5 • 10-8 K3 = 10-13
Таким образом, для разбавленных растворов электролитов справедливым является закон действия масс, который описывает количественно процесс э.д. по стадиям.
Рассмотрим э.д. слабого электролита:

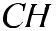
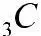
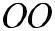
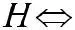
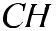
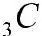
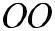

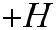
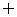
,
где С – исходная концентрация; α – степень э.д.
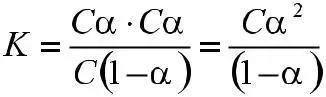
закон
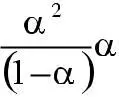

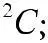
разбавления Оствальда,
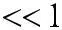
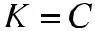

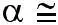
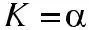
Таким образом, при понижении концентрации электролита степень э.д. увеличивается.
Читать дальшеИнтервал:
Закладка:










