Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться
- Название:Против часовой стрелки. Что такое старение и как с ним бороться
- Автор:
- Жанр:
- Издательство:Альпина нон-фикшн
- Год:2020
- Город:Москва
- ISBN:978-5-0013-9314-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться краткое содержание
В своей книге биолог и научный журналист Полина Лосева выступает в роли адвоката современной науки о старении и рассказывает о том, чем сегодня занимаются геронтологи и как правильно интерпретировать полученные ими результаты. Кто виноват в том, что мы стареем? Что может стать нашей защитой от старости: теломераза или антиоксиданты, гормоны или диеты? Биологи пока не пришли к единому ответу на эти вопросы, и читателю, если он решится перейти от размышлений к действиям, предстоит сделать собственный выбор.
Эта книга станет путеводителем по современным теориям старения не только для биологов, но и для всех, кому интересно, как помочь своему телу вести неравную борьбу со временем.
Против часовой стрелки. Что такое старение и как с ним бороться - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Постройкой и починкой матрикса занимаются клетки, которые в нем живут. Более того, для некоторых из них это единственная задача. Так работают, например, фибробласты – клетки волокнистой соединительной ткани, из которой построены внутренние слои кожи, прослойки между органами, суставные связки и частично стенки сосудов. В их должностные обязанности входит: размножаться, расползаться по ткани и производить молекулы матрикса. Повзрослев, они перестают делиться и становятся либо фиброцитами, которые поддерживают матрикс в рабочем состоянии, либо фиброкластами, которые разрушают поврежденные участки ткани.
Но и эти клетки стареют. А значит, их митохондрии работают все хуже, и запасов энергии не хватает даже на поддержание внутреннего спокойствия, не говоря уж о внешнем. Несмотря на то что каркасные белки матрикса и без того обновляются редко [219] Cole M. A., Quan T., Voorhess J. J., Fisher G. J. Extracellular matrix regulation of fibroblast function: redefining our perspective on skin aging // Journal of Cell Communication and Signaling. 2018 Feb; 12: 35–43.
– время полужизни молекулы коллагена в коже составляет около 15 лет, – стареющие клетки производят его все меньше и меньше [220] Mavrogonatou E., Pratsinis H., Papadopoulou A., Karamanos N. K., Kletsas D. Extracellular matrix alterations in senescent cells and their significance in tissue homeostasis // Matrix Biology. 2019 Jan; 75–76: 27–42.
. Вместо этого они выделяют белки SASP ("вредные советы"), среди которых немало ферментов для разрушения матрикса. Поэтому длинные белковые нити с возрастом замещаются более короткими, хаотично сшитыми друг с другом.
Та же судьба ждет и гиалуроновую кислоту. В отличие от каркасных белков, она обновляется очень быстро – около трети всех молекул человеческого тела за день, – но и ее нити в старом матриксе становятся существенно короче, чем в молодом. Все это вызывает фиброз, то есть разрастание соединительной ткани, которая постепенно замещает другие ткани в органах. Клеток становится [221] См. п. 71.
меньше, матрикса – больше, а короткие перекрестно сшитые белки делают его более жестким.
Нарастающий с возрастом в ткани хаос на руку клеткам опухоли: разрушенные волокна больше не тормозят их движение и размножение. Таким образом старый матрикс стимулирует развитие опухолей. И это позволяет объяснить парадоксальный факт, с которым мы встречались в первой части книги: люди, пережившие противоопухолевую терапию, стареют быстрее других. С точки зрения ткани это совершенно логично: возникает опухоль, организм облучают, под действием радиации опухоль умирает, а оставшиеся в живых клетки стареют, матрикс деградирует и в результате возникают условия для роста новой опухоли. Замкнутый круг из клеток и матрикса, которые стареют бок о бок, и порождает чудовищ.
Изменения в нише не проходят бесследно и для ее здоровых обитателей. Обломки матрикса привлекают в ткань иммунные клетки для разборки завалов, и начинается воспаление – битва иммунитета с внеклеточным мусором, в которой неизбежно страдают и мирные жители: им достается порция токсинов, которыми травят врага. Да и сигналов поддержки от старого матрикса поступает гораздо меньше. Поэтому, например, если поместить культуру молодых фибробластов на полуразрушенный матрикс, они начнут размножаться хуже.
Обратная процедура, кстати, тоже работает [222] Segel M. et al. Niche stiffness underlies the ageing of central nervous system progenitor cells // Nature. 2019 Aug; 573: 130–134.
: можно [223] Choi H. R. et al. Restoration of senescent human diploid fibroblasts by modulation of the extracellular matrix // Aging Cell. 2010 Nov; 10 (1): 148–157.
заставить фибробласты 80-летних людей размножаться, если пересадить их на подушку из длинных нитей гиалуроновой кислоты. Это могло бы стать хорошей стратегией омоложения – очищать матрикс от накопленного мусора или просто вводить новые, не тронутые временем молекулы. Однако тесная связь между клетками и межклеточным веществом мешает "омолодить" всю ткань разом. Если мы научимся очищать матрикс, избавлять его от углеводных остатков и удлинять нити, старые клетки все равно не смогут поддерживать его в молодом состоянии. А если введем в старую ткань молодые клетки, они неизбежно состарятся на руинах матрикса.
Потерянное поколение
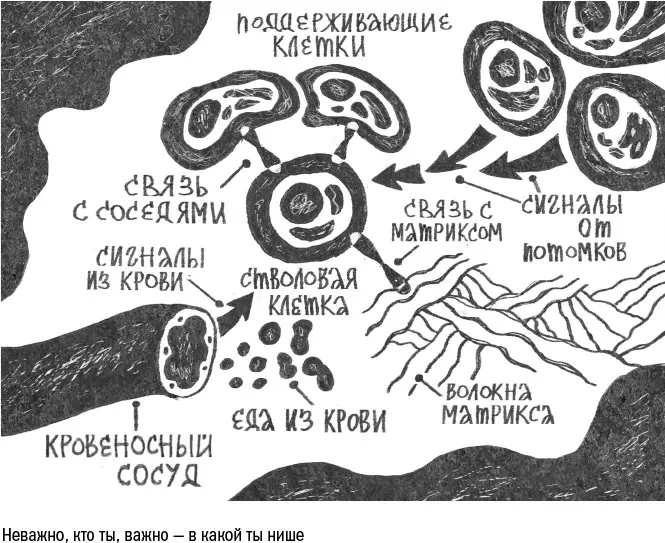
Среди множества клеток в ткани есть и те, чье старение особенно опасно, – это стволовые клетки. Подобно тому, как мы бережем детей от опасностей и тревог, ткань прячет свои стволовые клетки в самом безопасном месте, куда не проникают токсичные вещества и иммунные клетки. В коже их ниша находится под слоями остальных клеток, в стенке кишечника – на самом дне крипты (впячивания), в мышцах – на периферии, подальше от сокращающихся волокон.
Жизнь стволовых клеток устроена следующим образом: по умолчанию – покой, по сигналу – деление. Чаще всего клетки делятся асимметрично, то есть одна остается стволовой, а другая становится клеткой-предшественником, то есть активно размножается, поставляя новобранцев в клеточные ряды.
Асимметрию эту обычно задает сама ниша. Например, стволовые клетки кожи сидят на базальной мембране – подстилке из волокон матрикса. И от этой базальной мембраны поступает сигнал: оставаться стволовой, в дифференцировку не вступать. Когда клетка делится надвое, то ее верхняя половина оказывается лишена этих сигналов и теряет свои стволовые свойства. При этом число стволовых клеток в ткани остается неизменным, а ряды клеток-профессионалов пополняются.
Но если орган всерьез поврежден – например, после травмы или тяжелой болезни, – то стволовые клетки получают множество сигналов к размножению и начинают делиться симметрично, то есть дают начало двум одинаковым дочерним клеткам. В условиях травмы они сразу превращаются в клетки-предшественники, уходят в дифференцировку, и запас стволовых клеток постепенно истощается. Это одна из проблем, которая настигает многие ткани в старости: за свою жизнь человек переносит немало болезней и травм, которые заставляют стволовые клетки делиться симметрично.
Сами по себе стволовые клетки в большей степени устойчивы к старению, чем их потомки. В состоянии покоя [224] Pavlidou T. et al. Metformin Delays Satellite Cell Activation and Maintains Quiescence // Stem Cells International. 2019 Apr; 2019: 5980465.
они производят меньше свободных радикалов, синтезируют меньше белков и не копят внутриклеточный мусор, да и аутофагия у них работает эффективнее [225] Solanas G. et al. Aged stem cells reprogram their daily rhythmic functions to adapt to stress// Cell. 2017 Aug; 170 (4): 678–692. E20.
. Но стоит им "проснуться", как обмен веществ ускоряется, начинается деление, и поломок в клетке становится больше. Кроме того, стволовые клетки очень чувствительны к своей нише и стареют в ответ на ее повреждения – например, если окружающий матрикс распадается на маленькие кусочки или если сенесцентные соседи [226] Ahmed A. S. I., Sheng M. H. C., Wasnik S., Baylink D. J., Lau K.-H. W. Effect on aging on stem cells // World Journal of Experimental Medicine. 2017 Feb; 7 (1): 1–10.
заражают их старостью, выделяя SASP.
Интервал:
Закладка:










