Михаил Ермолаев - Биологическая химия
- Название:Биологическая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1974
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Ермолаев - Биологическая химия краткое содержание
В учебнике нашли отражение последние научные данные о ферментах, белках, гормонах, обмене веществ и энергии и т. д. Особое внимание обращено на значение и использование данных биохимии в медицине, в связи с чем расширены разделы, посвященные патологии разных видов обменов и их исследованиям в клинике Включены материалы по наследственным заболеваниям, связанным с нарушением синтеза белка и ферментов.
Учебник написан по программе, утвержденной Министерством здраво" хранения СССР, и предназначен для учащихся фельдшерско-лаборантских отделениях медицинских училищ.
Биологическая химия - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Выделение ферментов также осуществляется методом адсорбции. Адсорбенты типа окиси кремния, активированного угля, гидрата окиси железа, различных синтетических смол и др. обладают способностью обратимо связывать определенные ферменты. Извлечение ферментов при этом достигается промыванием адсорбентов различными специфическими растворителями, которые переводят ферменты в раствор. В настоящее время для выделения ферментов используют хроматографическое фракционирование на колонках с синтетическими смолами, разделение ферментов при помощи электрофореза и др. Получение ферментов в кристаллическом виде достигают путем высушивания очищенных ферментов при низких температурах и вакууме (лиофилизация).
О присутствии ферментов в растворе судят по производимому ими действию. Так, наличие пепсина, который катализирует расщепление белка, определяют по появлению свободных аминокислот, входящих в состав этого белка, о действии каталазы узнают по выделению кислорода при разложении перекиси водорода. Активность фермента выражают количеством распавшегося под действием фермента субстрата или образовавшихся продуктов реакции за единицу времени, в расчете на г ткани или мг белка.
Свойства ферментов
Обратимость действия ферментов
Ферменты в зависимости от концентрации исходных и конечных продуктов реакции могут катализировать как процессы распада, так и процессы синтеза, т. е. каталитические реакции являются обратимыми. Впервые такую способность ферментов отметил А. Я. Данилевский в 1888 г. Он показал, что ферменты желудочного сока, которые расщепляют белки на альбумозы и пептоны, в определенных условиях способны синтезировать из этих промежуточных продуктов более сложные соединения. В работах И. П. Павлова, А. И. Опарина и других авторов было также отмечено, что в организме в зависимости от условий одни и те же ферменты могут катализировать или распад, или синтез необходимых веществ. Однако на основании имеющихся в настоящее время сведений надо признать, что обратимость действия характерна не для всех ферментов. Многие процессы распада и синтеза происходят не только под влиянием различных ферментов, но и разных механизмов.
Температурный оптимум действия ферментов
Ферменты являются термолабильными веществами, т. е. весьма чувствительными к изменению температуры. Установлено, что наивысшую активность ферменты проявляют в очень узком пределе температуры — 40-50°. До этого предела с повышением температуры на каждые 10° скорость катализируемой ими реакции повышается в 2 раза. Выше температурного оптимума активность ферментов снижается, а при температуре 70-80° совершенно прекращается — фермент инактивируется. Это положение относится к большинству ферментов, в том числе ко всем ферментам человеческого организма. Однако некоторые ферменты, например, рибонуклеаза, могут выдерживать кратковременное нагревание. Наряду с этим имеются ферменты некоторых микроорганизмов, которые существуют в воде горячих источников. При понижении температуры (гипотермия) активность ферментов снижается, но не исчезает. Если же создать этим ферментам оптимальные условия для их деятельности, то они снова проявят наивысшую активность. Примером может служить зимняя спячка животных. Эта особенность ферментов нашла широкое применение в хирургической практике, когда для проведения операций на грудной полости организм больного подвергают охлаждению примерно до 22°.
Влияние рН среды
На активность ферментов влияет и определенная концентрация водородных ионов (рН среды).
Для каждого фермента существует определенный узкий предел рН среды, который является оптимальным для проявления его наивысшей активности. Отклонение рН от оптимального вызывает понижение активности фермента и даже его инактивацию.
Оптимальные значения рН среды для некоторых ферментов будут следующими: для пепсина — 1,5-2,5; трипсина — 8,0-8,5, амилазы слюны -6,8-7,4, аргиназы — 9,8, кислой фосфатазы крови — 4,5-5,0, сукцинатдегидрогеназы — 9,0.
Специфичность ферментов
Одним из основных свойств ферментов, отличающих их от других катализаторов, является высокая специфичность, которая заключается в том, что каждый фермент может катализировать одну или несколько близких по своей природе химических реакций. Специфичность основана на строгом соответствии структуры субстрата и того участка фермента, с которым он. соединяется. По образному выражению Э. Фишера, фермент должен подходить к субстрату, как ключ подходит к замку. В последние годы вскрыты более тонкие механизмы взаимодействия субстрата и фермента (Кошленд и др.).
Специфичность ферментов условно подразделяется на несколько видов:
1. Относительной специфичностьюобладают ферменты, которые действуют на соединения, имеющие определенный тип связи. Например, протеиназы гидролизуют все соединения, имеющие в своем составе пептидную связь -СО-NH- , эстеразы расщепляют эфирную связь -О- и т. д. Ферменты, обладающие относительной специфичностью, являются ферментами широкого спектра действия.
2. Групповая специфичностьхарактерна для ферментов, которые действуют на субстраты, имеющие одинаковый тип связи и одну из функциональных группировок. К их числу относятся:
фосфомоноэстеразы, гидролизующие субстраты следующей структуры:
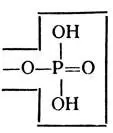
Для их действия обязательным условием является наличие эфирной связи (-О-) и остатка фосфорной кислоты
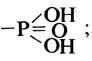
холинэстеразы, в субстратах которых имеются определенные группировки (эфирная связь и остаток холина):
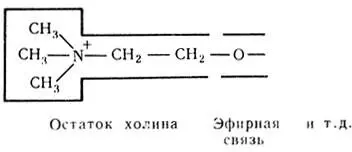
3. Абсолютная специфичностьхарактеризует ферменты, действующие только на один субстрат с вполне определенной структурой. Например: аргиназа расщепляет аргинин на орнитин и мочевину по следующей схеме:
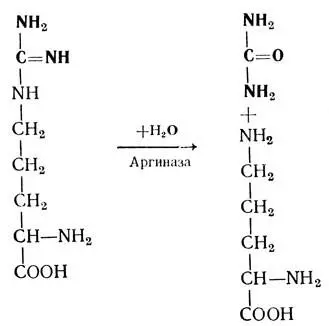
К ферментам, обладающим абсолютной специфичностью, относятся также уреаза, анетилхолинкгераза и др.
Следует выделить в отдельный вид специфичности и стереохимическую , при которой фермент будет действовать только на определенный сгереоиюмер субстрата.
Каталитическая активность
Интервал:
Закладка:






