Эрик Кандель - Расстроенная психика. Что рассказывает о нас необычный мозг
- Название:Расстроенная психика. Что рассказывает о нас необычный мозг
- Автор:
- Жанр:
- Издательство:Литагент Corpus
- Год:2021
- Город:М.
- ISBN:978-5-17-119013-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Эрик Кандель - Расстроенная психика. Что рассказывает о нас необычный мозг краткое содержание
В формате PDF A4 сохранен издательский макет книги.
Расстроенная психика. Что рассказывает о нас необычный мозг - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Генетические исследования болезней, связанных с нарушением фолдинга белка
Плодовая мушка дрозофила представляет собой великолепную беспозвоночную животную модель. Опыты на ней впервые поставил Томас Хант Морган из Колумбийского университета, изучая роль хромосом в наследственности. Затем Сеймур Бензер с ее помощью занялся генами, задействованными в поведенческих реакциях. Он обнаружил, что гены работают сообща в сложных сетях, называемых генетическими путями .
В развитии многих болезней у плодовых мушек и людей участвуют общие гены и даже общие генетические пути. Ученые используют эти общие, эволюционно стабильные черты, чтобы добыть важнейшие сведения о человеческих болезнях, включая неврологические расстройства. Одно из преимуществ использования дрозофил состоит в том, что они сильно ускоряют исследовательский процесс. Если у людей такие патологии, как болезнь Паркинсона, проявляются через десятки лет, то у мушек этот процесс занимает всего несколько дней или недель. Ключевой для болезни Паркинсона мутантный ген, synuclein alpha , или SNCA , впервые идентифицировали именно у плодовой мушки (рис. 7.10).
Болезнь Паркинсона обычно развивается спонтанно, и ее причины до сих пор не установлены. Однако известно о влиянии на ее развитие нескольких факторов, включая гены пациента (определенные генетические варианты предположительно повышают риск развития болезни Паркинсона) и воздействие некоторых токсинов. При редких наследственных формах болезни мутации гена SNCA приводят к избыточному накоплению белка альфа-синуклеина в мозге, к его неправильному фолдингу или и к тому, и к другому. Поскольку в мозге всех страдающих болезнью Паркинсона, даже если она не передалась им по наследству, находят одну из этих белковых аномалий или сразу обе, ученые заключили, что мутантный ген может рассказать о некоторых общих аспектах болезни.
Оказалось, что кодируемый мутантным геном белок и есть основной компонент телец Леви. Таким образом, тельца Леви – это токсичные агрегаты, которые образуются внутри нейронов из-за неполадок фолдинга альфа-синуклеина.
Исследователи вживили мутантный ген SNCA в производящие дофамин нейроны дрозофилы и стали наблюдать за происходящим. Они знали, что дофамин необходим для контроля работы мышц, а из-за недостатка дофамина возникают дрожательные и другие аномальные движения, характерные для болезни Паркинсона. Ученые обнаружили, что вживление мутантного гена мешало производящим дофамин нейронам нормально работать. В результате мушки демонстрировали поведенческие реакции, поразительно напоминающие симптомы болезни Паркинсона у людей 102 .
И у людей, и у мушек есть консервативные молекулярные пути, называемые путями молекулярных шаперонов [80] Молекулярные шапероны – разнородные белки, часто образующие в клетке сложные пути, чтобы “присматривать” за конфигурациями клеточных структур – помогать крупным молекулам правильно сворачиваться, надмолекулярным комплексам правильно собираться, а если что-то пошло не так, то обращать и повторять процесс. Однако фолдинг далеко не всегда требует участия помощников. Самая известная группа шаперонов – белки теплового шока (Hsp), названные так за способность предотвращать, а то и обращать стрессовую (в частности, термическую) денатурацию белков.
. Они помогают белкам принимать положенную им форму, а порой даже “переигрывать” неправильный фолдинг. Помогая белкам правильно сворачиваться, шаперонные пути предотвращают их агрегацию. Ученых заинтересовало, что случится, если дать мушкам больше ассистирующих белков, работающих на этих путях. А вдруг большое количество помощников поддержит правильный фолдинг альфа-синуклеина и жизнедеятельность дофаминергических нейронов?
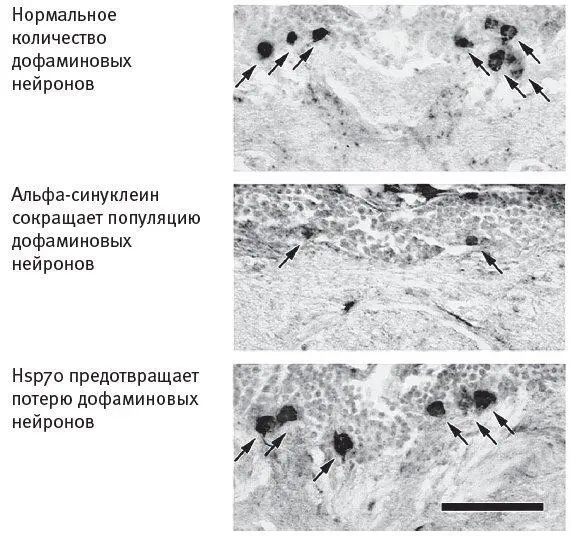
Рис. 7.10.Мозг плодовой мушки с нормальным альфа-синуклеином ( вверху ); с альфа-синуклеином, производимым по инструкции мутантного гена ( в центре ); с таким же мутантным белком, но в присутствии белка-помощника Hsp70, который способствует нормальному рефолдингу ( внизу ). Производящие дофамин нейроны отмечены стрелками.
И действительно, добавление белков-помощников спасало нейроны, производящие дофамин. Как оказалось, белкишапероны защищают организм и от развития двигательных расстройств: мушки с мутантным геном SNCA плохо ползают, однако их сородичи с такой же мутацией и сверхэкспрессией генов шаперонов ползают нормально. Тот же подход работает при моделировании других нейродегенеративных заболеваний (которых уже известно немало) на плодовых мушках, а в случае некоторых патологий и на мышах, что еще раз иллюстрирует ценность животных моделей для изучения человеческих болезней.
Заглядывая в будущее
Болезни Паркинсона, Хантингтона, Альцгеймера и Крейтцфельдта – Якоба, лобно-височная деменция и хроническая травматическая энцефалопатия по-разному влияют на наше мышление и поведение, эмоции и память. Тем не менее мы знаем, что эти и другие нейродегенеративные заболевания имеют общий молекулярный механизм: неполадки в фолдинге белков в конце концов убивают нейроны.
Мы знаем, что функции каждого белка определяются его уникальной формой, которую он принимает в ходе исключительно точного процесса фолдинга. Следовательно, выраженные различия симптомов болезней, связанных с нарушением фолдинга, объясняются изменениями формы специфических белков, отвечающих за определенные функции в мозге. Как мы видели, гибель производящих дофамин нейронов, обусловленная неправильным фолдингом белка, приводит к развитию болезни Паркинсона. Мутации гена, наводняющие его продукт глутаминами, ведут к появлению неправильно свернутых белков, которые комкуются в мозге и вызывают болезнь Хантингтона, а также несколько других заболеваний нервной системы. Самовоспроизводящиеся белки с аномальной пространственной организацией, известные как прионы, вызывают образование токсичных клубков, характерных для болезни Крейтцфельдта – Якоба и родственных расстройств, и могут даже служить инфекционными агентами.
Сейчас нет препаратов, замедляющих дегенерацию мозга, но глубокая стимуляция мозга может “успокаивать” нейронные сети, ответственные за неконтролируемые движения, и облегчать тем самым симптомы болезни Паркинсона. Текущие исследования генетических предпосылок и молекулярных механизмов неврологических расстройств могут снабдить ученых точками приложения усилий по предотвращению или обращению дефектного фолдинга белков. И, как мы видели, генетические исследования животных моделей уже начинают приближать нас к этой цели.
Читать дальшеИнтервал:
Закладка: