Михаил Никитин - Происхождение жизни. От туманности до клетки
- Название:Происхождение жизни. От туманности до клетки
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2016
- Город:Москва
- ISBN:978-5-9614-4350-9
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Никитин - Происхождение жизни. От туманности до клетки краткое содержание
Происхождение жизни. От туманности до клетки - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
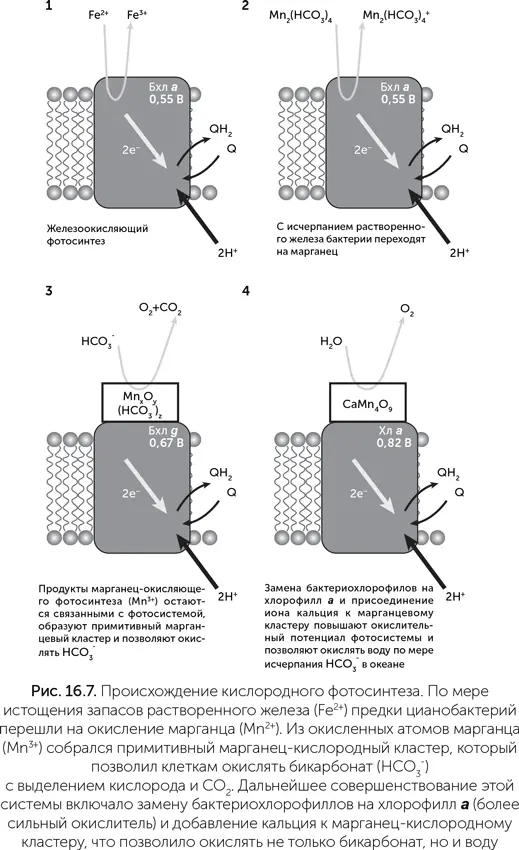
Далее бактериохлорофилл a в составе ФСII был заменен более редокс-активными пигментами, такими как бактериохлорофилл g , а затем и хлорофилл а , для повышения скорости бикарбонатного фотосинтеза. Одновременно совершенствовались системы защиты клеток от выделяемого кислорода. Наконец, по мере истощения запасов СО 2в атмосфере и бикарбонатов в море, к марганцевому кластеру присоединился ион кальция, повысивший его редокс-потенциал и сделавший возможным окисление воды. Так цианобактерии освоили неограниченный источник электронов для фотосинтеза и увеличили продуктивность всей биосферы в несколько раз (Dismukes et al., 2001).
Этот сценарий подтверждается новыми геологическими находками (Johnson et al., 2013). В Южной Африке были найдены морские осадки возраста 2,415 млрд лет, которые сильно обогащены оксидами марганца. Этот возраст примерно совпадает с началом оксигенизации атмосферы и гидросферы планеты. Там же присутствуют зерна легко окисляемого минерала пирита. Следовательно, в этих слоях осаждение марганца происходило не за счет реакций с кислородом. По-видимому, это следы деятельности марганец-окисляющих фотосинтезирующих организмов.
Итак, мы видим, что в течение 1,5 млрд лет после возникновения жизнь постепенно осваивала использование энергии Солнца и новые, все более распространенные восстановители для питания углекислым газом. С появлением кислородного фотосинтеза 2,4 млрд лет назад недостаток восстановителей (железа, водорода, соединений серы) более не ограничивал продуктивность экосистем. Появление в атмосфере кислорода, ядовитого для многих древних групп микробов, вызвало масштабное вымирание и перестройку экосистем. По-видимому, именно кислородная среда стала толчком к появлению новых организмов с более сложными клетками – эукариот, т. е. клеток с ядром. Только на основе эукариотной клетки стало возможно появление крупных многоклеточных растений и животных. В последней, 18-й главе мы рассмотрим движущие силы и механизмы появления эукариот.
Глава 17
Происхождение компонентов биоэнергетических систем [17]
Огромное разнообразие электрон-транспортных цепей разных организмов, работающих в хемосинтезе, фотосинтезе и дыхании, строится из ограниченного количества блоков. Ферментные комплексы состоят из многих отдельных белковых молекул, причем часто мы можем найти родственные компоненты в комплексах с разными функциями. По последовательностям аминокислот в белках и по составу белковых субъединиц в разных комплексах мы можем проследить их эволюцию. Небелковая часть электрон-транспортных цепей, гемы и хиноны, имеет свою эволюционную историю, которую можно проследить по взаимодействующим с ними белкам.
Разнообразие и происхождение гемов, хлорофиллов и родственных коферментов
Основной пигмент современного фотосинтеза – хлорофилл, как и основной компонент электрон-транспортных цепей, гем, относится к группе веществ, называемых порфиринами. Широкие плоские молекулы порфиринов, содержащие в центре атом какого-либо металла, легко могут окисляться и восстанавливаться, поглощать свет и проводить электроны от одной соседней молекулы к другой. Также они могут быть эффективными катализаторами химических реакций.
К порфиринам, кроме хлорофилла и обычных гемов ( a и b ), относятся некоторые другие молекулы, работающие в клетках, например гем d 1 и сирогем. Последние по сравнению с обычным гемом имеют в своей структуре меньше двойных связей и больше боковых карбоксильных (СООН) групп. Сирогем входит в состав двух типов ферментов: сульфит-редуктаз и ассимиляторных нитрит-редуктаз. Оба этих класса ферментов проводят реакции восстановления с переносом в общей сложности до шести электронов, восстанавливая сульфит до сероводорода и нитрит до аммиака. Гем d 1 входит в состав единственного фермента, диссимиляторной нитрит-редуктазы, которая восстанавливает нитрит до оксида азота, NO, с переносом одного электрона.
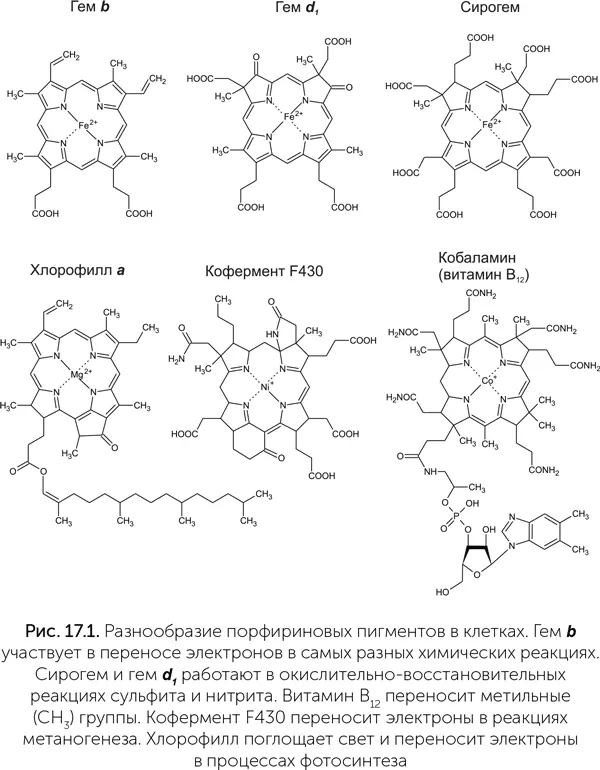
Более далекие родственники гемов – кофермент F430 и витамин В 12. Кофермент F430 содержит никель и участвует в процессах метаногенеза. Ни у каких других организмов, кроме архей-метаногенов, он не встречается. Витамин В 12же есть почти у всех организмов, содержит кобальт и участвует в реакциях переноса метильных групп. Его строение несколько отличается от типичных порфиринов: в нем отсутствует один из метиленовых мостиков, соединяющих малые кольца в большое порфириновое кольцо. Вместо этого два малых кольца из четырех связаны напрямую; такие молекулы называются «коррины» (рис. 17.1).
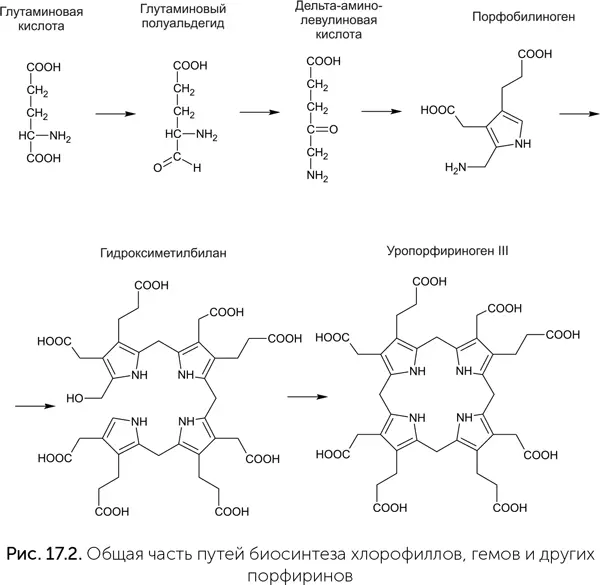
Синтез всех порфиринов и витамина В 12начинается одинаково (рис. 17.2). Глутаминовая кислота восстанавливается до альдегида, потом аминогруппа переносится на конец молекулы, и получается дельта-аминолевулиновая кислота. Две ее молекулы реагируют друг с другом, образуя порфобилиноген – вещество с пятичленным пиррольным кольцом в молекуле. Затем четыре молекулы порфобилиногена объединяются в цепочку (гидроксиметилбилан), которая замыкается в кольцо (уропорфириноген III). Отсюда пути синтеза разных порфиринов расходятся.
Известно несколько разных путей синтеза гемов и витамина В 12из уропорфириногена III. Их эволюционные отношения долго не удавалось распутать. Лишь недавно, с описанием всех ферментов и реакций пути синтеза витамина В 12у архей (Moore et al., 2013), удалось разобраться в этом разнообразии. Эти цепочки реакций делятся на две группы: аэробные (работающие в присутствии кислорода) и анаэробные . Их главное различие состоит в том, что в аэробных путях синтеза гема и В 12атом металла вставляется в молекулу на последней стадии, а в анаэробных – ближе к началу и участвует в последующих реакциях. Смысл этих различий, видимо, в том, что металлсодержащие промежуточные продукты в кислородной среде могут легко окисляться и быть источниками повреждающих активных форм кислорода.
Превращение уропорфириногена III в гемы и хлорофиллы сводится к восстановлению части двойных связей, вставке железа или магния и «обработке краев напильником» – отщеплению или укорочению боковых цепей. В аэробных путях синтеза порядок реакций с боковыми цепями может различаться в разных организмах (Dailey et al., 2015). У многих архей, а также у части анаэробных бактерий (сульфатвосстанавливающих, например Desulfovibrio, и некоторых денитрифицирующих) обнаружен, по-видимому, древнейший путь синтеза гема (Bali et al., 2011). Гемы b и d 1 у них образуются из сирогема, причем на всех стадиях превращений атом железа остается в центре молекулы. По-видимому, это означает, что и в эволюции сирогем был предшественником этих гемов (рис. 17.3).
Читать дальшеИнтервал:
Закладка:







