Игорь Дмитриев - Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи
- Название:Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1980
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Игорь Дмитриев - Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи краткое содержание
Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Перестановки электронов внутри системы А или В мы, следуя работе [48], будем обозначать далее буквой R, прочие перестановки (между А и В) — буквой Q. Соответственно можно различать параметры J QИ J R.
Основным допущением теории Гайтлера является предположение, что J 2 Qгораздо меньше J 2 R, и потому J 2 Qможно пренебречь, учитывая только члены, линейные по J Q. Такое допущение для равновесного межъядерного расстояния может оказаться довольно грубым. Поэтому можно было надеяться лишь на то, что теория даст правильный порядок величины энергии диссоциации. Упрощая секулярное уравнение (3.8), Гайтлер получил для энергии диссоциации выражение
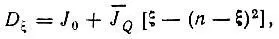 (3.9)
(3.9)
где квантовое число ξ пробегает значения 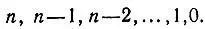
Параметр J 0представляет собой кулоновский интеграл, а 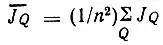 — среднее значение обменного интеграла, характеризующее взаимодействие А и В.
— среднее значение обменного интеграла, характеризующее взаимодействие А и В.
Согласно Гайтлеру, в рассматриваемом случае, как и в случае взаимодействия двух атомов водорода, величина 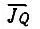 отрицательна и при не слишком малых расстояниях преобладает над J 0
отрицательна и при не слишком малых расстояниях преобладает над J 0 [6] При уменьшении межъядерного расстояния содержащийся в J 0 член отталкивания атомных ядер возрастает и становится определяющим.
. Кроме того, можно надеяться, что для различных взаимодействующих атомов рассматриваемые интегралы имеют не только одинаковый (отрицательный) знак, но и общий порядок величины. Тогда в зависимости от знака коэффициента 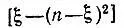 при обменном интеграле
при обменном интеграле 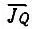 следует ожидать либо притяжения атомов вплоть до образования ими устойчивой молекулы, либо их отталкивания. В первом случае указанный множитель должен быть положительным, во втором — отрицательным. В частности, основному состоянию соответствует ξ = n и наибольшая прочность связи, так как при этом D ξпринимает наименьшее (с учетом знака) значение:
следует ожидать либо притяжения атомов вплоть до образования ими устойчивой молекулы, либо их отталкивания. В первом случае указанный множитель должен быть положительным, во втором — отрицательным. В частности, основному состоянию соответствует ξ = n и наибольшая прочность связи, так как при этом D ξпринимает наименьшее (с учетом знака) значение:
 (3.10)
(3.10)
Обсуждаемое состояние (ξ = n) коррелирует с теми термами изолированных А и В, для которых спиновые моменты электронов одной системы (А или В) антипараллельны спиновым моментам другой (В или А).
Кроме состояния с ξ = n могут существовать и состояния с меньшими ξ. Например, в таких соединениях азота, как N 2, NH 3и т. п., имеется по три валентных электрона в незамкнутой оболочке атома N. Эти три электрона могут соответствовать квартетному состоянию, причем именно это состояние наивысшей мультиплетности по спину является основным для изолированного атома. При учете взаимодействия двух атомов азота или одного атома азота с тремя атомами водорода множитель при 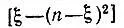 может принимать четыре значения: +3, +1, -3, -9, которые определяются значениями ξ = 3, 2, 1,0.
может принимать четыре значения: +3, +1, -3, -9, которые определяются значениями ξ = 3, 2, 1,0.
Гайтлер не определял численное значение J Q, он лишь качественно представил кривые энергии взаимодействия D ξ(R) для молекулы N 2(рис. 12).
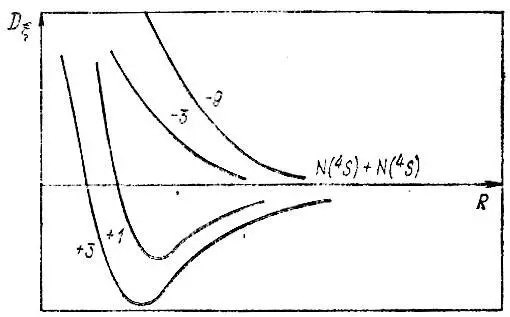
Рис. 12. Кривые энергии взаимодействия атомов D ξ(R) для молекулы N 2по Гайтлеру
Независимо от Гайтлера аналогичный подход был развит Лондоном, работы которого [60, 61] отличались, по существу, лишь более детальным изложением вопроса, а также более подробным исследованием химических примеров. В частности, им была установлена связь между валентностью атома и его спектроскопической мультиплетностью (магнитной тонкой структурой). По определению Лондона, валентность атома равна полному электронному спину в единицах h/ 2и поэтому на единицу меньше мультиплетности рассматриваемого атомного состояния [61, с. 49]. Кроме того, Лондон указал на возможность спектроскопического определения кратности ковалентной химической связи.
Пусть атомы характеризуются валентностью V 1и V 2и, следовательно, мультиплетностью по спину M 1= V 1+ 1 и М 2= V 2+ 1. Если при взаимодействии атомов связываются по одной валентности каждого атома, то в молекуле остается V(1) = V 1+ V 2— 2 свободных валентностей и ее спиновая мультиплетность M(1) = M 1+ M 2-3 (в круглых скобках указана кратность связи). В случае двойной связи V(2) = V 1+ V 2— 4 и М(2) = M 1+ М 2— 5.
В общем случае j-кратной связи
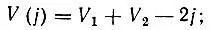 (3.11)
(3.11)
 (3.12)
(3.12)
Равенство j нулю означает отсутствие валентной связи.
Изложенный выше формализм, развитый независимо Гайтлером и Лондоном в 1927-1928 гг., интерпретирует понятие валентности как число спиновых моментов, спаренных при образовании молекулы. Однако в рамки этого формализма не укладывались молекулы, основное состояние которых является триплетным (В 2, O 2и др.)" Так, в случае молекулы В 2спаривания спиновых моментов электронов не происходит и, согласно (3.11), химическая связь вообще не должна образовываться. В связи с этим можно было бы повторить слова Хаксли, видевшего великую трагедию науки "в умерщвлении прекрасной теории мерзким фактом". Однако приведенные примеры, на наш взгляд, указывают не на ошибочность концепции спин-валентности, а на необходимость дополнения ее концепцией орбитальной валентности*. Идеи, позволившие осуществить такое обобщение [7] В 30-х годах употребляли также термин l (или р)- валентность.
были впервые высказаны Гайтлером в июне 1929 г. [49] и явились естественным обобщением созданной им и Лондоном теории ковалентной связи.
"Прежняя теория валентности,- писал Гайтлер,- рассматривала лишь те случаи, когда имело место только обменное вырождение. Однако для галогенов и элементов группы кислорода [8] Также и для других р-элементов.- Прим. авт.
это уже не верно. Их основным состоянием является Р-состояние, что говорит о наличии вырождения по магнитному квантовому числу. Расчеты автора показывают, что учет этого вырождения приводит к величине энергии связи между моментами количества движения l (bahnimpulsen l) того же порядка, что и энергия обмена. Вероятно, эта энергия также ответственна за образование молекул. Кроме рассматривавшейся ранее спин-валентности существует еще другой вид валентности (line zweite Arte Valenz) - l -валентность для атомов с l>0 . При этом могут насыщаться только валентности одинакового вида. Вероятно, здесь мы имеем более сложные соотношения, чем в случае спиновых валентностей" [49, с. 547]. В качестве примера использования концепции орбитальной валентности обратимся к молекуле В 2. Атом бора в основном состоянии характеризуется электронной конфигурацией 1s 22s 22p и термом 2Р. В соответствии с этим электронную структуру молекулы В2 можно было бы описать двухэлектронной функцией Гайтлера-Лондона, составленной, однако, из р -орбиталей атома бора [9] При этом можно исключить из рассмотрения 1s- и 2s-электроны, полагая, что они образуют "замороженный" остов.
. Спариванию одноэлектронных спиновых моментов соответствовало бы расщепление молекулярного терма на два — синглетный и триплетный — согласно схеме
Интервал:
Закладка:









