Игорь Дмитриев - Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи
- Название:Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1980
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Игорь Дмитриев - Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи краткое содержание
Квантовая химия — ее прошлое и настоящее. Развитие электронных представлений о природе химической связи - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Наиболее сложной проблемой было определение энергетической последовательности одноэлектронных состояний в молекуле. Поскольку о теоретическом расчете в то время не могло быть и речи, то Малликену пришлось использовать различную информацию (в основном экспериментальную): потенциалы ионизации, энергии электронных переходов и их интенсивности, эмпирически установленные правила отбора и т. п. Кроме того, он ввел дополнительное предположение о том, что число σ-, π-, δ-...электронов при переходе от объединенного атома к разделенным не изменяется. Однако такой переход неоднозначен, во-первых, потому, что в процессе разъединения могут получиться атомы в различных состояниях, а во-вторых, потому что объединенный атом может "расщепляться различными спобами" (например, 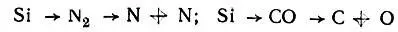 и т. д.).
и т. д.).
Ввиду неоднозначности указанного перехода существенным является использование принципа изоэлектронности, а также предположения о сохранении числа σ-, π-... электронов.
Заканчивая обсуждение работ Хунда и Малликена, остановимся на их оценке. Прежде всего следует отметить, что Хундом и Малликеном была дана вполне удовлетворительная интерпретация молекулярных спектров на основе квантовой механики. Была прослежена связь молекулярных спектров с атомными. Вместе с тем был достигнут прогресс в понимании квантовомеханической природы валентности атомов и удалось объяснить некоторые особенности их химического поведения. Существенным элементом теории Хунда-Малликена была идея одноэлектронного приближения в ее простейшей формулировке. Все эти результаты составляют непреходящую ценность их работ.
В то же время следует отметить, что метод МО [26] Термин "орбиталь" впервые появился, по-видимому, в 1932 г., в работе Малликена [66]. Сначала же Хунд использовал термин "bahn", a Малликен — "orbit".
выступает р их исследованиях преимущественно как качественная полу-^мпирическая теория молекулярных спектров. Описание молекул велось в терминах энергий и мультиплетностей термов, а не волновых функций, которые определяют распределение электронной плотности в системе. Изучались фактически корреляционные диаграммы "термы разделенных атомов — термы объединенного атома", но не детальное изменение энергии отдельных термов (или одноэлектронных состояний) при изменении межъядерного расстояния, характеризующееся потенциальными кривыми взаимодействия атомов.
Иными словами, речь шла об отношении величин, а не о функциональном отношении Е = E(R). Особенность функциональной зависимости состоит в том, что она может включать "особые точки" (например, экстремумы), в которых объект переходит в особое состояние и происходит образование нового качества.
Для того чтобы расширить значение метода Хунда-Малликена, необходимо было прежде всего выйти за рамки чисто качественных полуэмпирических построений и найти способ количественного теоретического расчета. Новой постановке задачи способствовали работы Леннард-Джонса и Герцберга.
Развитие метода МО в работе Леннард-Джонса
Почти сразу после своего возникновения метод Хунда-Малликена подвергся критике со стороны многих исследователей. Так, Герцберг [53] отметил трудности, с которыми сталкивались попытки интерпретировать некоторые экспериментальные факты, например, распад молекулярного иона N 2 +(основное состояние) на атом N (основное состояние) и ион N +(возбужденное состояние) на основе указанного метода.
Более того, он указал путь, позволяющий усовершенствовать эту теорию. Основываясь на идее Гайтлера и Лондона, согласно которой атомные орбитали в молекуле отчасти сохраняют свою индивидуальность, Герцберг предложил в качестве рабочей гипотезы сохранять за отдельными электронами в молекуле те квантовые числа, которыми они характеризовались в разъединенных атомах. Идеи Герцберга нашли поддержку в работе Леннард-Джонеа [58]. Последний считал недопустимым сопоставлять электронам в молекуле квантовые числа состояний, которые не могут быть реализованы. Значительно важнее, по его мнению, знать, что происходит с молекулой при ее диссоциации, чем рассматривать мысленный, физически нереализуемый процесс сжатия молекулярного полиэдрадо слияния ядер [27] К сожалению, эта правильная методологическая установка Леннард-Джонеа не смогла быть применена до конца в методе МО, который оказался не в состоянии даже качественно описать процесс диссоциации молекул.
. Далее он обращает внимание на то, что систематика одноэлектронных состояний по Хунду и Малликену становится слишком сложной для молекул, включающих тяжелые атомы. Даже для атомов, высшие одноэлектронные состояния которых характеризуются главным квантовым числом 2, электронные оболочки пришлось бы обозначать символами 3dπ, 4pσ..., которые нелегко интерпретировать. Наконец, наиболее убедительным аргументом против использования квантовых чисел объединенного атома для описания многоатомной системы, приведенным Леннард-Джонсом, является абсурдность такого подхода в случае кристаллов. Так, куску свинца должен соответствовать объединенный атом с астрономическим зарядом ядра и всего лишь двумя 1s-электронами, двумя 2s-электронами и т. п., хотя ясно, что при образовании кристалла состояния 1s, а также состояния других электронов внутренних оболочек должны оставаться почти неизменными.
Предлагая характеризовать электроны в молекуле квантовыми числами разъединенных атомов, Леннард-Джонс полагал, что принцип Паули можно считать выполняющимся, если, например, два 1s-электрона принадлежат к одному ядру или два — к другому. Более того, он считает возможным в некоторых случаях относить завершенные (замкнутые) оболочки к отдельным атомам. Таким образом, Леннард-Джонс различает атомные и молекулярные уровни даже в молекулах, причем только последние он считает ответственными за образование химической связи, что было, вообще говоря, нетривиальным моментом, так как детального теоретического анализа электронной структуры молекул в то время еще не было сделано.
Далее Леннард-Джонс ввел широко используемые в настоящее время при качественном рассмотрении химической связи диаграммы, связывающие одноэлектронные уровни молекулы с соответствующими уровнями разъединенных атомов. Однако эти диаграммы, отличались от современных отсутствием разрыхляющих состояний. В этом состоит ограниченность подхода Леннард-Джонса, связанная, по нашему мнению, с не вполне правильным пониманием работы Гайтлера и Лондона. В самом деле, исключая разрыхляющие одноэлектронные состояния, Леннард-Джонс исходил из того, что они порождаются одноэлектронными состояниями атомов, одно из которых (или оба) дважды занято, тогда как по Гайтлеру и Лондону взаимодействие таких состояний не должно способствовать образованию химической связи. Однако этот аргумент нельзя признать справедливым по крайней мере по двум причинам.
Читать дальшеИнтервал:
Закладка:









