Михаил Левицкий - Карнавал молекул. Химия необычная и забавная
- Название:Карнавал молекул. Химия необычная и забавная
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2019
- Город:Москва
- ISBN:978-5-0013-9101-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Левицкий - Карнавал молекул. Химия необычная и забавная краткое содержание
В книге рассказано о некоторых драматичных, а, порой, забавных поворотах судьбы как самих открытий, так и их авторов. Кроме того, читатель потренируется в решении занятных задач, что особенно приятно, когда рядом помещена подсказка, а потом и сам ответ.
В отличие от учебника в книге нет последовательного изложения основ химии, поэтому ее можно читать, начиная с любой главы.
Карнавал молекул. Химия необычная и забавная - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Столкнуть эффекты лбами
Для того чтобы выяснить, какой фактор играет решающую роль, необходимо поставить дополнительные эксперименты, при этом большинство исследователей методично меняют один параметр за другим и следят за результатами. Стефан пошел необычным путем: он решил изменить сразу два основных параметра – усилить донорно-акцепторное «взаимовлечение» атомов и одновременно увеличить пространственные затруднения при сближении молекул, т. е. два противоположных эффекта «столкнуть лбами».
В качестве донора Стефан взял молекулу, содержащую атом фосфора Р, который способен проявлять те же свойства, что и атом азота N в предыдущем примере, т. е. играть роль донора. Вокруг атома фосфора находятся бензольные ядра с метильными группами, они нагнетают электроны к фосфору, увеличивая его «донорность». Вторая молекула содержит атом бора В, окруженный фенильными группами, «усеянными» заместителями – атомами фтора F. Они оттягивают от бора на себя электроны и повышают его акцепторую способность. В результате тяга к образованию связи (условно показана на рис. 2.35 в виде стягивающей пружины) у бора и фосфора сильно повышена, однако связь образоваться не может. Пространственные затруднения велики, окружающие громоздкие группы не дают бору и фосфору сблизиться на такое расстояние, чтобы могла образоваться связь.
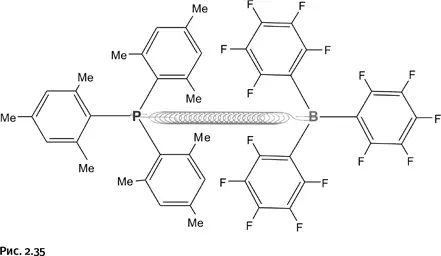
Такая борьба противоположностей не проходит бесследно; на атоме В сосредоточен положительный заряд, и бор находится в нетерпеливом ожидании донора электронов, а атом Р, наоборот, жаждет присоединить к себе что-либо, имеющее положительный заряд. При взаимодействии такого соединения с молекулярным водородом Н 2произошло нечто неожиданное.
Молекулу Н 2можно считать эталоном ковалентной связи, однако находящиеся «в напряженном ожидании» ветвистые молекулы разрывают связь Н – Н, но не ковалентно (т. е. оставив по одному электрону каждому атому Н), а на ионы Н +и Н –, почти так же, как вода «растаскивает» NaCl на Na +и Cl –. В итоге Н +притягивается атомом фосфора, Н –направляется к бору (рис. 2.36).
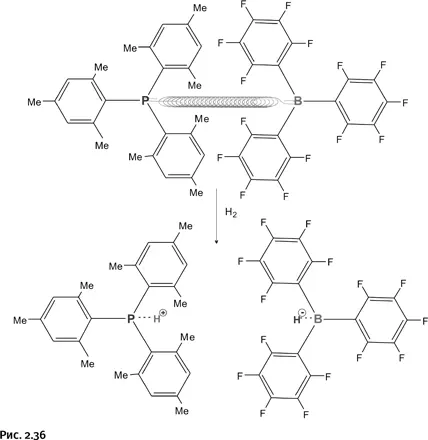
Пожалуй, главное в протекающей реакции то, что после присоединения водорода каждый из двух атомов ( Ри В) «утоляет» свою донорное (или акцепторное) стремление, в результате напряжение спадает, что можно условно изобразить схемой (рис. 2.37).
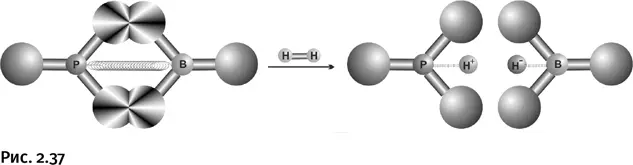
Обе части пары слегка отходят друг от друга, но недалеко, поскольку теперь они несут противоположные заряды, что позволяет им с помощью электростатических сил держаться вместе.
Реакция обратима, при комнатной температуре водород присоединяется, а при 150 °С вновь выделяется, причем это можно даже наблюдать визуально: соединение с ионами водорода бесцветно, но если его нагреть, то выделится Н 2, а оставшееся вещество приобретет красный цвет (рис. 2.38).

Стефан изучил несколько вариантов таких «энергичных» пар (рис. 2.39).
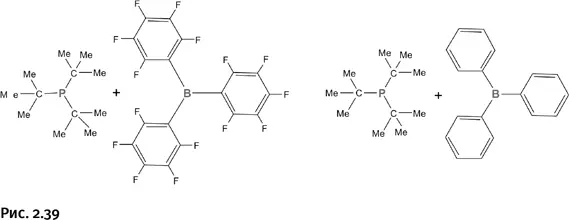
Все они присоединяют молекулярный водород, расщепляя его на ионы. Если принять во внимание, что в наше время постоянно обсуждают вопросы водородной энергетики, то на первый взгляд кажется, что одна из проблем решена – найдена хорошая «емкость» для хранения водорода. Однако для такого применения здесь слишком невыгодное соотношение масс: контейнер в 380 раз тяжелее содержимого (по соотношению атомных масс). Пока что проще и дешевле хранить водород в стальных баллонах под давлением или в созданных недавно ажурных молекулярных контейнерах, о которых рассказано в главе «Наилегчайшие вещества». Тем не менее полученный Стефаном результат впечатляет, разрыв связи Н – Н на ионы при комнатной температуре и в отсутствие металлсодержащих катализаторов – факт весьма необычный.
«Озадаченные» комплексы
Все рассмотренные нами пары с увеличенными пространственными затруднениями Стефан назвал frustrated lewis pairs. Интересно, что помимо пространственных возникли затруднения несколько иного рода. Здесь, пожалуй, уместно будет немного остановиться на вопросах терминологии. Два последних слова из предложенного английского названия особых вопросов не вызывают, это льюисовы пары, зато с первым термином не все гладко. Английское слово frustration (фрустрация) не имеет однозначного перевода на русский язык, приблизительно это огорчение, смущение, недоумение, расстройство, озадаченность, тщетное ожидание. Довольно часто иностранные термины используют в русской научной литературе без перевода, но в нашем случае сложность состоит в том, что из существительного «фрустрация» необходимо сделать прилагательное (как у Стефана), и здесь русский язык начинает сопротивляться. Маловероятно, что кто-то станет употреблять слова «фрустральный» или «фрустратный», они трудно произносимы и неблагозвучны. Наиболее близкое по смыслу слово – «озадаченный», именно оно стоит в заголовке этого раздела главы. Какой именно термин будет выбран окончательно, покажет будущее, важно лишь, чтобы он стал общеупотребимым, иначе в публикациях возникнут путаница и неясность. Интересно, что термин «фрустрация» (в форме существительного) часто используют психиатры для обозначения состояния, предшествующего нервному расстройству. Далее мы будем использовать название «озадаченные льюисовы пары» и соответствующее сокращение ОЛП.
Горизонты ОЛП
Вполне естественно, к изучению соединений со столь интересными свойствами подключились другие исследователи, создавая для ожидаемых льюисовых пар необычные пространственные ситуации. Чтобы о них рассказать более подробно, мы ниже вместо объемистых структурных формул будем использовать более компактное написание молекул: R 3 Pи R′ 3 B.
Одна из идей состояла в том, чтобы связать компоненты таких пар в одну молекулу с помощью гибкого мостика – СН 2–СН 2–, в результате фрагменты с атомами Р и В, находящиеся на концах подобной перемычки, могут свободно поворачиваться. Вполне естественно, соединение приняло такую форму, в которой атомы Р и В расположились по возможности ближе друг к другу, однако эта форма несколько напряжена из-за того, что крупные группы у фосфора и бора приблизились и создали пространственные затруднения. Как только в систему добавили водород, он присоединился по той схеме, что была рассмотрена выше. При этом молекула развернулась таким образом, чтобы отвести друг от друга объемные группы и тем самым снизить напряжение (рис. 2.40).
Читать дальшеИнтервал:
Закладка:









