Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
3Fe + 4Н 2O (пар) = (Fe IIFe 2 III)O 4+ 4Н 2(800 °C)
В ряду напряжений стоит левее водорода, реагирует с разбавленными кислотами НCl и H 2SO 4, при этом образуются соли железа(II) и выделяется водород:
Fe + 2Н += Fe 2++ Н 2↑
(реакции проводятся без доступа воздуха, иначе Fe IIпостепенно переводится кислородом в Fe III).
При действии на железо более сильного окислителя (здесь – азотная кислота) оно сразу переходит в катион Fe 3+:
Fe + 4HNO 3(разб.) = Fe(NO 3) 3+ NO↑ + 2H 2O
Амфотерность железа проявляется только в концентрированных щелочах при кипячении:
Fe + 2NaOH (50 %) + 2Н 2O = Na 2[Fe(OH) 4]↓ + Н 2↑
и образуется осадок тетрагидроксоферрата(II) натрия.
Железо вытесняет (по ряду напряжений) менее активные металлы из растворов их солей:
Fe + CuSO 4= FeSO 4+ Cu↓
Железо медленно окисляется во влажном воздухе (ржавеет ), из-за рыхлости коричневой ржавчины (Fe IIFe 2 III)O 4защитный слой не создается. Процесс ржавления:
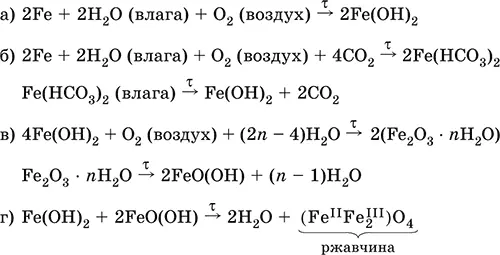
Техническое железо – сплавы железа с углеродом: чугун содержит 2,06—6,67 % С, сталь 0,02—2,06 % С, часто присутствуют другие естественные примеси (S, Р, Si) и вводимые искусственно специальные добавки (Mn, Ni, Cr), что придает сплавам железа технически полезные свойства – твердость, термическую и коррозионную стойкость, ковкость и др.
Доменный процесс производства чугуна составляют следующие стадии:
а) подготовка (обжиг) сульфидных и карбонатных руд – перевод в оксидную руду:
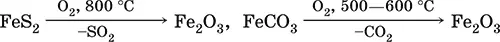
б) сжигание кокса при горячем дутье:
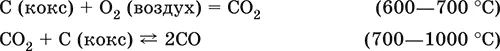
в) восстановление оксидной руды угарным газом СО последовательно (см. рубрики соответствующих оксидов):
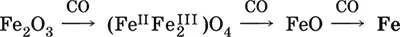
г) науглероживание железа (до 6,67 % С) и расплавление чугуна:
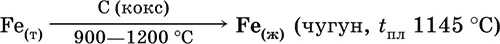
В чугуне всегда в виде зерен присутствуют цементит Fe 2C и графит.
Передел чугуна в сталь проводится в специальных печах (конвертерных, мартеновских, электрических), отличающихся способом обогрева; температура процесса 1700–2000 °C. Продувание воздуха, обогащенного кислородом, приводит к выгоранию из чугуна избыточного углерода, а также серы, фосфора и кремния в виде оксидов. При этом оксиды либо улавливаются в виде отходящих газов (СO 2, SO 2), либо связываются в легко отделяемый шлак – смесь Са 3(РO 4) 2и CaSiO 3. Для получения специальных сталей в печь вводят легирующие добавки других металлов.
Получение чистого железа в промышленности – электролиз раствора солей железа, например:
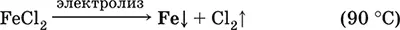
(существуют и другие специальные методы, в том числе восстановление оксидов железа водородом).
Чистое железо применяется в производстве специальных сплавов, при изготовлении сердечников электромагнитов и трансформаторов, чугун – в производстве литья и стали, сталь – как конструкционный и инструментальный материалы, в том числе износо-, жаро– и коррозионно-стойкие.
Оксид железа(II) FeO.Амфотерный оксид с большим преобладанием основных свойств. Черный, имеет ионное строение Fe 2+O 2-. При нагревании вначале разлагается, затем образуется вновь. Не образуется при сгорании железа на воздухе. Не реагирует с водой. Разлагается кислотами, сплавляется со щелочами. Медленно окисляется во влажном воздухе. Восстанавливается водородом, коксом. Участвует в доменном процессе выплавки чугуна. Применяется как компонент керамики и минеральных красок. Уравнения важнейших реакций:
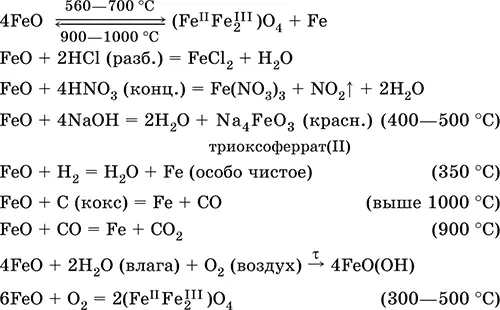
Получение в лаборатории: термическое разложение соединений железа (II) без доступа воздуха:
Fe(OH) 2= FeO+ H 2O (150–200 °C)
FeCO 3= FeO+ СO 2(490–550 °C)
Оксид дижелеза (III) – железа(II) (Fe IIFe 2 III)O 4.Двойной оксид. Черный, имеет ионное строение Fe 2+(Fe 3+) 2(O 2-) 4. Термически устойчив до высоких температур. Не реагирует с водой. Разлагается кислотами. Восстанавливается водородом, раскаленным железом. Участвует в доменном процессе производства чугуна. Применяется как компонент минеральных красок ( железный сурик), керамики, цветного цемента. Продукт специального окисления поверхности стальных изделий ( чернение, воронение). По составу отвечает коричневой ржавчине и темной окалине на железе. Применение брутто-формулы Fe 3O 4не рекомендуется. Уравнения важнейших реакций:
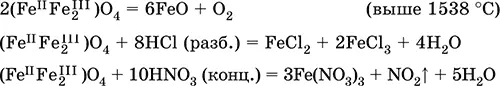
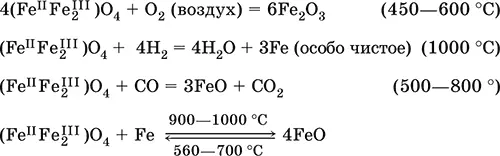
Получение : сгорание железа (см.) на воздухе.
В природе – оксидная руда железа магнетит.
Оксид железа(III) Fe 2O 3.Амфотерный оксид с преобладанием основных свойств. Красно-коричневый, имеет ионное строение (Fe 3+) 2(O 2-) 3. Термически устойчив до высоких температур. Не образуется при сгорании железа на воздухе. Не реагирует с водой, из раствора выпадает бурый аморфный гидрат Fe 2O 3nН 2O. Медленно реагирует с кислотами и щелочами. Восстанавливается монооксидом углерода, расплавленным железом. Сплавляется с оксидами других металлов и образует двойные оксиды — шпинели (технические продукты называются ферритами). Применяется как сырье при выплавке чугуна в доменном процессе, катализатор в производстве аммиака, компонент керамики, цветных цементов и минеральных красок, при термитной сварке стальных конструкций, как носитель звука и изображения на магнитных лентах, как полирующее средство для стали и стекла.
Уравнения важнейших реакций:
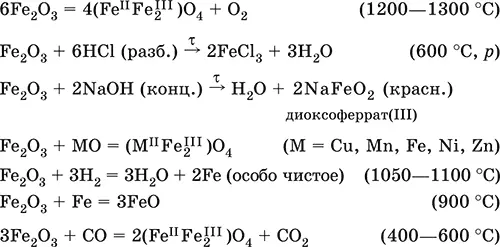
Получение в лаборатории– термическое разложение солей железа(III) на воздухе:
Fe 2(SO 4) 3= Fe 2O 3+ 3SO 3(500–700 °C)
4{Fe(NO 3) 39 H 2O} = 2Fe aO 3+ 12NO 2+ 3O 2+ 36H 2O (600–700 °C)
В природе – оксидные руды железа гематит Fe 2O 3и лимонит Fe 2O 3nН 2O.
Гидроксид железа (II) Fe(OH) 2.Амфотерный гидроксид с преобладанием основных свойств. Белый (иногда с зеленоватым оттенком), связи Fe – ОН преимущественно ковалентные. Термически неустойчив. Легко окисляется на воздухе, особенно во влажном состоянии (темнеет). Нерастворим в воде. Реагирует с разбавленными кислотами, концентрированными щелочами. Типичный восстановитель. Промежуточный продукт при ржавлении железа. Применяется в изготовлении активной массы железоникелевых аккумуляторов.
Читать дальшеИнтервал:
Закладка:










